Свойства растворов ВМС: особенности растворения, реологические свойства, осмос. Устойчивость растворов ВМС
Содержание
- 2. Высокомолекулярные соединения… … вещества, молекулярная масса которых, по данным одних авторов составляет от 104 до 106
- 3. Сходства и различия растворов ВМС и коллоидных растворов
- 4. Растворы ВМС … … лиофильные коллоидные системы, термодинамически устойчивые и обратимые; … молекулярнодисперсные системы, в которых
- 5. Строение (структура) ВМС линейная разветвлённая пространственная Специфические свойства ВМС обусловлены их способностью принимать различные конформации (глобулы,
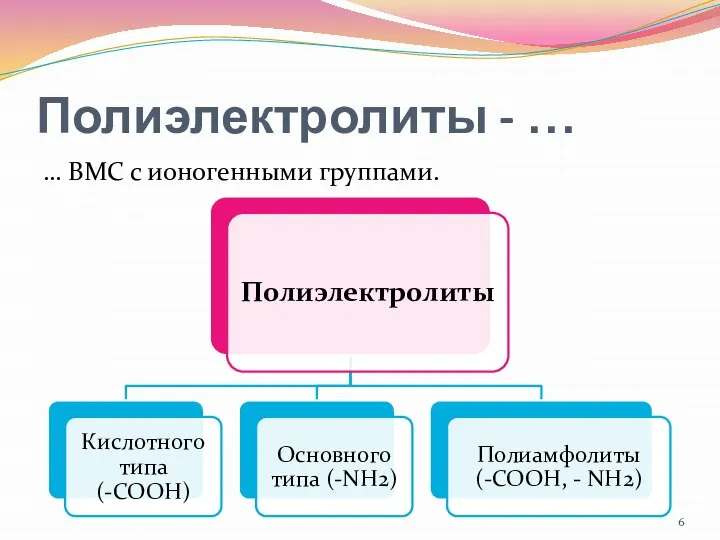
- 6. Полиэлектролиты - … … ВМС с ионогенными группами.
- 7. В растворе полиамфолита устанавливается равновесие Заряд белка зависит от: количества и способности к диссоциации его –СООН
- 8. Особенности растворения ВМС Взаимодействие ВМС с водой начинается с процесса набухания. Набухание – самопроизвольный процесс поглощения
- 9. Ограниченное набухание Сопровождается образованием студня. Студень – пространственная сетка из цепей макромолекул, заполненная НМС. Оно характерно
- 10. Неограниченное набухание Ведёт к растворению ВМС.
- 11. Количественная оценка набухания Степень набухания где m0, V0 – масса и объём ВМС до набухания. m,
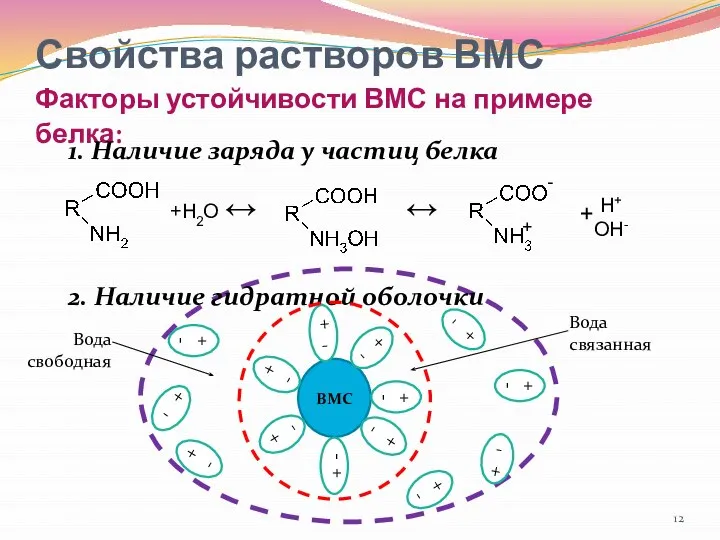
- 12. Свойства растворов ВМС Факторы устойчивости ВМС на примере белка: 1. Наличие заряда у частиц белка 2.
- 13. Пути коагуляции растворов ВМС К коагуляции растворов приводит: одновременная нейтрализация заряда частицы ВМС и полное разрушение
- 14. Коацервация… … расслаивание концентрированного раствора ВМС при действии дегидратирующих веществ на 2 фазы, одна из которых
- 15. Высаливание… …нарушение устойчивости растворов ВМС при действии неорганических солей. Высаливающее действие соли заключается в её собственной
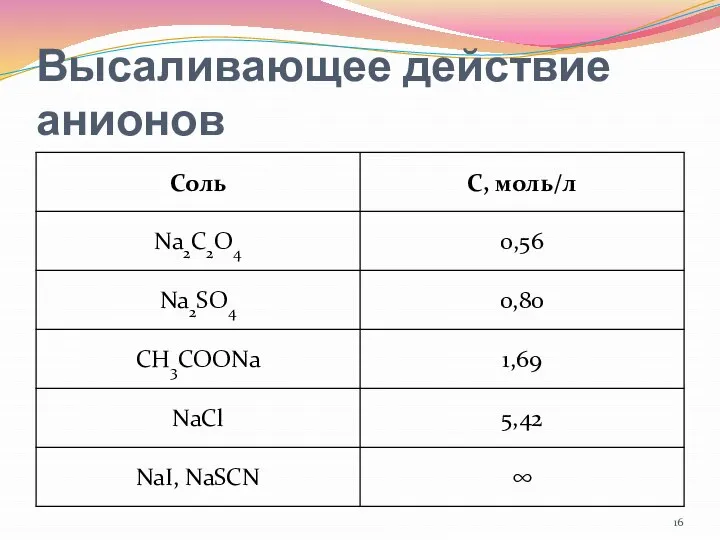
- 16. Высаливающее действие анионов
- 17. Ряды Гофмейстера C2O42- > SO42- > CH3COO- > Cl- > NO3- > I- > SCN- высаливающее
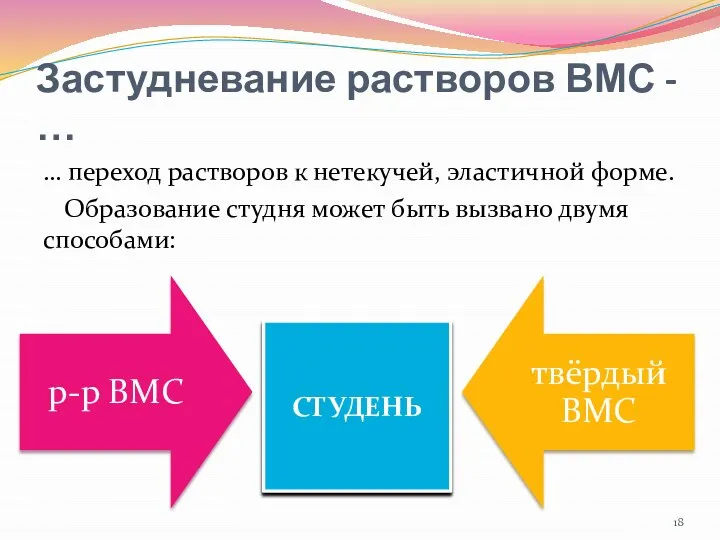
- 18. Застудневание растворов ВМС - … … переход растворов к нетекучей, эластичной форме. Образование студня может быть
- 19. Основу студня составляет пространственная сетка из цепей полимера, заполненная молекулами НМС. Студни со слабыми связями (водородными
- 20. Старение студней… Синерезис – уплотнение пространственной сетки студня за счёт выдавливания части НМС; гель при этом
- 21. Вязкость растворов ВМС (η) … … внутреннее трение между слоями ВМС, движущимися относительно друг друга. Величина
- 22. Уравнение Эйнштейна η=η0(1+αϕ) η - вязкость раствора η0 – вязкость растворителя α – коэффициент, зависящий от
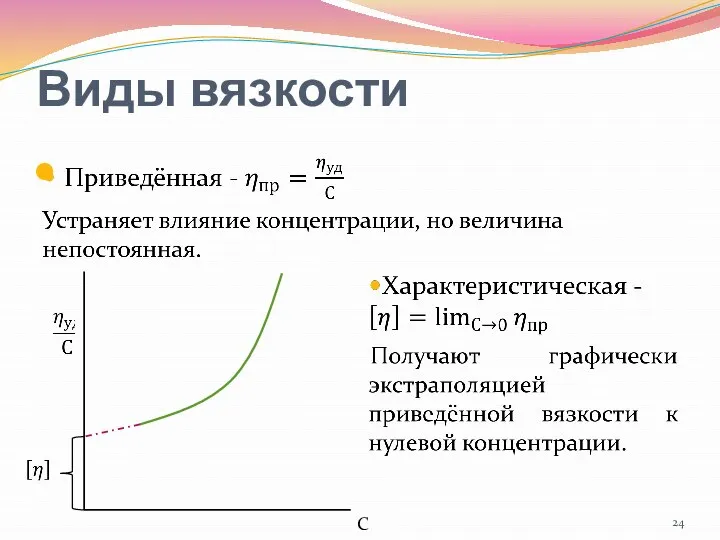
- 23. Виды вязкости
- 24. Виды вязкости С
- 25. Модифицированное уравнение Штаудингера
- 26. Вязкость крови… … очень важный показатель крови, определяющий максимальный срок службы сердца и сосудов. Чем выше
- 27. Вязкость крови В норме для плазмы крови и лимфы η=1,4∙10-3Па∙С (t=37°С). ↑ концентрации форменных элементов и
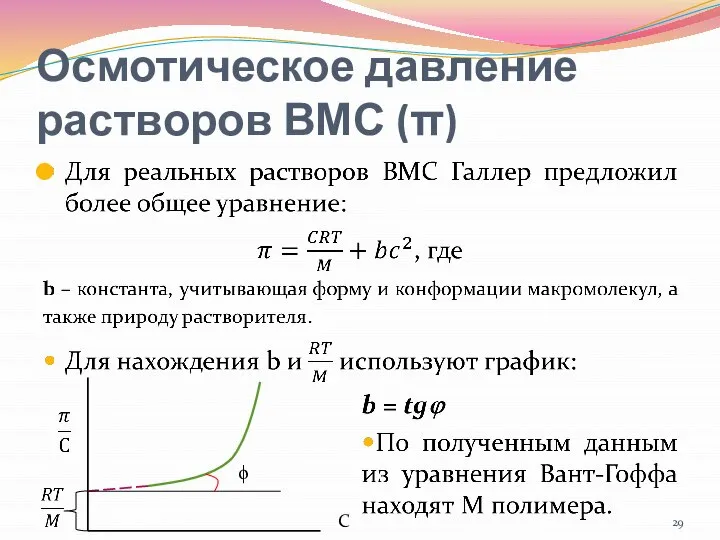
- 28. Осмотическое давление растворов ВМС (π)…
- 29. Осмотическое давление растворов ВМС (π) ϕ C
- 30. Онкотическое давление(πонк) … …часть осмотического давления крови, обусловленная наличием белков и их отдельных сегментов коллоидного размера.
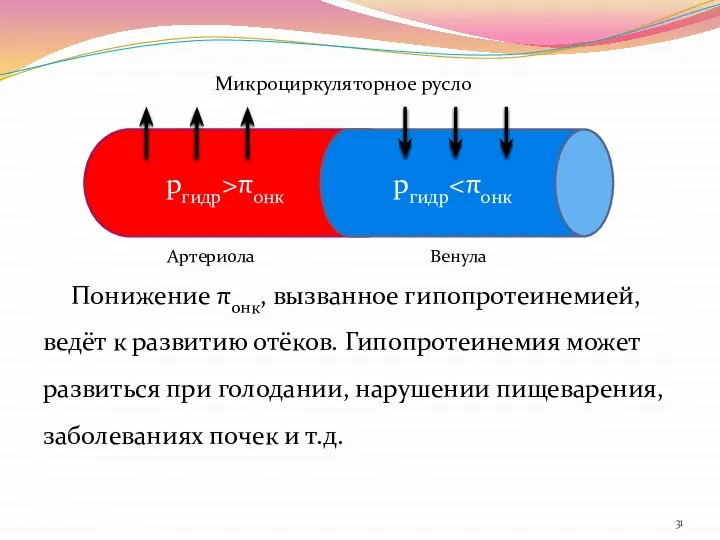
- 31. Понижение πонк, вызванное гипопротеинемией, ведёт к развитию отёков. Гипопротеинемия может развиться при голодании, нарушении пищеварения, заболеваниях
- 32. Мембранное равновесие Доннана Описывает распределение электролитов по обе стороны клеточной мембраны. сout – концентрация ионов в
- 33. Анализ уравнения Доннана Возможны 3 варианта распределения ионов: 1) cout > cin ⇒ 2) cin >
- 34. Причина мембранного равновесия избирательная проницаемость клеточных мембран, из-за которой соли белка всегда остаются в клетке и
- 36. Скачать презентацию


























 Теория химического строения А. М. Бутлерова. Часть II. Раздел 2
Теория химического строения А. М. Бутлерова. Часть II. Раздел 2 Химические средства защиты растений
Химические средства защиты растений Химический эксперимент в современной школе
Химический эксперимент в современной школе Презентация к уроку окружающего мира по теме: ,,Про воздух и про воду” Цель урока: знакомство учеников с богатствами природы - воздухом и водой, их свойствами. Задачи: Продолжить расширение и углубление представлений
Презентация к уроку окружающего мира по теме: ,,Про воздух и про воду” Цель урока: знакомство учеников с богатствами природы - воздухом и водой, их свойствами. Задачи: Продолжить расширение и углубление представлений  Презентация тест по химии
Презентация тест по химии Композиционные материалы, состав и классификация композиционных материалов
Композиционные материалы, состав и классификация композиционных материалов Презентация на тему «Биография Д.И. Менделеева» Работа Ученицы 9 – «А» класса СОШ № 1 Давыдовой Полины Под руководством Конд
Презентация на тему «Биография Д.И. Менделеева» Работа Ученицы 9 – «А» класса СОШ № 1 Давыдовой Полины Под руководством Конд Периодическая таблица Д.И. Менделеева Элемент № 24 ХРОМ
Периодическая таблица Д.И. Менделеева Элемент № 24 ХРОМ Гетероциклические соединения. Шестичленные гетероциклы с одним гетероатомом
Гетероциклические соединения. Шестичленные гетероциклы с одним гетероатомом Пластмассы (пластики)
Пластмассы (пластики) Оксиды. Оксиды металлов и оксиды неметаллов
Оксиды. Оксиды металлов и оксиды неметаллов Предпосылки открытия Периодического закона Д. И. Менделеевым
Предпосылки открытия Периодического закона Д. И. Менделеевым Тайна снежинки. Что такое снег. Как же образуются снежинки
Тайна снежинки. Что такое снег. Как же образуются снежинки Производные моносахаридов. Дисахариды
Производные моносахаридов. Дисахариды Многоатомные спирты. Вопросы для повторения
Многоатомные спирты. Вопросы для повторения Презентация по Химии "Мыло. Синтетические моющие средства" - скачать смотреть
Презентация по Химии "Мыло. Синтетические моющие средства" - скачать смотреть  Кислоты. Соли (8 класс)
Кислоты. Соли (8 класс) Ферменты
Ферменты Фiзико-хімічні основи розвитку пожеж. Тепломасообмін, температурний режим пожежі в огородженні. (Розділ 4.13.5)
Фiзико-хімічні основи розвитку пожеж. Тепломасообмін, температурний режим пожежі в огородженні. (Розділ 4.13.5) Оксид серы (VI). Серная кислота
Оксид серы (VI). Серная кислота Структура и функции клеточных мембран
Структура и функции клеточных мембран Композитные материалы
Композитные материалы Методи визначення хімічного складу ґрунту
Методи визначення хімічного складу ґрунту  Почему протекают химические реакции Начала термодинамики Автор: Фельдман Людмила Валентиновна, учитель химии МБОУ СОШ им. А.М.Гор
Почему протекают химические реакции Начала термодинамики Автор: Фельдман Людмила Валентиновна, учитель химии МБОУ СОШ им. А.М.Гор Полиамиды. Классификация по методу получения
Полиамиды. Классификация по методу получения Коллоидно-химический синтез квантовых точек на основе сульфидов свинца и кадмия
Коллоидно-химический синтез квантовых точек на основе сульфидов свинца и кадмия Метаболизм нуклеиновых кислот
Метаболизм нуклеиновых кислот Chimia coordinativă
Chimia coordinativă