Содержание
- 2. 1. Виды эксперимента и методика его использования. 2. Функции химического эксперимента. 3. Проблемный эксперимент. ПЛАН ЛЕКЦИИ
- 3. Химический эксперимент - важнейший метод и средство обучения химии.
- 4. 1. Виды эксперимента и методика его использования.
- 5. Демонстрационный химический эксперимент — главное средство наглядности на уроке.
- 6. Когда применяется демонстрационный эксперимент на уроке? В начале школьного курса — для привития экспериментальных умений и
- 7. ТРЕБОВАНИЯ К ДЕМОНСТРАЦИОННОМУ ЭКСПЕРИМЕНТУ 1. Наглядность — большой объем реактивов и посуды, виден с последних рядов,
- 8. МЕТОДИКА ПРОВЕДЕНИЯ ДЕМОНСТРАЦИОННЫХ ОПЫТОВ Постановка цели опыта: для чего проводится данный опыт, в чем должны убедиться
- 9. последовательность демонстраций: • горение угля • горение серы • горение фосфора • горение железа ТЕМА «КИСЛОРОД»
- 10. ЛАБОРАТОРНЫЕ ОПЫТЫ УЧЕНИЧЕСКИЙ ЭКСПЕРИМЕНТ ПРАКТИЧЕСКИЕ РАБОТЫ
- 11. ЭТАПЫ ВЫПОЛНЕНИЯ - осознание цели опыта - изучение веществ - монтаж прибора - выполнение опыта -
- 12. ПО ФОРМЕ ОРГАНИЗАЦИИ ЛАБОРАТОРНЫЕ ОПЫТЫ - Индивидуальными - Групповыми - Коллективными
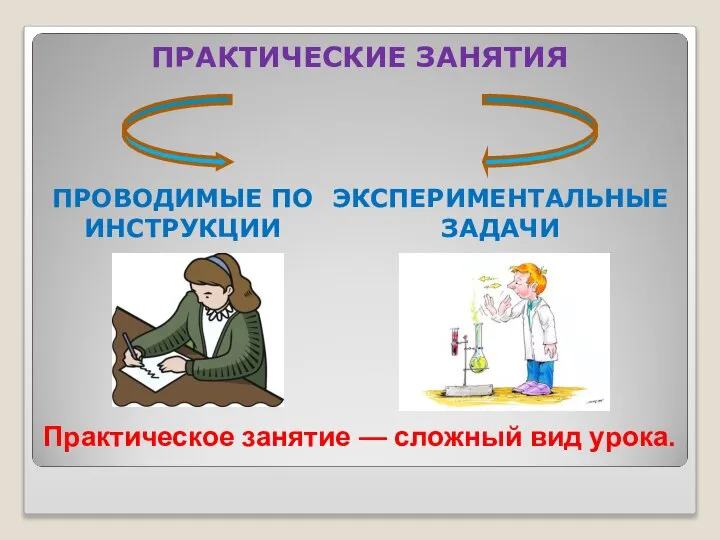
- 13. ПРОВОДИМЫЕ ПО ИНСТРУКЦИИ ПРАКТИЧЕСКИЕ ЗАНЯТИЯ ЭКСПЕРИМЕНТАЛЬНЫЕ ЗАДАЧИ Практическое занятие — сложный вид урока.
- 14. ЛИСТ УЧЕТА
- 15. ДОМАШНИЙ ХИМИЧЕСКИЙ ЭКСПЕРИМЕНТ – один из видов самостоятельной работы учащихся Используемые реактивы должны быть безопасными и
- 16. ОПЫТЫ С РАЗДЕЛЕНИЕМ СМЕСИ ВЕЩЕСТВ
- 17. 2. Функции химического эксперимента. - Эвристическая - Корректирующая - Обобщающая - Исследовательская
- 18. РЕАКЦИЯ ВЗАИМОДЕЙСТВИЯ ГАЗООБРАЗНОГО ВОДОРОДА С ОКСИДОМ МЕДИ (II) ЭВРИСТИЧЕСКАЯ ФУНКЦИЯ
- 19. CПОСОБ ПОЛУЧЕНИЯ КИСЛОРОДА ИЗ ПЕРОКСИДА ВОДОРОДА
- 20. СКОРОСТЬ ХИМИЧЕСКОЙ РЕАКЦИИ
- 21. КОРРЕКТИРУЮЩАЯ ФУНКЦИЯ
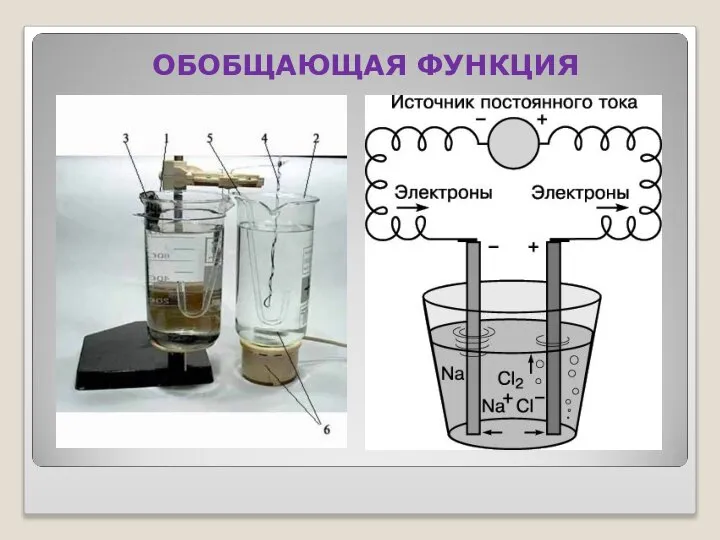
- 22. ОБОБЩАЮЩАЯ ФУНКЦИЯ
- 23. 3. Проблемный эксперимент.
- 24. ДЛЯ ХИМИИ ХАРАКТЕРЕН ЭКСПЕРИМЕНТ, КОТОРЫЙ НОСИТ ИССЛЕДОВАТЕЛЬСКИЙ И ПРОБЛЕМНЫЙ ХАРАКТЕР
- 25. 1) В чем причина наблюдаемого явления? 2) Почему добавление азотной кислоты влияет на выделение водорода из
- 26. водород, выделяющийся из соляной кислоты, затрачивается на восстановление азотной кислоты. РАБОЧАЯ ГИПОТЕЗА HNО3 + 8Н =
- 27. - актуализация знаний; - постановка целей исследования; - проведение теоретического анализа; - построение гипотезы; - составление
- 28. Слабая кислота вытесняет сильную из ее соли ПРИМЕРЫ ПАРАДОКСАЛЬНЫХ ОПЫТОВ Реактивы. Борная кислота, хлорид натрия, универсальная
- 29. ИЗМЕНЕНИЕ ЭНТАЛЬПИИ ХИМИЧЕСКОЙ РЕАКЦИИ ∆Н°(р-ции) ТЕРМОДИНАМИЧЕСКИЕ РАСЧЕТЫ 2NaCl + 4Н3ВО3 = Na2B4О7 + 5Н2O + 2HCl↑
- 30. 2NaCl + 4Н3ВО3 = Na2B4О7 + 5Н2O+ 2HCl↑ ∆S°298 72,36 89,49 189,5 188,74 186,7 (ж/(моль •
- 31. Т= ∆Н/∆S ТЕМПЕРАТУРА, ПРИ КОТОРОЙ ВОЗМОЖНО ПРОТЕКАНИЕ РЕАКЦИИ Т= ∆Н/∆S = 486,6/1 = 486,6 К, или
- 32. Реактивы. Свежеосажденная медь, 10%-й раствор хлорида железа (III). Растворение меди в растворе хлорида железа(III) Объяснение опыта.
- 33. Е = E(ок-ля ) — E(в-ля) ЭДС (Е) окислительно-восстановительного элемента равна: Если Е>0, то данная реакция
- 34. Реактивы. 15-25 %-й раствор аммиака, свежеосажденная медь. Растворение меди в растворе аммиака Объяснение опыта. 2Cu +
- 35. РАСЧЕТ ЭДС: Cu + 4NH3 - 2ē = 2[Cu(NH3)4]2+ Е° = - 0,07 В O2 +
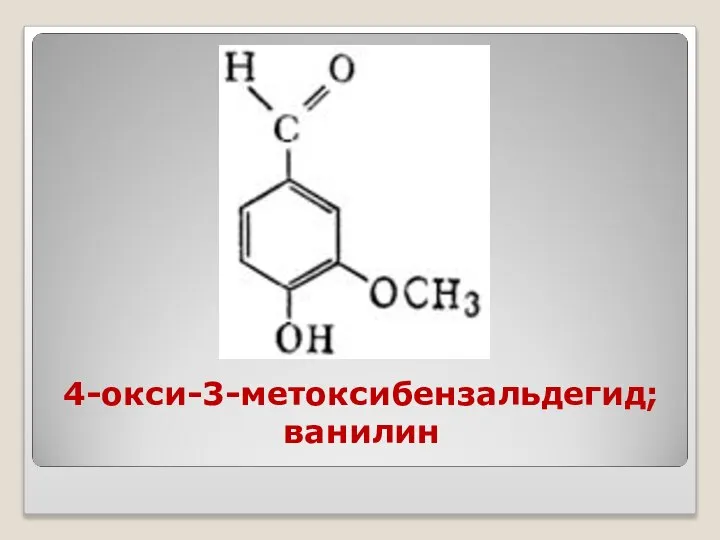
- 36. Ваниль, - душистая добавка к кондитерским изделиям. Ванилью называют высушенные плоды, стручки тропического растения из семейства
- 37. 4-окси-3-метоксибензальдегид; ванилин
- 39. 1. Приготовьте 3%-ый водный раствор ванилина (при 14˚С в 100 г воды растворяется 1 г вещества,
- 40. 2. Несколько миллилитров 3%-ого водного раствора ванилина поместите в пробирку и прилейте к нему 1 мл
- 42. Скачать презентацию































![РАСЧЕТ ЭДС: Cu + 4NH3 - 2ē = 2[Cu(NH3)4]2+ Е° =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1395317/slide-34.jpg)




 Осадочные горные породы
Осадочные горные породы Фізичні та хімічні властивості солей
Фізичні та хімічні властивості солей  Комплексные соединения
Комплексные соединения Total Syntheses of Trichorabdal A and Maoecrystal Z
Total Syntheses of Trichorabdal A and Maoecrystal Z Презентация по Химии "Кто хочет стать отличником" - скачать смотреть
Презентация по Химии "Кто хочет стать отличником" - скачать смотреть  Каталитический синтез нуклеозидов и других пребиотических производных формамида при протонном облучении метеоритов
Каталитический синтез нуклеозидов и других пребиотических производных формамида при протонном облучении метеоритов Тема урока "Основания" - презентация_
Тема урока "Основания" - презентация_ Материаловедение. Текстильные волокна, пряжа и ткань
Материаловедение. Текстильные волокна, пряжа и ткань Урок по химии в 10 классе по теме Каучуки
Урок по химии в 10 классе по теме Каучуки Презентация по Химии "Основы" - скачать смотреть бесплатно
Презентация по Химии "Основы" - скачать смотреть бесплатно Органічні сполуки: ліпіди
Органічні сполуки: ліпіди Алкадиены. Состав и строение
Алкадиены. Состав и строение Химики на службе у дорог
Химики на службе у дорог Серная кислота и её свойства
Серная кислота и её свойства Презентация по Химии "РЕАКЦИИ АЛЬДЕГИДНОЙ ГРУППЫ" - скачать смотреть бесплатно
Презентация по Химии "РЕАКЦИИ АЛЬДЕГИДНОЙ ГРУППЫ" - скачать смотреть бесплатно Электродные потенциалы. Гальванические элементы. ЭДС
Электродные потенциалы. Гальванические элементы. ЭДС Роль ионов в неживой природе и в жизни людей
Роль ионов в неживой природе и в жизни людей ФКХ-Л2 2016
ФКХ-Л2 2016 Вода: фізичні та хімічні властивості. Поширеність в природі
Вода: фізичні та хімічні властивості. Поширеність в природі Соли «Na2SO4»
Соли «Na2SO4» Химическая реакция
Химическая реакция Атомы, молекулы и ионы
Атомы, молекулы и ионы Вещества по их способности проводить электрический ток в растворах
Вещества по их способности проводить электрический ток в растворах Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Исследование воздействия плазмы метана на свойства оксида графена
Исследование воздействия плазмы метана на свойства оксида графена Значення хімії у повсякденному житті Значення хімії у побуті
Значення хімії у повсякденному житті Значення хімії у побуті  Липиды. Классификация
Липиды. Классификация ХИМИЧЕСКОЕ РАВНОВЕСИЕ. ФАКТОРЫ, ВЛИЯЮЩИЕ НА СМЕЩЕНИЕ РАВНОВЕСИЯ.
ХИМИЧЕСКОЕ РАВНОВЕСИЕ. ФАКТОРЫ, ВЛИЯЮЩИЕ НА СМЕЩЕНИЕ РАВНОВЕСИЯ.