Содержание
- 2. Лекция 5 Теория сплавов Величина С, называемая числом степеней свободы (вариантностью) системы, определяет количество параметров (р,
- 3. Лекция 5 Теория сплавов СПЛАВЫ С ПОЛНОЙ РАСТВОРИМОСТЬЮ КОМПОНЕНТОВ Зависимости температуры от времени охлаждения расплавов (кривые
- 4. Лекция 5 Теория сплавов Кривая, замыкающая точки начала кристаллизации сплавов I, III (TА, T1, T3, T5
- 5. Лекция 5 Теория сплавов СПЛАВЫ С ОГРАНИЧЕННОЙ РАСТВОРИМОСТЬЮ КОМПОНЕНТОВ Существует три принципиально разных типа таких сплавов:
- 6. Лекция 5 Теория сплавов Кривые охлаждения расплавов (а) и диаграмма состояния (б) сплава, компоненты которого ограниченно
- 7. Лекция 5 Теория сплавов Существуют сплавы, компоненты которых практически не растворимы в твердом состоянии и образуют
- 8. Лекция 5 Теория сплавов Для некоторых типов сплавов с ограниченной растворимостью компонентов (например, Сu — Zn,
- 9. Лекция 5 Теория сплавов СПЛАВЫ ОБРАЗУЮЩИЕ ХИМИЧЕСКИЕ СОЕДИНЕНИЯ Известны сплавы, компоненты которых образуют устойчивые химические соединения
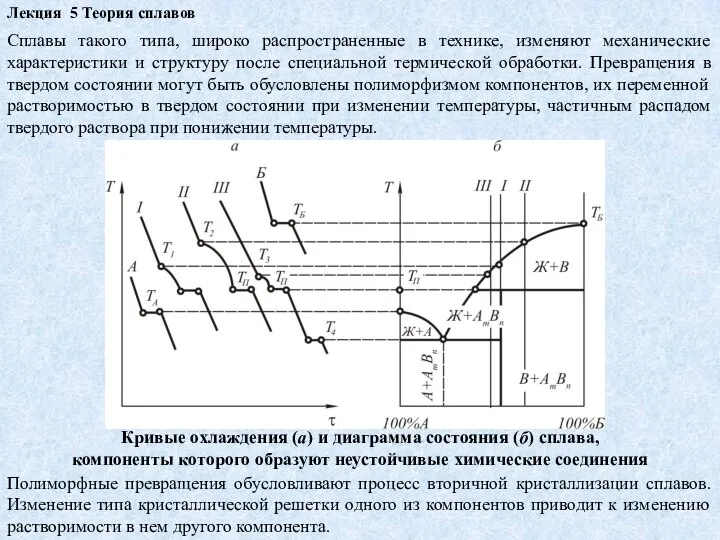
- 10. Лекция 5 Теория сплавов Сплавы такого типа, широко распространенные в технике, изменяют механические характеристики и структуру
- 11. Лекция 5 Теория сплавов СВЯЗЬ МЕЖДУ СТРУКТУРОЙ И СВОЙСТВАМИ СПЛАВОВ Диаграмма состояния сплава позволяет не только
- 12. Лекция 5 Теория сплавов При образовании механической смеси в сплавах металлов, взаимно не растворяющихся в твердом
- 13. Лекция 5 Теория сплавов Твердые растворы внедрения характерны для сплавов переходных металлов с неметаллами, имеющими атомы
- 15. Скачать презентацию
Лекция 5 Теория сплавов
Величина С, называемая числом степеней свободы (вариантностью) системы,
Лекция 5 Теория сплавов
Величина С, называемая числом степеней свободы (вариантностью) системы,
При кристаллизации металлического расплава в системе существуют две фазы — жидкая и твердая, что возможно только при постоянной температуре. Поэтому процесс кристаллизации является изотермическим (С=0). После полного исчезновения одной фазы число степеней свободы системы С = 1.
Параметр п = 2 характеризует внешние факторы (р, Т), оказывающие влияние на систему. В условиях атмосферы давление является постоянным фактором и не оказывает заметного влияния на состояние системы, поэтому обычно принимают n = 1. Из этого следует важный практический вывод: при атмосферном давлении число фаз (Ф), находящихся в равновесии, не может превышать больше, чем на единицу, количество компонентов (К) сплава, т.е.:
С = К – Ф + 1, Ф ≤ К+1
Лекция 5 Теория сплавов
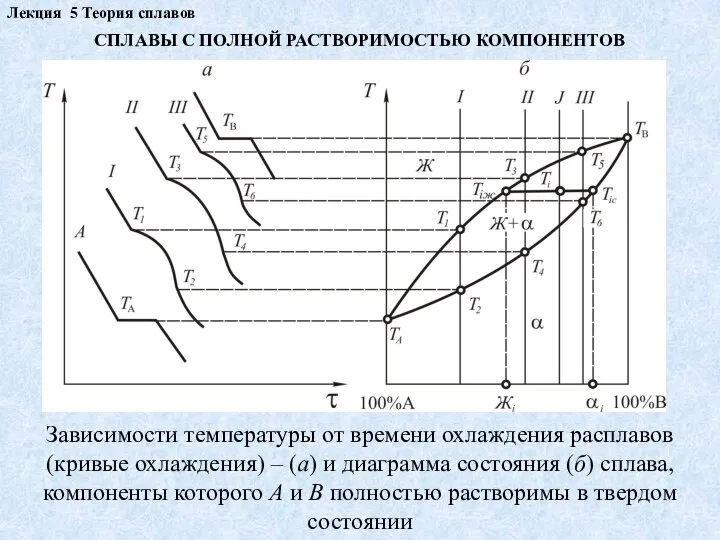
СПЛАВЫ С ПОЛНОЙ РАСТВОРИМОСТЬЮ КОМПОНЕНТОВ
Зависимости температуры от времени
Лекция 5 Теория сплавов
СПЛАВЫ С ПОЛНОЙ РАСТВОРИМОСТЬЮ КОМПОНЕНТОВ
Зависимости температуры от времени
Лекция 5 Теория сплавов
Кривая, замыкающая точки начала кристаллизации сплавов I, III
Лекция 5 Теория сплавов
Кривая, замыкающая точки начала кристаллизации сплавов I, III
Диаграмма состояния сплава позволяет количественно оценить состав любой фазы при любой температуре. Для этого используют правило концентрации: состав жидкой фазы при температуре Тi (см. рис.) определяется проекцией точки Тiж на ось концентраций (Жi), состав твердой фазы при температуре Тi — проекцией точки Тiс на ось концентрации (αi).
Для реализации правила концентраций необходимо провести из точки Тi линию, параллельную оси концентраций. Отрезок, соединяющий точки её пересечения с линиями ликвидус (Тiж) и солидус (Тiс), называют конодой.
Соотношение фаз при кристаллизации металлической системы устанавливают с помощью правила отрезков: массовые (объемные) соотношения твердой и жидкой фаз в сплаве пропорциональны отношению отрезков коноды, примыкающих к линиям ликвидус и солидус.
Лекция 5 Теория сплавов
СПЛАВЫ С ОГРАНИЧЕННОЙ РАСТВОРИМОСТЬЮ КОМПОНЕНТОВ
Существует три принципиально разных
Лекция 5 Теория сплавов
СПЛАВЫ С ОГРАНИЧЕННОЙ РАСТВОРИМОСТЬЮ КОМПОНЕНТОВ
Существует три принципиально разных
сплавы с ограниченной растворимостью компонентов и эвтектическим превращением;
сплавы компонентов, практически не растворимых в твердом состоянии, с эвтектическим превращением;
сплавы с ограниченной растворимостью компонентов и перитектическим превращением.
Эвтектикой («легкоплавящейся», греч.) называют высокодисперсную механическую смесь нескольких твердых фаз, одновременно кристаллизующихся из расплава при постоянной температуре. Эвтектическим превращением называют процесс одновременной кристаллизации из расплава нескольких твердых фаз при постоянной температуре.
При охлаждении эвтектического сплава (Э) до температуры Тэ на кривой охлаждения появляется горизонтальный участок, связанный с выделением теплоты кристаллизации. Закристаллизовавшаяся эвтектика состоит из механической смеси кристаллов α+β. Согласно теории кристаллизации, процесс образования эвтектики начинается с зарождения кристаллов одной из фаз.
Лекция 5 Теория сплавов
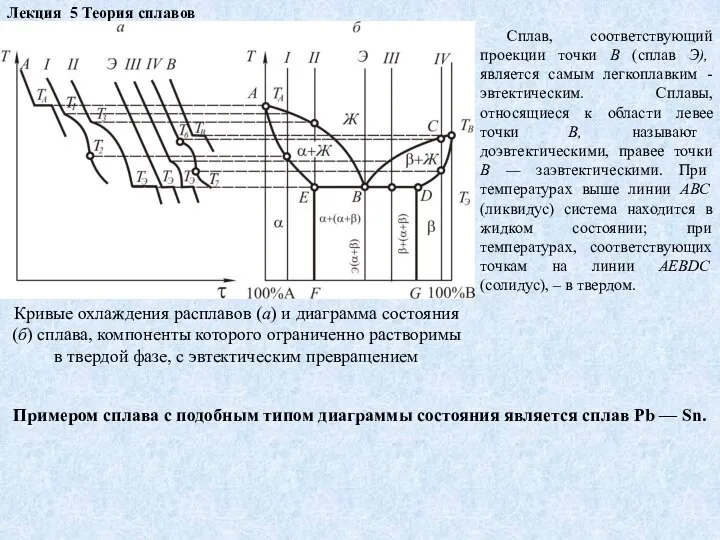
Кривые охлаждения расплавов (а) и диаграмма состояния (б)
Лекция 5 Теория сплавов
Кривые охлаждения расплавов (а) и диаграмма состояния (б)
Сплав, соответствующий проекции точки В (сплав Э), является самым легкоплавким -эвтектическим. Сплавы, относящиеся к области левее точки В, называют доэвтектическими, правее точки В — заэвтектическими. При температурах выше линии АВС (ликвидус) система находится в жидком состоянии; при температурах, соответствующих точкам на линии AEBDC (солидус), – в твердом.
Примером сплава с подобным типом диаграммы состояния является сплав Рb — Sn.
Лекция 5 Теория сплавов
Существуют сплавы, компоненты которых практически не растворимы в
Лекция 5 Теория сплавов
Существуют сплавы, компоненты которых практически не растворимы в
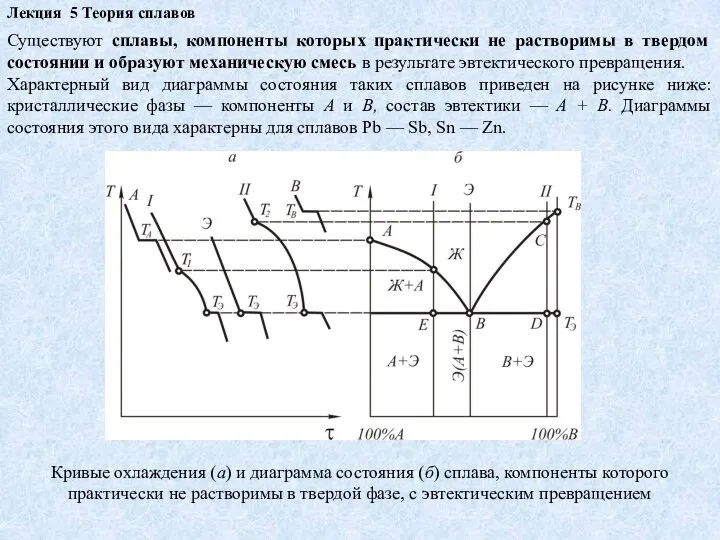
Характерный вид диаграммы состояния таких сплавов приведен на рисунке ниже: кристаллические фазы — компоненты A и В, состав эвтектики — A + В. Диаграммы состояния этого вида характерны для сплавов Рb — Sb, Sn — Zn.
Кривые охлаждения (а) и диаграмма состояния (б) сплава, компоненты которого практически не растворимы в твердой фазе, с эвтектическим превращением
Лекция 5 Теория сплавов
Для некоторых типов сплавов с ограниченной растворимостью компонентов
Лекция 5 Теория сплавов
Для некоторых типов сплавов с ограниченной растворимостью компонентов
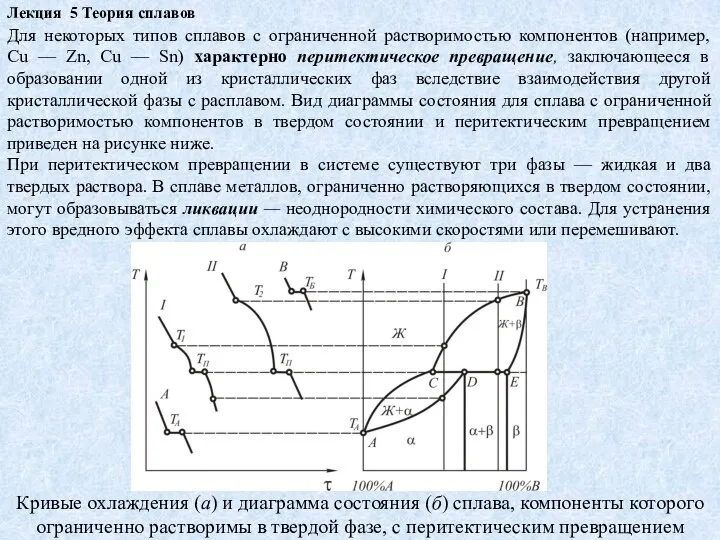
При перитектическом превращении в системе существуют три фазы — жидкая и два твердых раствора. В сплаве металлов, ограниченно растворяющихся в твердом состоянии, могут образовываться ликвации — неоднородности химического состава. Для устранения этого вредного эффекта сплавы охлаждают с высокими скоростями или перемешивают.
Кривые охлаждения (а) и диаграмма состояния (б) сплава, компоненты которого ограниченно растворимы в твердой фазе, с перитектическим превращением
Лекция 5 Теория сплавов
СПЛАВЫ ОБРАЗУЮЩИЕ ХИМИЧЕСКИЕ СОЕДИНЕНИЯ
Известны сплавы, компоненты которых образуют
Лекция 5 Теория сплавов
СПЛАВЫ ОБРАЗУЮЩИЕ ХИМИЧЕСКИЕ СОЕДИНЕНИЯ
Известны сплавы, компоненты которых образуют
Фаза устойчивого химического соединения обозначена АтВп. Каждая диаграмма включает по два эвтектических превращения. Состав эвтектик: а+АтВп (эвтектика I) и β+АтВп (эвтектика II) для диаграммы состояния химического соединения с переменным составом.
Неустойчивая промежуточная фаза химического соединения АтВп неустойчива и при нагревании сплава до температуры, соответствующей точке Тп, распадется.
Диаграммы состояния сплавов, компоненты которых образуют устойчивые химические соединения:
а — постоянного состава;
б — переменного состава
Лекция 5 Теория сплавов
Сплавы такого типа, широко распространенные в технике, изменяют
Лекция 5 Теория сплавов
Сплавы такого типа, широко распространенные в технике, изменяют
Кривые охлаждения (а) и диаграмма состояния (б) сплава,
компоненты которого образуют неустойчивые химические соединения
Полиморфные превращения обусловливают процесс вторичной кристаллизации сплавов. Изменение типа кристаллической решетки одного из компонентов приводит к изменению растворимости в нем другого компонента.
Лекция 5 Теория сплавов
СВЯЗЬ МЕЖДУ СТРУКТУРОЙ И СВОЙСТВАМИ СПЛАВОВ
Диаграмма состояния сплава
Лекция 5 Теория сплавов
СВЯЗЬ МЕЖДУ СТРУКТУРОЙ И СВОЙСТВАМИ СПЛАВОВ
Диаграмма состояния сплава
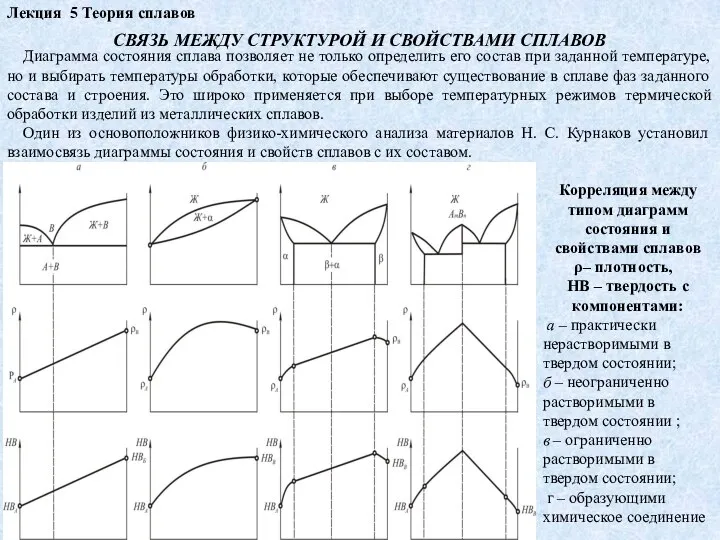
Один из основоположников физико-химического анализа материалов Н. С. Курнаков установил взаимосвязь диаграммы состояния и свойств сплавов с их составом.
Корреляция между типом диаграмм состояния и свойствами сплавов
– плотность,
НВ – твердость с компонентами:
а – практически нерастворимыми в твердом состоянии;
б – неограниченно растворимыми в твердом состоянии ;
в – ограниченно растворимыми в твердом состоянии;
г – образующими химическое соединение
Лекция 5 Теория сплавов
При образовании механической смеси в сплавах металлов, взаимно
Лекция 5 Теория сплавов
При образовании механической смеси в сплавах металлов, взаимно
ТАКИМ ОБРАЗОМ, подведем итоги вышеизложенному:
Лекция 5 Теория сплавов
Твердые растворы внедрения характерны для сплавов переходных металлов
Лекция 5 Теория сплавов
Твердые растворы внедрения характерны для сплавов переходных металлов
Металлы при сплавлении обладают свойством растворяться друг в друге, образуя смесь компонентов, находящихся в твердом состоянии. Установлены эмпирические правила такого растворения:
увеличение разницы атомных радиусов компонентов сплава снижает их способность к образованию раствора (размерный фактор),
2) увеличение разности в валентностях компонентов при соответствии их атомных радиусов снижает растворимость (относительная валентность).
Образование твердых растворов замещения возможно при любом соотношении атомных масс компонентов. Для образования твердых растворов с неограниченной растворимостью необходимо выполнение следующих условий:
компоненты сплава должны обладать изоморфными (полностью подобными) кристаллическими решетками;
2) различие атомных размеров компонентов не должно превышать 8—15%;
3) внешние электронные оболочки атомов компонентов должны иметь одинаковое строение (равная валентность). Примерами таких сплавов являются сплавы Сu—Аu, Сu—Ni, Ge — Si, Ag — Au, Mo — V.






 Органические и неорганические вещества. Нуклеиновые кислоты
Органические и неорганические вещества. Нуклеиновые кислоты ОМЕГА 3 и ОМЕГА 6 полиненасыщенные жирные кислоты (ПНЖК) Все более популярными в ветеринарии становятся ОМЕГА 3 и ОМЕГА 6 полиненасы
ОМЕГА 3 и ОМЕГА 6 полиненасыщенные жирные кислоты (ПНЖК) Все более популярными в ветеринарии становятся ОМЕГА 3 и ОМЕГА 6 полиненасы Тест: Азот
Тест: Азот Витамины и их производные-коферменты ферментов
Витамины и их производные-коферменты ферментов Получение гидроксида никеля (II)
Получение гидроксида никеля (II) Розчини електролітів
Розчини електролітів Вода – растворитель. Растворы. Значение воды
Вода – растворитель. Растворы. Значение воды Використання кислот
Використання кислот Гелий
Гелий Индол. Методы синтеза. Химические свойства. Биологически активные производные. (Лекция 4)
Индол. Методы синтеза. Химические свойства. Биологически активные производные. (Лекция 4) Карбон қышқылдары
Карбон қышқылдары Вступ в гетерогенний катализ. Загальні положення каталізу
Вступ в гетерогенний катализ. Загальні положення каталізу Синтез и свойства кукурбитурилов
Синтез и свойства кукурбитурилов Жиры. 9 класс
Жиры. 9 класс ОКСИДЫ АЗОТА.
ОКСИДЫ АЗОТА.  ВПР Окружающий мир 4 класс
ВПР Окружающий мир 4 класс  Урок по теме: «Жиры. Техническая переработка жиров» Пермякова Ирина Александровна Учитель химии ГБОУ СОШ № 982 г. Москва Индиф
Урок по теме: «Жиры. Техническая переработка жиров» Пермякова Ирина Александровна Учитель химии ГБОУ СОШ № 982 г. Москва Индиф Условия хранения и подготовка скоропортящихся грузов к перевозкам
Условия хранения и подготовка скоропортящихся грузов к перевозкам Инертные газы
Инертные газы Агрегатные состояния вещества
Агрегатные состояния вещества Нанопористые материалы
Нанопористые материалы Предельные углеводороды. Химические свойства. 10 класс
Предельные углеводороды. Химические свойства. 10 класс Природные и синтетические красители и ароматизаторы
Природные и синтетические красители и ароматизаторы Химические свойства фурана, пиррола, тиофена. Биологически активные производные ряда фурана, пиррола, тиофена. (Лекция 3)
Химические свойства фурана, пиррола, тиофена. Биологически активные производные ряда фурана, пиррола, тиофена. (Лекция 3) МОУ «Каратунская СОШ с углубленным изучением отдельных предметов» Выполнила : учитель химии второй квалификационной категор
МОУ «Каратунская СОШ с углубленным изучением отдельных предметов» Выполнила : учитель химии второй квалификационной категор Элективный курс "Решение задач по химии повышенного уровня сложности"
Элективный курс "Решение задач по химии повышенного уровня сложности" Сложные эфиры R-COOR'
Сложные эфиры R-COOR' Оценка опасности взрыва горючих газов
Оценка опасности взрыва горючих газов