Содержание
- 2. Химическая термодинамика Может предсказывать: возможность протекания химической реакции . Используется: для расчета энергии, необходимой для осуществления
- 3. “Термодинамическая система ” Система- это любая совокупность веществ, отделённая от окружающей среды реальной или воображаемой поверхностью
- 4. ТИПЫ СИСТЕМ Полностью изолированные Отсутствует обмен энергией и веществом с окружающей средой, (примером может служить вселенная).
- 5. СОСТОЯНИЯ СИСТЕМЫ стационарное Для открытых систем: все живые организмы, для которых характерно постоянство параметров pH, t0,
- 6. ТЕРМОДИНАМИЧЕСКИЙ ПРОЦЕСС Переход системы из одного состояния в другое называется процессом. В зависимости от условий процессы
- 7. Внутренняя энергия системы Энергия – это способность совершать работу (кДж/моль) Внутренняя энергия равна сумме потенциальной и
- 8. Первый закон термодинамики (Ю.Р.МАЙЕР 1842) энергия может превращаться из одного вида в другой, но не может
- 9. термохимия изучает энергетические эффекты химических и физико-химических процессов. Тепловой эффект реакции – это количество энергии, которое
- 10. Расчеты в термохимии. Закон Гесса (1836). “Тепловой эффект (энтальпия) реакции зависит только от природы и физического
- 11. Следствия из закона Гесса : Энтальпия образования вещества равна энтальпии разложения вещества, но противоположна по знаку:
- 12. Типовая задача. Рассчитать тепловой эффект реакции окисления 1 моль глюкозы: С6Н12О6 (т)+ 6О2(г) = 6Н2О(ж) +
- 13. Движущие силы реакции Энтальпийный фактор экзотермический процесс : ∆H эндотермический : ∆H > 0 Самопроизвольно любая
- 14. Второй закон термодинамики тенденция частиц объединяться , понижая U and H (∆H тенденция частиц распадаться ,
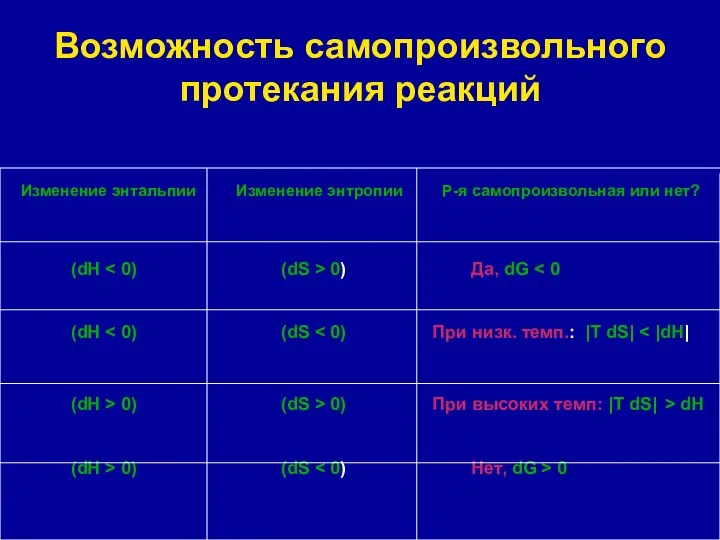
- 15. Влияние температуры на направление реакции ( по уравнению Гиббса: ∆G=∆H - T∆S ) Четыре возможных случая:
- 16. Возможность самопроизвольного протекания реакций Изменение энтальпии Изменение энтропии Р-я самопроизвольная или нет? (dH 0) Да, dG
- 17. Термодинамическая вероятность биологических процессов Метаболизм – это совокупность химических реакций, протекающих в живых клетках Ключевую роль
- 19. Скачать презентацию















 Общие электронные конфигурации элементов главных подгрупп
Общие электронные конфигурации элементов главных подгрупп Аминокислоты. Свойства
Аминокислоты. Свойства Классификация металлов в соответствии с ионным потенциалом и параметром мягкости
Классификация металлов в соответствии с ионным потенциалом и параметром мягкости Сульфаниламидные препараты. (Тема 5)
Сульфаниламидные препараты. (Тема 5) Химия. 8 класс. Подготовка к контрольной работе
Химия. 8 класс. Подготовка к контрольной работе Атомный уровень. Химия простых веществ. Молекулярный уровень. Химия соединений. Живое субклеточный уровень
Атомный уровень. Химия простых веществ. Молекулярный уровень. Химия соединений. Живое субклеточный уровень Присадки к маслам
Присадки к маслам Периодический закон и периодическая система Д.И.Менделеева. Лекция 4
Периодический закон и периодическая система Д.И.Менделеева. Лекция 4 Презентация по Химии "Фосфор" - скачать смотреть бесплатно_
Презентация по Химии "Фосфор" - скачать смотреть бесплатно_ Химия в быту
Химия в быту Химия муравьиной кислоты
Химия муравьиной кислоты Количество вещества. Моль. Молярная масса
Количество вещества. Моль. Молярная масса Генетическая связь основных классов неорганических соединений
Генетическая связь основных классов неорганических соединений Подача питательной воды в парогенератор при запроектной аварии
Подача питательной воды в парогенератор при запроектной аварии Именные реакции в органической химии
Именные реакции в органической химии Презентация по Химии "Оксиды получение, свойства, применение" - скачать смотреть бесплатно
Презентация по Химии "Оксиды получение, свойства, применение" - скачать смотреть бесплатно Презентация по Химии "Металлическая связь" - скачать смотреть
Презентация по Химии "Металлическая связь" - скачать смотреть  Углеводы. Дисахариды и полисахариды
Углеводы. Дисахариды и полисахариды Окислительно-восстановительные реакции . Алканолы
Окислительно-восстановительные реакции . Алканолы Тяжёлая вода
Тяжёлая вода Нитраты и нитриты. Азотные удобрения
Нитраты и нитриты. Азотные удобрения ПРЕЗЕНТАЦИЯ «Химия и повседневная жизнь человека»
ПРЕЗЕНТАЦИЯ «Химия и повседневная жизнь человека»  Применение неметаллов
Применение неметаллов Бензойная кислота
Бензойная кислота Окислительно- восстановительные процессы
Окислительно- восстановительные процессы Выполнила: Смирнова Маргарита Ученица: 9-а класса
Выполнила: Смирнова Маргарита Ученица: 9-а класса Тест 1.Тип кристаллической решетки у белого фосфора…. а) молекулярный б) атомный в) ионный а) молекулярный Р4 2. У фосфора…..
Тест 1.Тип кристаллической решетки у белого фосфора…. а) молекулярный б) атомный в) ионный а) молекулярный Р4 2. У фосфора…..  Лекция 1. Топливо. Горение топлива
Лекция 1. Топливо. Горение топлива