Содержание
- 2. ОБЯЗАТЕЛЬНО!!! Закон, который нельзя нарушать: «Конспекты готовим накануне лекции, дома!!! На лекциях идет обсуждение материала и
- 3. «Термодинамика химических процессов." Кафедра общей и медицинской химии
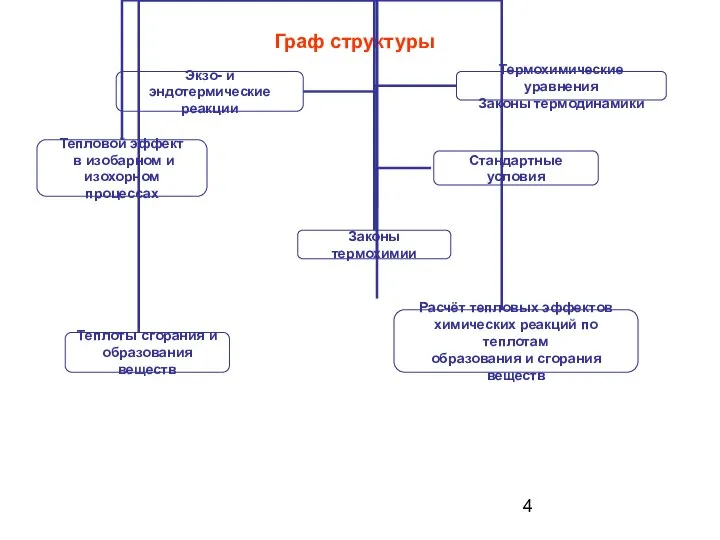
- 4. Граф структуры
- 5. Термодинамика изучает: соотношение между тепловой и другими формами энергии в химических реакциях; возможность самопроизвольного протекания реакций
- 6. Системы в термодинамике: Открытые – обмен веществом и энергией 2. Закрытые (замкнутые) – обмен только энергией
- 7. 3. Гомогенные – нет раздела границы фаз 4. Гетерогенные– граница раздела фаз присутствует
- 8. 5. Равновесные – не происходит видимых изменений 6. Стационарные – видимых изменений нет, но есть обмен
- 9. I закон термодинамики: Если к закрытой системе подводить тепло, энергия будет расходоваться на увеличение внутренней энергии
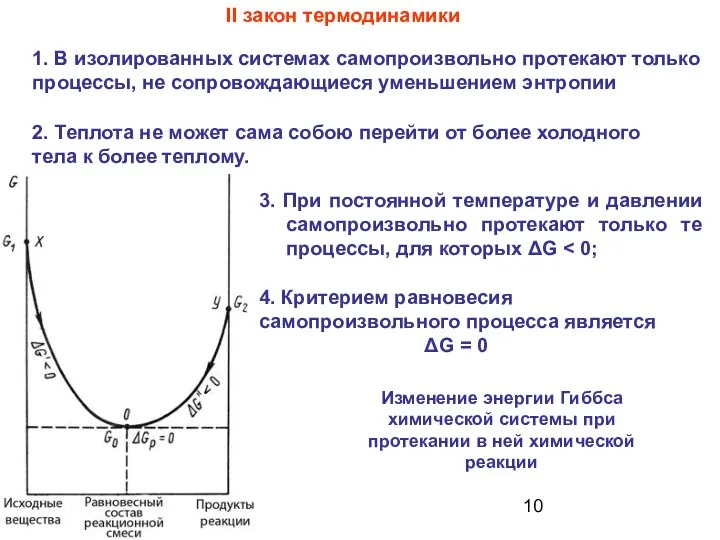
- 10. 3. При постоянной температуре и давлении самопроизвольно протекают только те процессы, для которых ΔG II закон
- 11. 2. Абсолютный нуль недостижим ( так называемая «смерть Вселенной») 1. Энтропия идеального кристалла при абсолютном нуле
- 12. Внутренняя энергия – это такая энергия тела, за счет которой может совершаться механическая работа, не вызывая
- 13. Теплота – количественная мера хаотического движения молекул в данной системе. Мерой интенсивности движения молекул является температура.
- 14. Работа – количественная мера направленного движения молекул в одностороннем направлении.
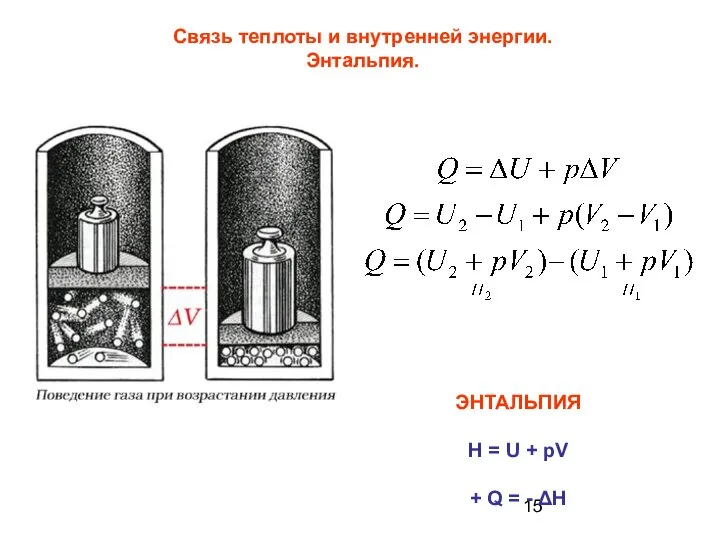
- 15. Связь теплоты и внутренней энергии. Энтальпия. ЭНТАЛЬПИЯ H = U + pV + Q = -
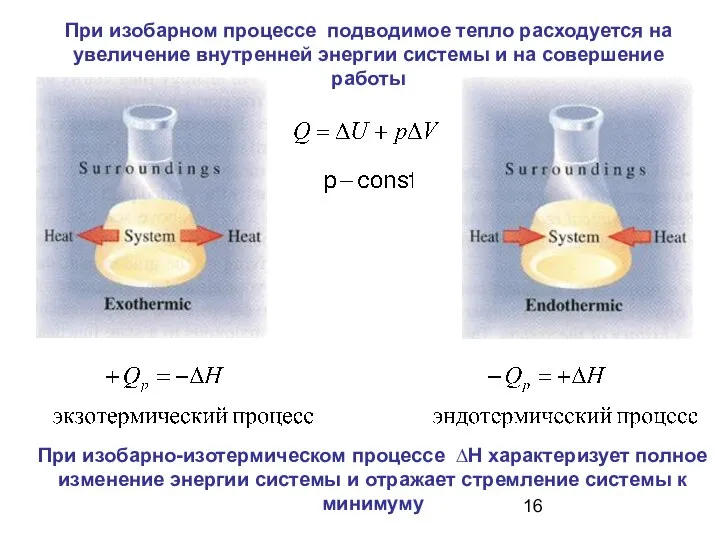
- 16. При изобарно-изотермическом процессе ∆Н характеризует полное изменение энергии системы и отражает стремление системы к минимуму При
- 17. При изохорном процессе все подводимое тепло расходуется на увеличение внутренней энергии системы.
- 18. I закон термодинамики: Если к закрытой системе подводить тепло, энергия будет расходоваться на увеличение внутренней энергии
- 19. Открыл (1840) основной закон термохимии. Установил катализирующее и адсорбционное свойства мелкораздробленной платины. Одним из первых изучил
- 20. Закон Гесса Тепловой эффект реакции зависит только от ………. Термодинамическая функция состояния — функция, зависящая от
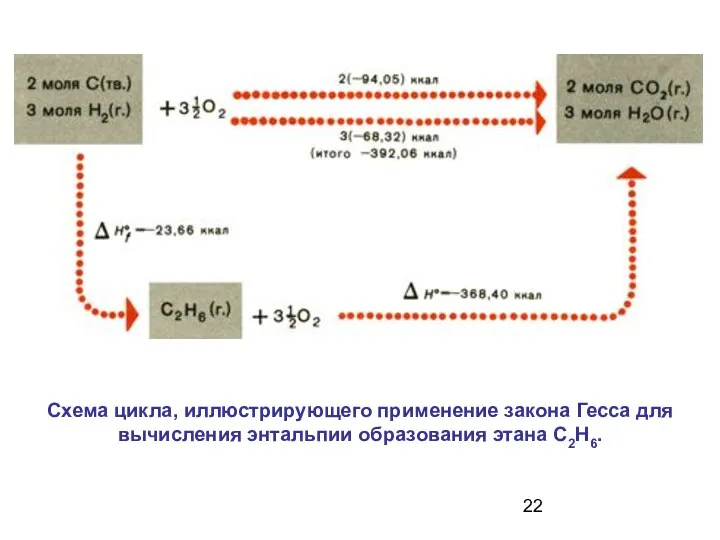
- 21. Следствия из закона Гесса: 1. Тепловой эффект реакции при стандартных условиях равен разности между суммой теплот
- 22. Схема цикла, иллюстрирующего применение закона Гесса для вычисления энтальпии образования этана С2Н6.
- 23. 2. Тепловой эффект реакции при стандартных условиях равен разности между суммой теплот сгорания исходных веществ и
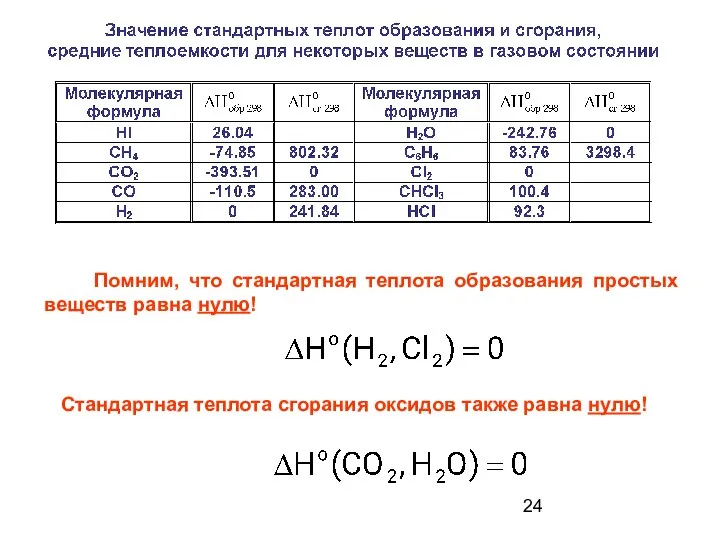
- 24. Помним, что стандартная теплота образования простых веществ равна нулю! Стандартная теплота сгорания оксидов также равна нулю!
- 25. Первый закон термодинамики позволяет рассчитать энергетический баланс химического процесса.
- 26. Пример 2 Рассчитайте тепловой эффект реакции C6H6 + 7.5O2=6CO2(г)+3H2O(ж), по стандартным теплотам сгорания Решение:
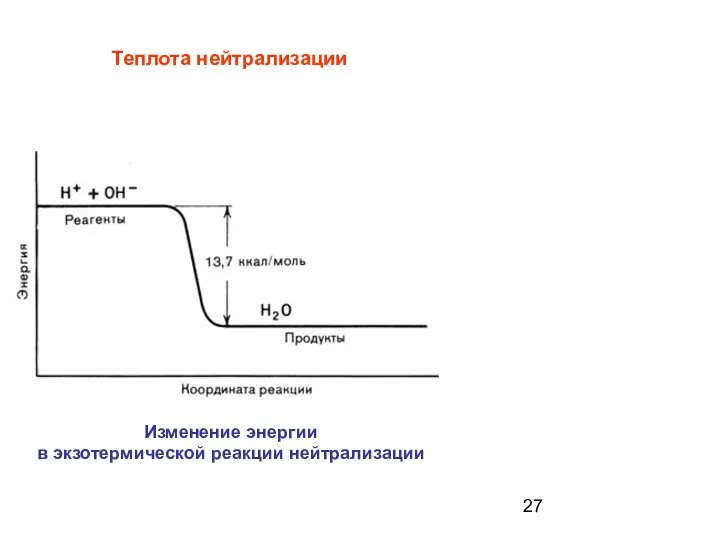
- 27. Теплота нейтрализации Изменение энергии в экзотермической реакции нейтрализации
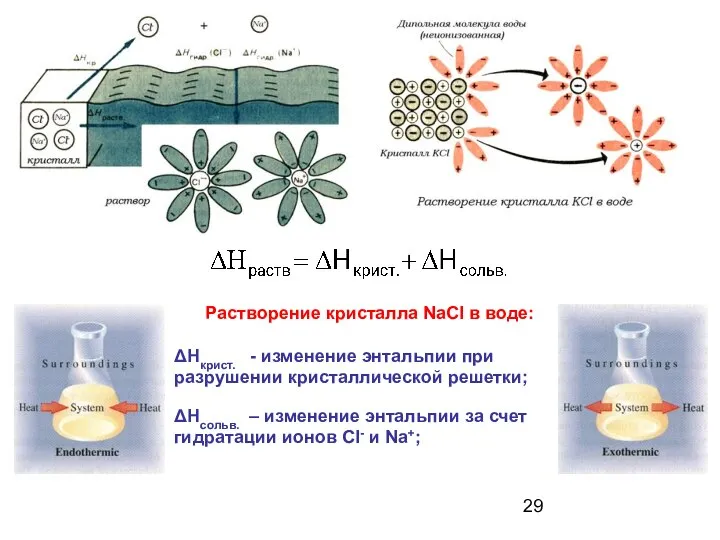
- 28. Механизм растворения кристаллов. Гидратация: молекулы воды окружают частицы растворенного вещества, образуя гидраты. Процесс экзотермический. ΔН гидр.
- 29. Растворение кристалла NaCl в воде: ΔНкрист. - изменение энтальпии при разрушении кристаллической решетки; ΔНсольв. – изменение
- 30. Для прогнозирования возможности и направления процессов необходимо ввести еще одну функцию, которая должна отвечать двум требованиям:
- 31. Немецкий физик. Главные работы Клаузиуса посвящены основам термодинамики и кинетической теории газов. 1850 году получил соотношение
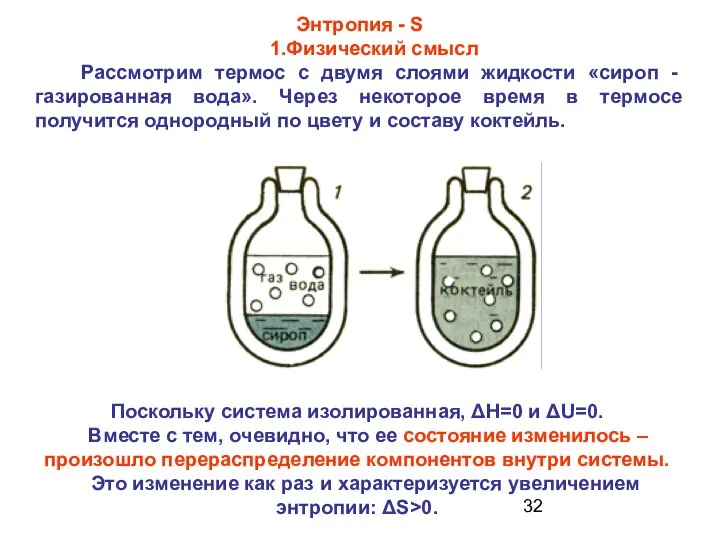
- 32. Энтропия - S 1.Физический смысл Рассмотрим термос с двумя слоями жидкости «сироп - газированная вода». Через
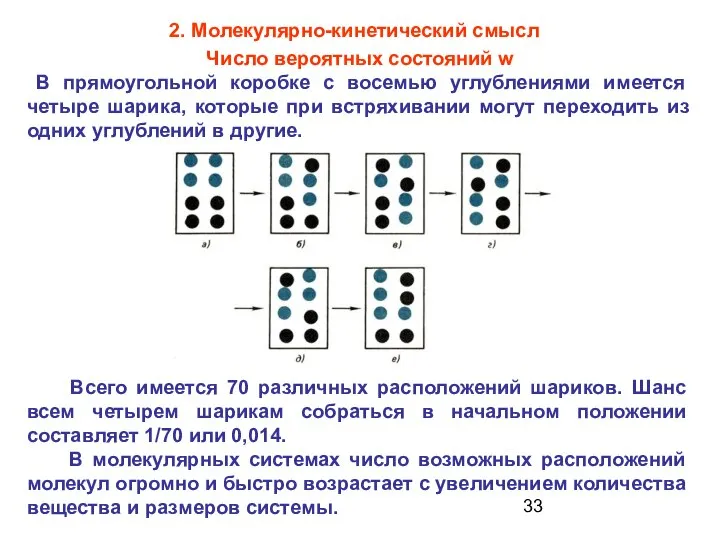
- 33. Число вероятных состояний w В прямоугольной коробке с восемью углублениями имеется четыре шарика, которые при встряхивании
- 34. Чем большим числом микрочастиц представлена рассматриваемая макросистема, тем больше вариантов распределения этих частиц, тем выше значение
- 35. Без постороннего вмешательства невозможен ни один процесс, результатом которого является повышение порядка, то есть уменьшение энтропии!
- 36. Окончил Венский университет в 1867 г. Занимал профессорские должности в университетах Вены, Граца, Мюнхена и Лейпцига.
- 37. Могила Больцмана в Вене с бюстом и формулой энтропии
- 38. Понятие об энтропии как термодинамической функции состояния для обратимых процессов было выведено Р.Клаузиусом: В обратимых изотермических
- 39. Примером может служить медленное таяние льда в термосе с водой при 273о К (0оС), для чего
- 40. Энтропия газообразного вещества больше, чем жидкого, последняя – больше, чем твердого вещества. Рост температуры и снижение
- 41. При абсолютном нуле (- 273.130С) S=0, что позволяет измерить или теоретически рассчитать абсолютные значения энтропии S0
- 42. Задача Определить энтропию образования этанола из элементов (пользуясь табличными данными). 2С + 3Н2 + 0.5О2 →
- 43. Критерии самопроизвольного протекания процесса Энтальпийный фактор (ΔН) - характеризует стремление системы к упорядочению, поскольку процесс сопровождается
- 44. T∆S – характеризует ту часть энергии, которую нельзя превратить в работу (связанная энергия), и отражает стремление
- 45. Функцией, учитывающей оба фактора и противоположность в тенденции их изменения является энергия Гиббса G (изобарно-изотермический потенциал):
- 46. Факторы, определяющие ход изобарно- изотермического процесса ( Р и Т – постоянны) (помним, что +Q =
- 47. Свободная энергия Гиббса (разность между энтальпийным и энтропийным факторами) ∆G=∆H–T∆S ∆G – характеризует часть энергии системы,
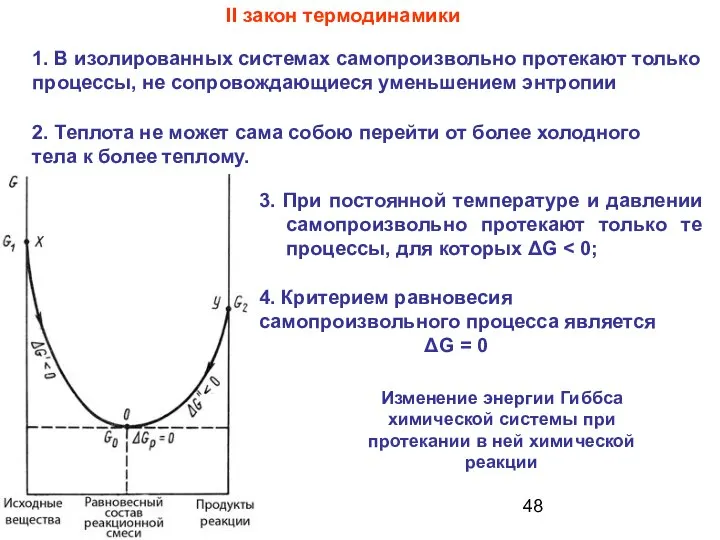
- 48. 3. При постоянной температуре и давлении самопроизвольно протекают только те процессы, для которых ΔG II закон
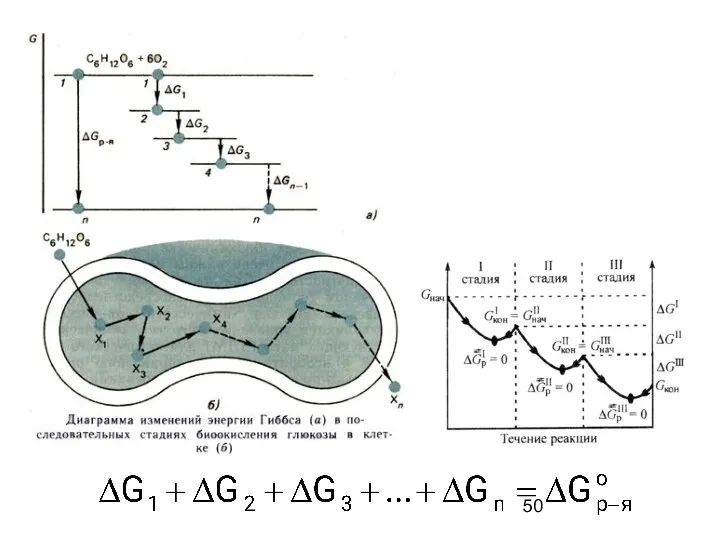
- 49. Так как энергия Гиббса есть функция состояния, к ней также применим закон Гесса: Важный пример применения
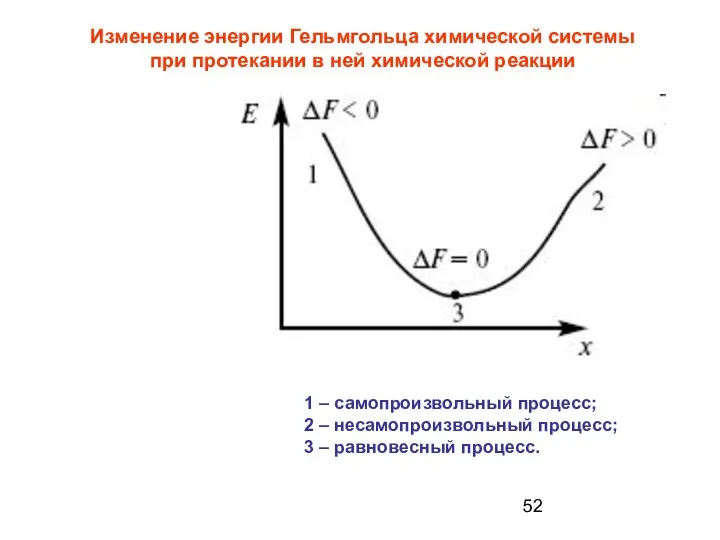
- 51. Для процессов, протекающих в изохорно –изотермических условиях, ( V и Т – постоянны), используется энергия Гельмгольца
- 52. 1 – самопроизвольный процесс; 2 – несамопроизвольный процесс; 3 – равновесный процесс. Изменение энергии Гельмгольца химической
- 53. Немецкий физик, математик, физиолог и психолог. Родился в Потсдаме в семье учителя гимназии. Несмотря на интерес
- 54. КПД при переходе тепла в работу всегда меньше 1 η = (Т1–Т2)/Т1 (часть тепла всегда расходуется
- 55. Поскольку при абсолютном нуле поступательное, вращательное и колебательное движение молекул прекращается, число вероятных состояний W=1, Вальтер
- 56. 3. Абсолютный нуль недостижим ( так называемая «смерть Вселенной») 2. Энтропия идеального кристалла при абсолютном нуле
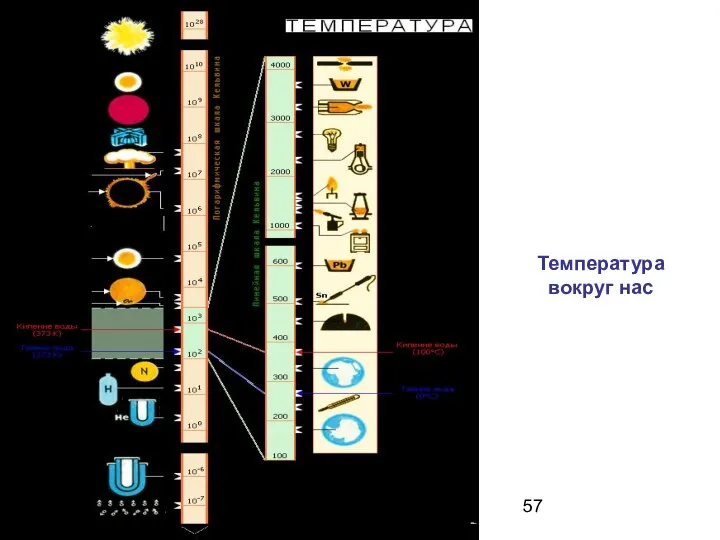
- 57. Температура вокруг нас
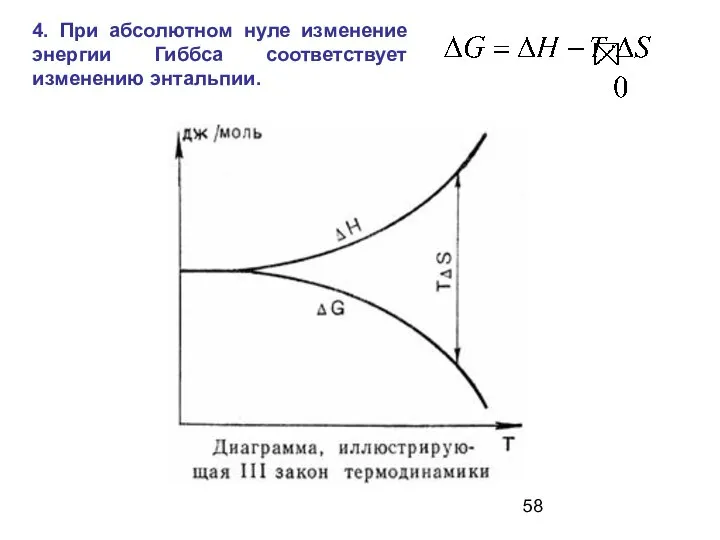
- 58. 4. При абсолютном нуле изменение энергии Гиббса соответствует изменению энтальпии.
- 59. Гилберт Льюис – 23.10.1875 – 23.03.1946 Предложил новую теорию кислот как акцепторов пары электронов и оснований
- 60. 1. Большинство биохимических реакций в организме – обратимы и протекают многостадийно. 2. Биологическое развитие организма возможно
- 61. 3. Живые организмы поддерживают присущую им упорядоченность за счет увеличения энтропии внешней среды (поступающие с низким
- 62. Принцип Пригожина В открытой системе в стационарном состоянии прирост энтропии в единицу времени ∆S / ∆t
- 63. 4. Реализация принципа энергетического сопряжения: Эндэргонические реакции (∆G>0 –процесс самопроизвольно не идет!!!) сопряжены с экзэргоническими (∆G
- 64. Термодинамические особенности открытых систем для живого организма ( постоянство кислотно-основного, гетерогенного, лигандообменного баланса) объясняют его устойчивость,
- 65. В основе гомеостаза организма находятся следующие химические и физико-химические балансы: Кислотно-основной Окислительно-восстановительный Металло-лигандный Гидрофильно-липофильный Водно-электролитный
- 66. Человеческий организм, является открытой, стационарной термодинамической системой. Основным источником энергии для него является химическая энергия, заключенная
- 67. Главными компонентами пищи являются: углеводы, жиры, белки
- 68. Углеводы – CnH2nOn (сахар, хлеб, крупы, макаронные изделия) В процессе усвоения углеводы расщепляются до моносахаридов, которые
- 69. Белки - основной строительный материал клеток (рыба, творог, сыр, говядина, крупы) Вещества, молекулы которых состоят из
- 70. Жиры - сложные эфиры глицерина и жирных кислот. где R, R' и R" — радикалы жирных
- 71. Запас жира позволяет представителям животного мира некоторое время обходиться без потребления воды, поскольку при окислении 100
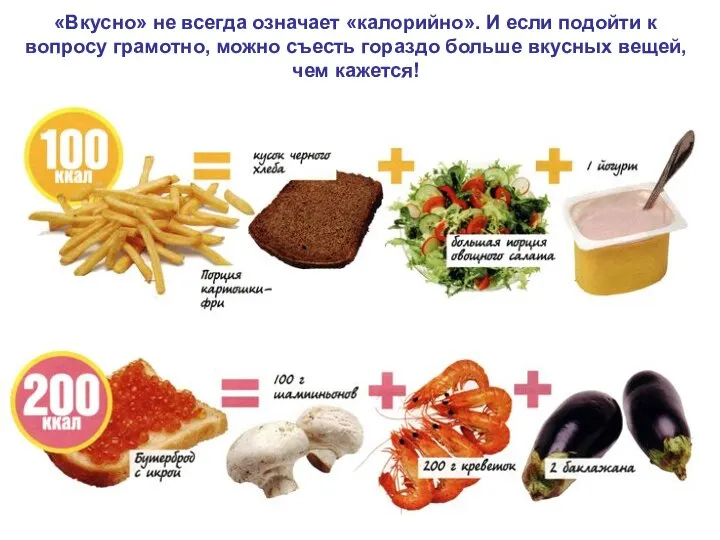
- 73. «Вкусно» не всегда означает «калорийно». И если подойти к вопросу грамотно, можно съесть гораздо больше вкусных
- 75. Аналогичный подход относится к витаминам Без витамина Е мы страдали бы от простуд, нам бы угрожали
- 76. В основе научной диетологии лежит согласование режима питания (калорийности потребляемой человеком пищи) с расходом энергии, который
- 77. Суточная потребность человека в энергии 1) при легкой работе в сидячем положении: канцелярские работники, секретари, портные,
- 78. 2) при умеренной и напряженной мышечной работе: лаборанты, врачи, почтальоны, столяры, токари, трактористы, учащиеся, студенты -
- 79. 3) при тяжелом физическом труде: литейщики, каменщики, кузнецы, плотники, пахари – 4000- 5000 ккал (16700-20900 кДж
- 80. 4) при особо тяжелом труде - ручная косьба, спортсмены - до 7200 ккал ( 30100 кДж
- 82. Скачать презентацию































































 Направление исследований в биофармации
Направление исследований в биофармации Строение молекулы воды
Строение молекулы воды Перманганат калия
Перманганат калия АЛЬДЕГИДЫ - органические соединения, содержащие карбонильную группу, в которой атом углерода связан с радикалом и одним атомом во
АЛЬДЕГИДЫ - органические соединения, содержащие карбонильную группу, в которой атом углерода связан с радикалом и одним атомом во Кислотные дожди
Кислотные дожди Свойства океанической воды
Свойства океанической воды Липиды, биологическая роль, классификация
Липиды, биологическая роль, классификация The Krebs cycle
The Krebs cycle Виды присадок к моторному топливу. Керосин
Виды присадок к моторному топливу. Керосин Презентация по Химии "Номенклатура алканов разветвлённого строения" - скачать смотреть
Презентация по Химии "Номенклатура алканов разветвлённого строения" - скачать смотреть  Обобщение знание и умений и предельных и непредельных углеводородах
Обобщение знание и умений и предельных и непредельных углеводородах Комплексные соединения
Комплексные соединения Allgemeine Chemie für PharmazeutInnen
Allgemeine Chemie für PharmazeutInnen Кремний и его соединения
Кремний и его соединения Свинец (Pb)
Свинец (Pb) Виды присадок к моторным топливам (бензин)
Виды присадок к моторным топливам (бензин) Лексикология и фразеология Однозначные и многозначные слова Прямое и переносное значение слова
Лексикология и фразеология Однозначные и многозначные слова Прямое и переносное значение слова Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Получение металлов. Металлы в природе
Получение металлов. Металлы в природе Фiзико-хімічні основи розвитку пожеж. Тепломасообмін, температурний режим пожежі в огородженні. (Розділ 4.13.5)
Фiзико-хімічні основи розвитку пожеж. Тепломасообмін, температурний режим пожежі в огородженні. (Розділ 4.13.5) Горные породы
Горные породы Биологически активные вещества. Витамины. Ферменты. Гормоны
Биологически активные вещества. Витамины. Ферменты. Гормоны Каучук и резина
Каучук и резина Формирование и развитие системы знаний о химической реакции
Формирование и развитие системы знаний о химической реакции Нитраттарды қолдану
Нитраттарды қолдану Основы коррозии и защиты металлов. Химическая коррозия
Основы коррозии и защиты металлов. Химическая коррозия Изучение физико-химических показателей качества сушек
Изучение физико-химических показателей качества сушек Работу выполняла: Шумкова Елизавета. Руководитель: Шилоносова Елена Леонидовна.
Работу выполняла: Шумкова Елизавета. Руководитель: Шилоносова Елена Леонидовна.