Содержание
- 2. 1. Основные понятия термохимии Термохимия - раздел физической химии изучающий тепловые эффекты, сопровождающие химические и физико-химические
- 3. 1. Основные понятия термохимии Химическая реакция как термодинамический процесс, заключается в превращении одних веществ в другие,
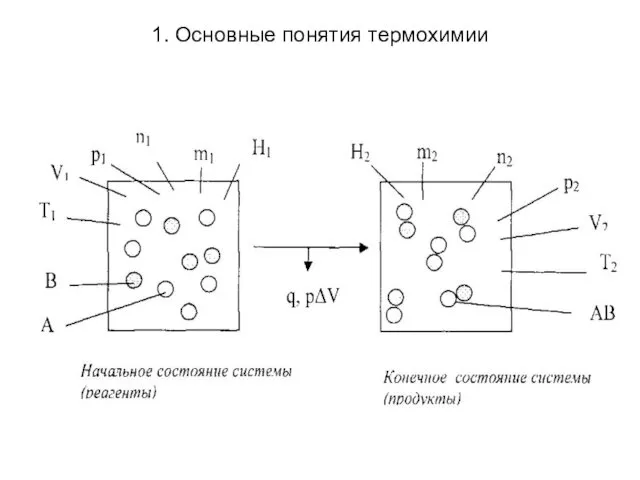
- 4. 1. Основные понятия термохимии
- 5. 1. Основные понятия термохимии Для физико-химических процессов действует закон сохранения массы, установленный М.В. Ломоносовым (m1 =
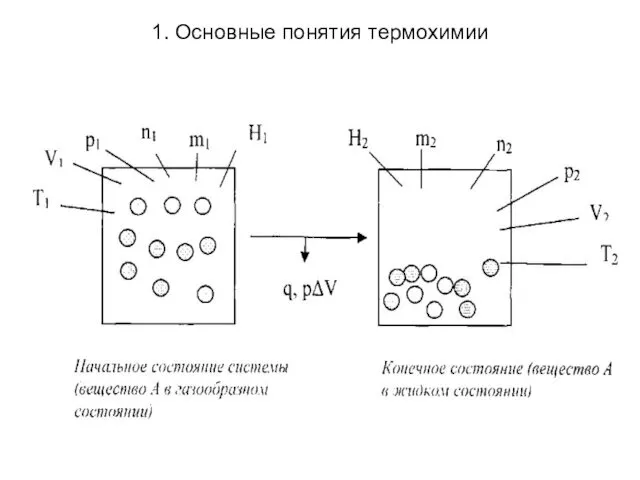
- 6. 1. Основные понятия термохимии Фазовый переход - переход вещества из одной фазы в другую, связанный с
- 7. 1. Основные понятия термохимии
- 8. 1. Основные понятия термохимии Термохимия рассматривает процессы превращения частиц вещества: диссоциацию молекул простых газообразных веществ на
- 9. 1. Основные понятия термохимии Тепловой эффект этих процессов позволяет определить важнейшие физические величины, характеризующие свойства вещества:
- 10. 1. Основные понятия термохимии Термохимическое уравнение - условное изображение физико-химического процесса, в котором помимо формул и
- 11. 1. Основные понятия термохимии Тепловой эффект (Q, kДж/моль) - энергия, которая выделяется или поглощается в форме
- 12. 1. Основные понятия термохимии Стандартный тепловой эффект - теплота физико-химического процесса, протекающего в стандартных условиях: Т=298К,
- 13. 1. Основные понятия термохимии К основным способам выражения тепловых эффектов физико-химических процессов относят: Теплоту образования ΔНобр
- 14. 1. Основные понятия термохимии 2. Теплоту сгорания ΔНсгор - тепловой эффект химической реакции окисления 1 моль
- 15. 1. Основные понятия термохимии 3. Теплоту нейтрализации ΔНнейт - тепловой эффект взаимодействия 1 эквивалента кислоты и
- 16. 1. Основные понятия термохимии 4. Теплоту фазовых переходов ΔН°ф.п. - тепловой эффект перехода 1 моль вещества
- 17. 1. Основные понятия термохимии 5. Теплоту растворения. Поскольку тепловой эффект при растворении зависит от концентрации раствора,
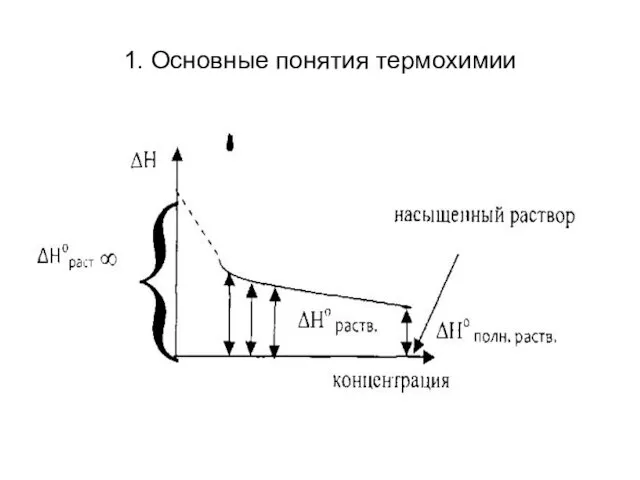
- 18. 1. Основные понятия термохимии Предельная интегральная теплота растворения ΔН°раст ∞ - изменение энтальпии при растворении 1
- 19. 1. Основные понятия термохимии
- 20. 1. Основные понятия термохимии 6. Энергия связи - теплота, выделяющаяся в процессе образования связи между двумя
- 21. 2. Закон Гесса и его следствия В 1836 г. профессор Петербургского горного института Герман Иванович Гесс
- 22. 2. Закон Гесса и его следствия Закон Гесса позволяет обращаться с термохимическими уравнениями, как с алгебраическими,
- 23. 2. Закон Гесса и его следствия 1-е следствие закона Гесса: тепловой эффект разложения какого-либо вещества точно
- 24. 2. Закон Гесса и его следствия 2 -e следствие: тепловой эффект реакции равен алгебраической сумме теплот
- 25. 2. Закон Гесса и его следствия
- 26. 2. Закон Гесса и его следствия 3 - е следствие: тепловой эффект реакции равен алгебраической сумме
- 27. 2. Закон Гесса и его следствия 4 —е следствие: если совершаются две реакции, приводящие из различных
- 28. 2. Закон Гесса и его следствия 5 —е следствие: если совершаются две реакции, приводящие из одинаковых
- 29. 3. Зависимость теплоты процесса от темп. З-н Кирхгоффа Все описанные выше расчеты тепловых эффектов, основанные на
- 30. 3. Зависимость теплоты процесса от темп. З-н Кирхгоффа Тепловой эффект химической реакции зависит от температуры. Эта
- 31. 3. Зависимость теплоты процесса от темп. З-н Кирхгоффа
- 32. 3. Зависимость теплоты процесса от темп. З-н Кирхгоффа Согласно этой схеме, переход из начального состояния (вещества
- 33. 3. Зависимость теплоты процесса от темп. З-н Кирхгоффа Согласно закону Гесса, ΔНТ1 + ΔН3 + ΔН4
- 34. 3. Зависимость теплоты процесса от темп. З-н Кирхгоффа Полученное уравнение является интегральной формой уравнения Кирхгоффа, связывающего
- 35. 3. Зависимость теплоты процесса от темп. З-н Кирхгоффа Интегральная форма уравнения Кирхгоффа Дифференциальная форма уравнения Кирхгоффа
- 36. 3. Зависимость теплоты процесса от темп. З-н Кирхгоффа Аналогично, можно показать, что справедливы следующие соотношения для
- 37. 3. Зависимость теплоты процесса от темп. З-н Кирхгоффа Уравнения Кирхгоффа в дифференциальной форме позволяют качественно оценить
- 39. Скачать презентацию

































 Природные полимеры. Белки и нуклеиновые кислоты
Природные полимеры. Белки и нуклеиновые кислоты Презентация Теллур
Презентация Теллур Алмаз (С)
Алмаз (С) Свойства спирта и воды
Свойства спирта и воды Стероиды, их химическое и пространственное строение
Стероиды, их химическое и пространственное строение Химический тренажер. Химические элементы
Химический тренажер. Химические элементы Білки. Властивості та функції
Білки. Властивості та функції Лабораторное оборудование, посуда и средства защиты Разработка для проведения практических работ по химии подготовила Нерев
Лабораторное оборудование, посуда и средства защиты Разработка для проведения практических работ по химии подготовила Нерев Презентация по химии ХИМИЧЕСКАЯ СВЯЗЬ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ
Презентация по химии ХИМИЧЕСКАЯ СВЯЗЬ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ  Презентация по Химии "Соединения" - скачать смотреть бесплатно
Презентация по Химии "Соединения" - скачать смотреть бесплатно The application nanotechnology in chemistry
The application nanotechnology in chemistry Основания. Состав оснований
Основания. Состав оснований Щелочные металлы
Щелочные металлы Природный каучук
Природный каучук Закон збереження маси речовини. Хімічні рівняння
Закон збереження маси речовини. Хімічні рівняння АВТОР: НАЗАРЕНКО МАКСИМ ВОЛОДИМИРОВИЧ 10-А КЛАС,ГІМНАЗІЯ №32 ПЕЧЕРСЬКИЙ РАЙОН, М. КИЇВ ПЕДАГОГІЧНИЙ КЕРІВНИК: КУЗНЄЦОВА ЛЮДМИ
АВТОР: НАЗАРЕНКО МАКСИМ ВОЛОДИМИРОВИЧ 10-А КЛАС,ГІМНАЗІЯ №32 ПЕЧЕРСЬКИЙ РАЙОН, М. КИЇВ ПЕДАГОГІЧНИЙ КЕРІВНИК: КУЗНЄЦОВА ЛЮДМИ Свойства металлов Свойства металлов
Свойства металлов Свойства металлов Вещественный состав магматических горных пород
Вещественный состав магматических горных пород Хімія як наука
Хімія як наука Фосфаттар - минералдар класы - ортофосфорлы қышқыл (Н3РO4) тұздары
Фосфаттар - минералдар класы - ортофосфорлы қышқыл (Н3РO4) тұздары Генезис различных типов промежуточных фаз. Теория плотнейших упаковок
Генезис различных типов промежуточных фаз. Теория плотнейших упаковок Қатты дене-сұйық жанасу шегіндегі адсорбция
Қатты дене-сұйық жанасу шегіндегі адсорбция Степень окисления. Бинарные соединения металлов и не металлов: оксиды, хлориды, сульфиды и др.
Степень окисления. Бинарные соединения металлов и не металлов: оксиды, хлориды, сульфиды и др.  Химическая природа и состав нефти и газа. Физико-химические свойства нефтей и нефтепродуктов
Химическая природа и состав нефти и газа. Физико-химические свойства нефтей и нефтепродуктов Элементы третьего периода, периодической системы Д. И. Менделеева
Элементы третьего периода, периодической системы Д. И. Менделеева Программа «Gaussian»
Программа «Gaussian» Электролитическая диссоциация
Электролитическая диссоциация Обобщающий урок по теме «Основные классы неорганических веществ»
Обобщающий урок по теме «Основные классы неорганических веществ»