Содержание
- 2. Основания – это сложные вещества, состоящие из атома металла и одной или нескольких гидроксогрупп.
- 3. Состав оснований: Назовите составные части оснований. Ме(ОН)х Валентность гидроксогруппы (ОН) – I Количество гидроксогрупп определяется валентностью
- 4. Выберите формулы оснований. Назовите их. НСl, NaOH, Na2O, Ca(OH)2, H2SO4, P2O5, Fe(OH)3, MgO, Cи(OH)2
- 5. Основания NaOH – гидроксид натрия Ca(OH)2 – гидроксид кальция Fe(OH)3 – гидроксид железа (III) Cи(OH)2 –
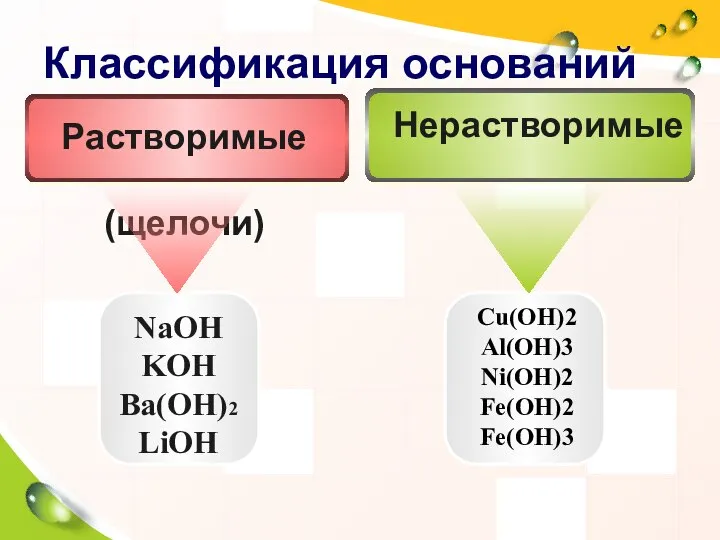
- 6. Классификация оснований NaOH KOH Ba(OH)2 LiOH Cu(OH)2 Al(OH)3 Ni(OH)2 Fe(OH)2 Fe(OH)3 Нерастворимые Растворимые (щелочи)
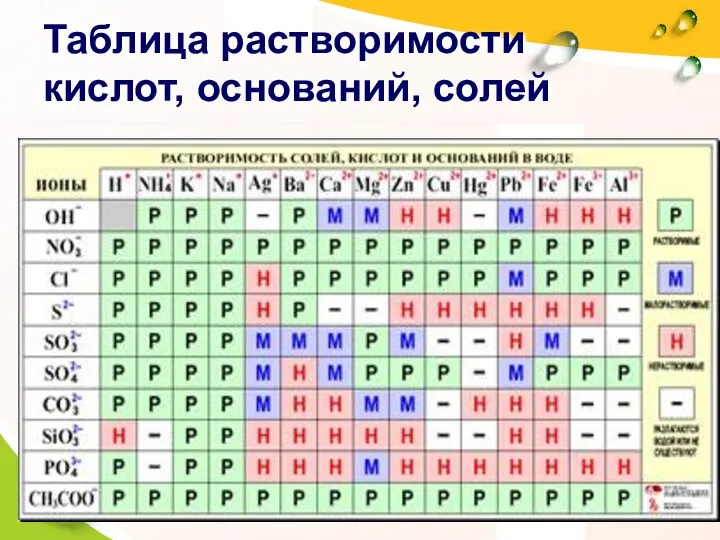
- 7. Таблица растворимости кислот, оснований, солей
- 9. По какому признаку основания разделены на группы? NaOH KOH LiOH СsOH Cu(OH)2 Ba(OH)2 Pb(OH)2 Fe(OH)2 Al(OH)3
- 10. Однокислотные NaOH, KOH Двухкислотные Pb(OH)2, Fe(OH)2 Трехкислотные Al(OH)3 Классификация оснований по числу гидроксогрупп. Основания
- 11. Физические свойства оснований Агрегатное состояние: Все твердые вещества Цвет кислот: Белого – КОН, Голубого - Cu(OH)2
- 12. Химические свойства нерастворимых оснований. 1). Разлагаются при нагревании. 2). Взаимодействуют с кислотами (реакция нейтрализации).
- 13. Химические свойства щелочей. 1). Изменяют окраску индикаторов. Взаимодействуют с: 2). кислотами (реакция нейтрализации), 3). кислотными оксидами,
- 14. ПРАВИЛА БЕЗОПАСНОСТИ Едкое вещество—щелочь! Разрушает и раздражает кожу, слизистые оболочки. Попавшие на кожу капли раствора щелочи
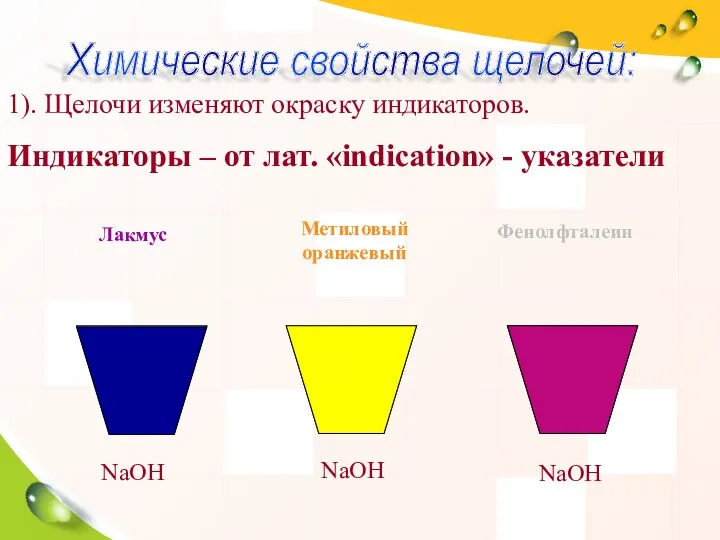
- 15. 1). Щелочи изменяют окраску индикаторов. Индикаторы – от лат. «indication» - указатели NaOH NaOH NaOH Лакмус
- 16. Щелочь + кислота : Ва(ОН)2 + 2НСl = ВаСl2 + 2Н2О хлорид бария Химические свойства щелочей:
- 18. Скачать презентацию












 Көміртек
Көміртек Аминокислоты. Белки
Аминокислоты. Белки Начала органической химии
Начала органической химии Основы химической технологии
Основы химической технологии Презентация по Химии "Обобщение" - скачать смотреть
Презентация по Химии "Обобщение" - скачать смотреть  Некоторые структурные особенности макромолекул
Некоторые структурные особенности макромолекул Тривиальные названия неорганических соединений
Тривиальные названия неорганических соединений Физиология бактерий. Химический состав бактериальной клетки
Физиология бактерий. Химический состав бактериальной клетки Physical chemistry of nanostructured systems
Physical chemistry of nanostructured systems Алкалоиды, производные хинолина, изохинолина. Общая характеристика, методы анализа
Алкалоиды, производные хинолина, изохинолина. Общая характеристика, методы анализа Моделирование (7 класс)
Моделирование (7 класс) Материаловедение. Теория термической обработки стали. (Тема 8)
Материаловедение. Теория термической обработки стали. (Тема 8) Вуглеводні. Насичені, ненасичені та ароматичні вуглеводні: їх склад, будова, фізичні та хімічні властивості
Вуглеводні. Насичені, ненасичені та ароматичні вуглеводні: їх склад, будова, фізичні та хімічні властивості Методы обучения химии
Методы обучения химии Презентация по Химии "Сульфатна кислота і сульфати." - скачать смотреть бесплатно
Презентация по Химии "Сульфатна кислота і сульфати." - скачать смотреть бесплатно Показатель концентрации водородных ионов (лекция 6)
Показатель концентрации водородных ионов (лекция 6) Урок в 8 классе На тему ???
Урок в 8 классе На тему ??? Физические и химические явления. Химические реакции
Физические и химические явления. Химические реакции Полимеры, пластмассы и изделия из них
Полимеры, пластмассы и изделия из них Карбонильные соединения (оксосоединения). 10 класс
Карбонильные соединения (оксосоединения). 10 класс Презентация по Химии "8 класс Обобщение знаний по теме СЛОЖНЫЕ ВЕЩЕСТВА" - скачать смотреть бесплатно
Презентация по Химии "8 класс Обобщение знаний по теме СЛОЖНЫЕ ВЕЩЕСТВА" - скачать смотреть бесплатно Свойства растворов ВМС: особенности растворения, реологические свойства, осмос. Устойчивость растворов ВМС
Свойства растворов ВМС: особенности растворения, реологические свойства, осмос. Устойчивость растворов ВМС Комплексы хлорида и иодида цинка (II) с карбамидом: синтез, характеристика и биологическая активность
Комплексы хлорида и иодида цинка (II) с карбамидом: синтез, характеристика и биологическая активность Применение неметаллов
Применение неметаллов Презентация по Химии "Оксиды. Состав. Классификация. Номенклатура. Свойства. Получение. Применение" - скачать смотреть бесплат
Презентация по Химии "Оксиды. Состав. Классификация. Номенклатура. Свойства. Получение. Применение" - скачать смотреть бесплат Презентация по Химии "Органические вещества. Нуклеиновые кислоты" - скачать смотреть
Презентация по Химии "Органические вещества. Нуклеиновые кислоты" - скачать смотреть  Подготовлено ученицей 9 "А" класса Михневской СОШ Темновой Яной.
Подготовлено ученицей 9 "А" класса Михневской СОШ Темновой Яной. Химические свойства металлов
Химические свойства металлов