Содержание
- 2. Мы начинаем наш турнир, Для чего и зачем? Чтоб лучше химию познать И все ответы разгадать!
- 3. Разминка «Галерея химиков». 4. 2. 1. 3.
- 4. «Галерея химиков». Ответ: 1) Йёнс Якоб Берцелиус 2) Михайло Ломоносов 3) Дмитрий Менделеев 4) Мари́я Склодо́вская-
- 5. Блок № 1 «Атомы химических элементов, строение атома» Задание № 1 1.Оксид меди - это сложное
- 6. 2. При разложении воды электрическим током, образуются два простых вещества - водород и кислород. 3. Сложное
- 7. 4. Простое вещество - азот называют безжизненным, но в то же время без химического элемента азота
- 8. Задание № 2 В каком ряду формулы веществ записаны в порядке возрастания их молярной массы (указать
- 9. Ответ: 1) NaOH, CaO, MgCl2, Cu(OH)2 М (NaOH) = 40 г/ моль М (CaO) = 56
- 10. Задание № 3 Определите химический элемент по предложенным данным: 1) 15р + , 16n0 , 15e
- 11. Задание № 4 Символ изотопа элемента: а) 3014Э; б) 8737Э Укажите: 1. название элемента; 2. число
- 12. Задание № 4 Ответ: а) 3014Э Si кремний 14 протонов и 16 нейтронов 14 электронов в
- 13. Из вулканов появляюсь, И в воде не растворяюсь, В кислотном ряду командиром иду. Очищаю нефть и
- 14. СЕРА
- 15. Хранят обычно в керосине, И «бегает» он по воде, В природе, помните отныне, Свободным нет его
- 16. НАТРИЙ
- 17. Отгадаем без проблем, Элемент известный всем. Входит он в состав оксидов, И в кислоты разных видов,
- 18. ХЛОР
- 19. Блок № 2 «Простые и сложные вещества. Структура Периодической системы химических элементов Д. И. Менделеева.» Задание
- 20. Ответ:
- 21. Задание № 2 Определить период, группу и подгруппу, в которых находятся элементы с порядковыми номерами 37
- 22. Ответ: элемент с № 37 - рубидий Rb, Ar (Rb) = 85 элемент с № 17
- 23. Задание № 3 Наиболее ярко выраженные неметаллические свойства имеет: а) S б) P в) Ar г)
- 24. Ответ: Аргон, 3 период, 8 группа, главная (А) подгруппа. +18, 18р, 22n 18е (2е, 8е, 8е)
- 25. Задание № 4 В каком ряду химические элементы расположены в порядке возрастания их атомных радиусов: 1.
- 26. Ответ: 2) Li, Na, K, Rb. Наиболее ярко выражены металлические свойства у рубидия.
- 27. Ребусы
- 28. Никель Иод Азот Бор Марганец Кремний Мышьяк Углерод Цирконий Аргон Медь Криптон
- 29. Блок № 3 Классификация сложных неорганических соединений
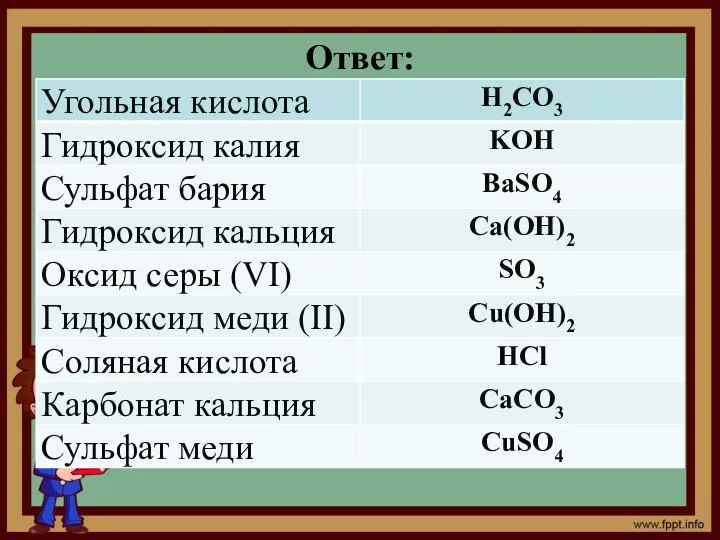
- 30. Задание № 1 Пред вами названия веществ поставьте в соответствие с ними их формулы.
- 31. Ответ:
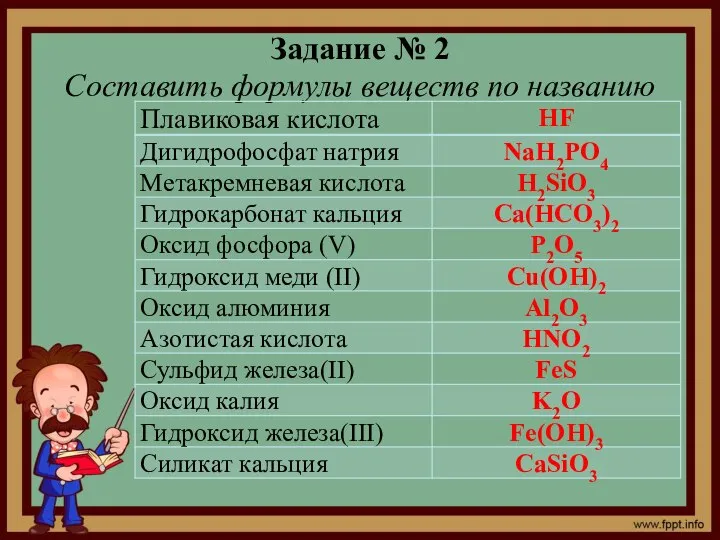
- 32. Задание № 2 Составить формулы веществ по названию
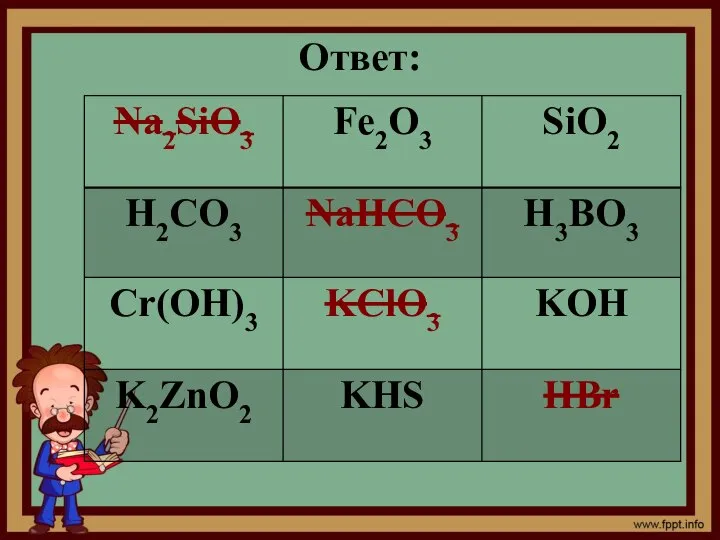
- 33. Задание № 3 «Третий лишний». Вычеркнуть формулу вещества в каждом горизонтальном ряду, которое принадлежит к другому
- 34. Ответ:
- 35. Из меня состоит всё живое. Я графит, антрацит и алмаз. Я на улице, в школе и
- 36. УГЛЕРОД
- 37. Не трудна загадка эта, Ведь металл - родня планете.
- 38. УРАН
- 39. Прославлен всеми именами Металл, испытанный огнём, Манил к себе людей веками, Алхимик жил мечтой о нём.
- 40. ЗОЛОТО
- 41. Блок № 4. «Химические реакции (типы реакций, составление уравнений реакций)» Расставить коэффициенты и указать тип реакции.
- 42. Ответ: 3MnO2 + 4Al → 2Al2O3 + 3Mn - замещения 2H2O2 →2 H2O + O2↑ -
- 43. Задание № 2 Дописать уравнение химической реакции. сера + …. = оксид серы (IV) нитрат серебра
- 44. Ответ: S + O2 = SO2 AgNO3 + HCl = AgCl↓ + HNO3 BaCl2 + Na2SO4
- 45. Задание № 3 Дописать уравнения реакций ионного обмена с учетом признаков реакций, расставить коэффициенты. Для реакций
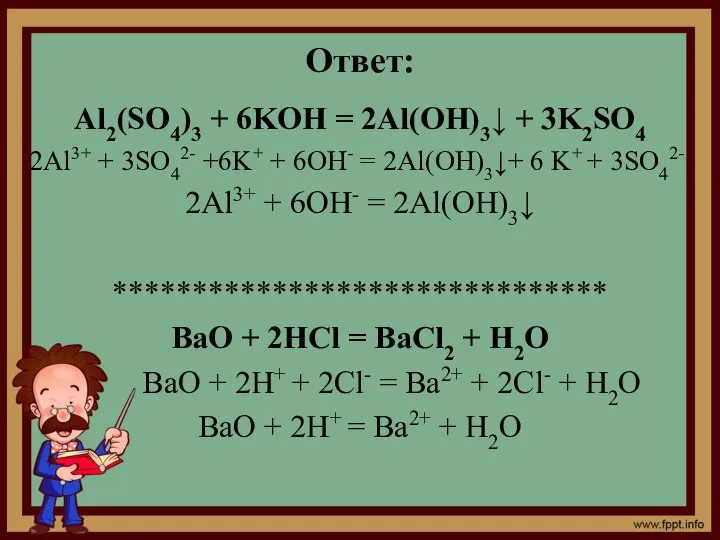
- 46. Ответ: Al2(SO4)3 + 6KOH = 2Al(OH)3↓ + 3K2SO4 2Al3+ + 3SO42- +6K+ + 6OH- = 2Al(OH)3↓+
- 47. Mg + H2SO4 = MgSO4 + H2↑ не реакция ионного обмена ********************* MgCl2 + 2NaOH =
- 48. Я металл серебристый и лёгкий, Я зовусь самолётный металл, И покрыт я оксидною плёнкой, Чтоб меня
- 49. АЛЮМИНИЙ
- 50. Без него мы жить не можем- Он всегда нам всем поможет. Он находится везде – И
- 51. КИСЛОРОД
- 52. Задание на смекалку Составьте как можно больше формул веществ, используя следующие символы: O N Na S
- 54. Скачать презентацию






































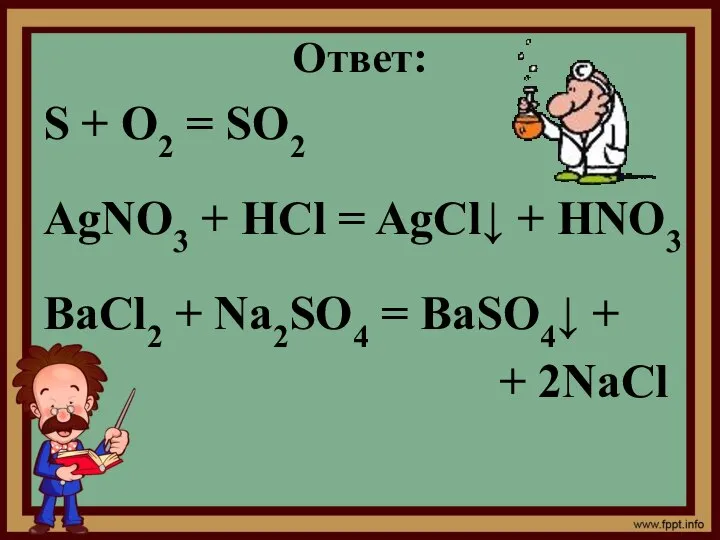







 Презентация на тему: Кислотные дожди
Презентация на тему: Кислотные дожди Химиялық тепе-теңдік және оның ығысуына әсер етуші жағдайлар. Ле Шателье-Браун принциптері
Химиялық тепе-теңдік және оның ығысуына әсер етуші жағдайлар. Ле Шателье-Браун принциптері Методы разделения белковых смесей. Электрофорез
Методы разделения белковых смесей. Электрофорез Основные классы органических соединений. Углеводороды
Основные классы органических соединений. Углеводороды Многоатомные спирты
Многоатомные спирты Кислород. Свойства кислорода
Кислород. Свойства кислорода Презентация Витамин Е
Презентация Витамин Е  ZnS и ZnSe как оптические материалы,люминофоры, лазерные матрицы
ZnS и ZnSe как оптические материалы,люминофоры, лазерные матрицы Строение атома, изотопы
Строение атома, изотопы Методические проблемы преподавания органической химии и ее основные теоретические понятия
Методические проблемы преподавания органической химии и ее основные теоретические понятия Состав краски
Состав краски Биополимеры
Биополимеры "Металлы тоже воевали…" урок по химии в 8 классе Учитель Герасименко Е.В.
"Металлы тоже воевали…" урок по химии в 8 классе Учитель Герасименко Е.В. Группы атомов водорода (12 групп)
Группы атомов водорода (12 групп) Аттестационная работа. Методразработка по проведению исследовательской работы Выращивание кристаллов в домашних условиях
Аттестационная работа. Методразработка по проведению исследовательской работы Выращивание кристаллов в домашних условиях Важнейшие химические понятия и законы
Важнейшие химические понятия и законы Кристалічні та аморфні тіла. Рідкі кристали та їх властивості. Підготувала учениця 10 класу Стрельчук Катерина
Кристалічні та аморфні тіла. Рідкі кристали та їх властивості. Підготувала учениця 10 класу Стрельчук Катерина  Арены и ароматичность
Арены и ароматичность Кинетика сложных реакций
Кинетика сложных реакций Полимеры. Каучуки. Резина
Полимеры. Каучуки. Резина Номенклатура органических соединений. Структурные формулы соединений. Алканы. (Лабораторная работа 2)
Номенклатура органических соединений. Структурные формулы соединений. Алканы. (Лабораторная работа 2) Природный каучук
Природный каучук Реакции ионного обмена
Реакции ионного обмена Презентация по Химии "Глюкоза. Строение. Физические и химические свойства" - скачать смотреть
Презентация по Химии "Глюкоза. Строение. Физические и химические свойства" - скачать смотреть  Презентация по Химии "Алюминий и его соединения" - скачать смотреть
Презентация по Химии "Алюминий и его соединения" - скачать смотреть  Алкалоиды, производные тропана
Алкалоиды, производные тропана Дисахариды и полисахариды
Дисахариды и полисахариды Анілін. Фізичні властивості
Анілін. Фізичні властивості