Углерод и его соединения Лекция.(§29 -30, с.172 -178). Цель: Какие соединения образует углерод? Какие свойства, связанные со строением атома углерода, характерны для углерода и его соединений? Где находят применение соединения углерода?
Содержание
- 2. Необходимо вспомнить. Положение химического элемента в таблице Д.И.Менделеева. Электронная формула атома углерода. Какие высшую и низшую
- 3. Нам известно, что Углерод – химический элемент с порядковым номером 6, расположен во 2 периоде, ΙVгруппе
- 4. Составить конспект-ответ, придерживаясь следующих вопросов. Какова форма существования химического элемента углерода? Какого строение атома углерода? Какие
- 5. Соединения углерода.
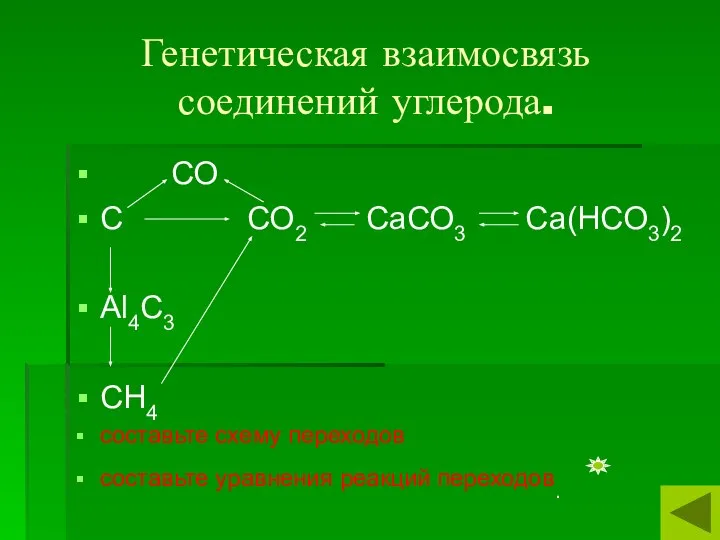
- 6. Генетическая взаимосвязь соединений углерода. СО С СО2 СаСО3 Са(НСО3)2 Аl4С3 СН4 составьте схему переходов составьте уравнения
- 7. 4Al + 3С → Al4С3 Al4С3 + 12H2O → 4Al(OH)3 +3CH4↑ CH4 + 2O2 → CO2
- 8. 1.Качественная реакция на СО32- = получение СО2 в лаборатории. 2.Качественная реакция на СО2. 1) СаСО3 +
- 9. Переход карбонаты в гидрокарбонаты и обратно. СаСО3 + СО2 + Н2О → Са(НСО3)2 t исчезновение помутнения
- 11. Скачать презентацию




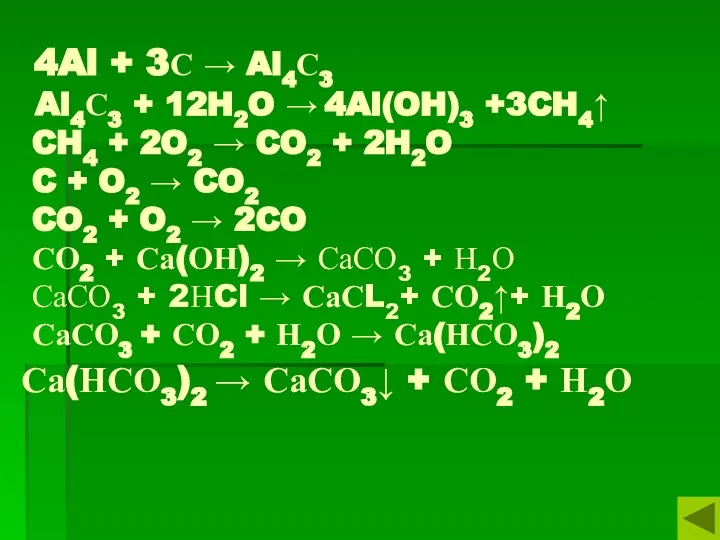


 Уран. Применение. Ядерное топливо
Уран. Применение. Ядерное топливо Заседание временного творческого коллектива ОМО УГПС Технологии материалов, УГПС Химические технологии
Заседание временного творческого коллектива ОМО УГПС Технологии материалов, УГПС Химические технологии КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ Лекция по теме: «Обмен белко
КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ Лекция по теме: «Обмен белко Классификация сталей
Классификация сталей Реакции окисления различных классов органических соединений
Реакции окисления различных классов органических соединений «Созвездие талантов». Игра-зачет по теме «Основные классы неорганической химии» 8 класс
«Созвездие талантов». Игра-зачет по теме «Основные классы неорганической химии» 8 класс Вторичная переработка нефти. Лекция 9
Вторичная переработка нефти. Лекция 9 Сложные эфиры. Жиры
Сложные эфиры. Жиры Хлор. Нахождение в природе
Хлор. Нахождение в природе Празеодим
Празеодим Многоатомные Спирты
Многоатомные Спирты  Биологическая химия с основами физической и коллоидной химии
Биологическая химия с основами физической и коллоидной химии Биосинтез углеводов в организме. Метаболизм гексоз. (Лекция 11)
Биосинтез углеводов в организме. Метаболизм гексоз. (Лекция 11) Обзор основных методов исследования супрамолекулярных объектов
Обзор основных методов исследования супрамолекулярных объектов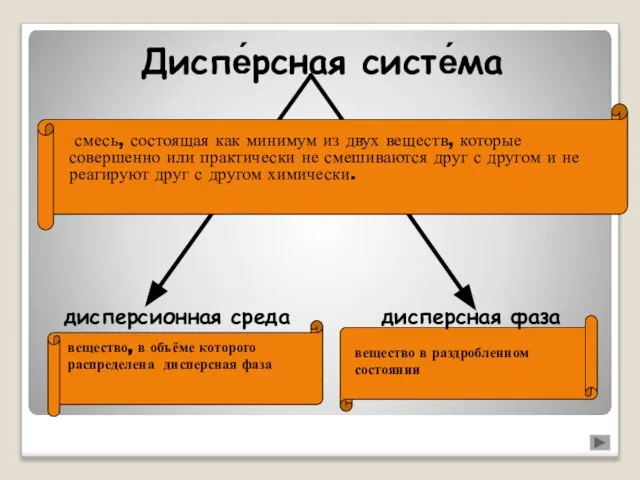 Дисперсные системы
Дисперсные системы Разработка системы подготовки лаборанта химического анализа
Разработка системы подготовки лаборанта химического анализа Элементы группы VII B
Элементы группы VII B Геохимия природных процессов. Редкие элементы, как индикаторы геодинамических обстановок формирования комплексов. (Лекция 5)
Геохимия природных процессов. Редкие элементы, как индикаторы геодинамических обстановок формирования комплексов. (Лекция 5) Применение этанола
Применение этанола Закономерности протекания химических реакций. Основы химической термодинамики. Лекция 6
Закономерности протекания химических реакций. Основы химической термодинамики. Лекция 6 Кислоты. Классификация кислот
Кислоты. Классификация кислот Презентация "Основания"
Презентация "Основания" Высoкомолекулярные соединения (ВМС). Основные понятия. Химическое строение
Высoкомолекулярные соединения (ВМС). Основные понятия. Химическое строение Радиофармацевтическая химия
Радиофармацевтическая химия Экзогенная серия. Группа выветривания
Экзогенная серия. Группа выветривания Колообіг фосфору у природі
Колообіг фосфору у природі  Обмен липидов
Обмен липидов Основы химической термодинамики. Термохимические расчеты
Основы химической термодинамики. Термохимические расчеты