Влияние производных бензохинона на радиационно-индуцированную фрагментацию биомолекул и моделирующих их соединений
Содержание
- 2. Цель исследования: Изучить радикалрегуляторные свойства тимохинона по отношению к органическим радикалам, образующимся при γ-радиолизе деаэрированных водных
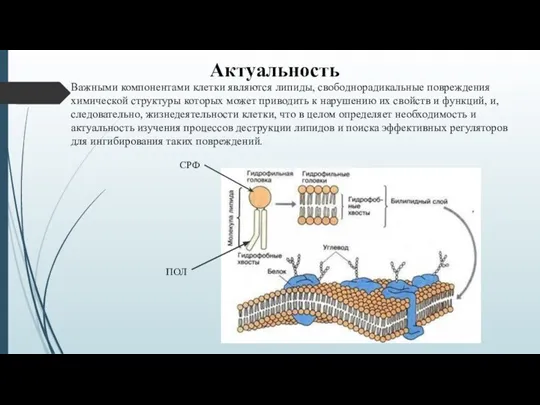
- 3. Актуальность Важными компонентами клетки являются липиды, свободнорадикальные повреждения химической структуры которых может приводить к нарушению их
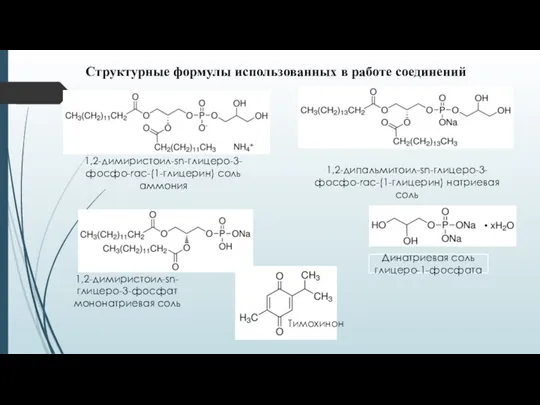
- 5. Структурные формулы использованных в работе соединений
- 6. Тимохинон является активным компонентом выделенным из растения Nigella Sativa, которое является широко используемым в восточной медицине
- 7. Методика эксперимента Концентрации тестируемого соединения в деаэрированных растворах глицерофосфата составляли 10-4÷2×10-3 моль/л, водных растворов глицеро-1-фосфата –
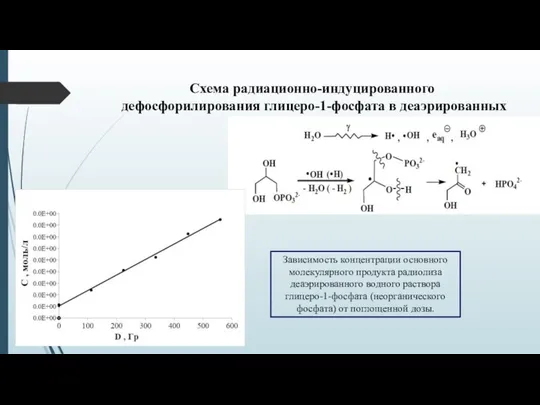
- 8. Схема радиационно-индуцированного дефосфорилирования глицеро-1-фосфата в деаэрированных водных растворах: Зависимость концентрации основного молекулярного продукта радиолиза деаэрированного водного
- 9. Влияние тимохинона на радиационно-химическое дефосфорилирование глицеро-1-фосфата (0,001 М) в деаэрированных водных растворах при рН=7.
- 10. Влияние тимохинона на радиационно-химическое дефосфорилирование глицеро-1-фосфата (0,01 М) в деаэрированных водных растворах при рН=7.
- 11. Влияние тимохинона на радиационно-химическое дефосфорилирование глицеро-1-фосфата (0,1 М) в деаэрированных водных растворах при рН=7.
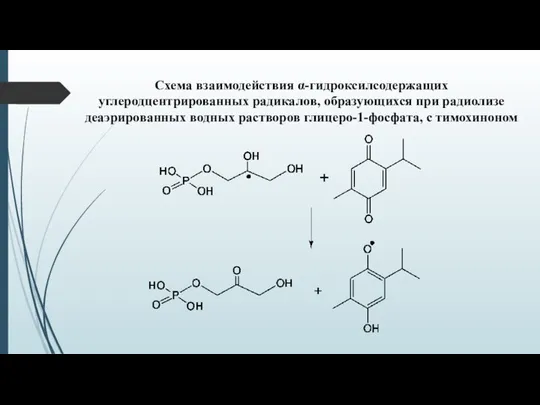
- 12. Схема взаимодействия α-гидроксилсодержащих углеродцентрированных радикалов, образующихся при радиолизе деаэрированных водных растворов глицеро-1-фосфата, с тимохиноном
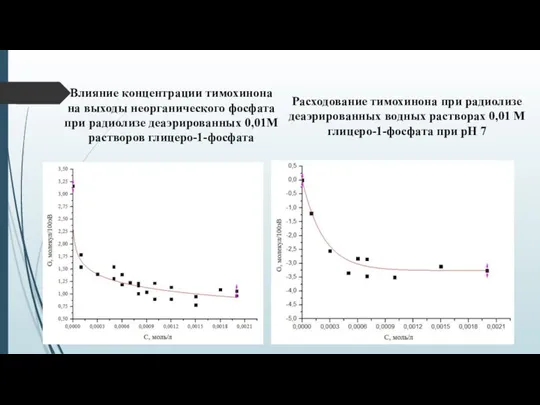
- 13. Влияние концентрации тимохинона на выходы неорганического фосфата при радиолизе деаэрированных 0,01М растворов глицеро-1-фосфата Расходование тимохинона при
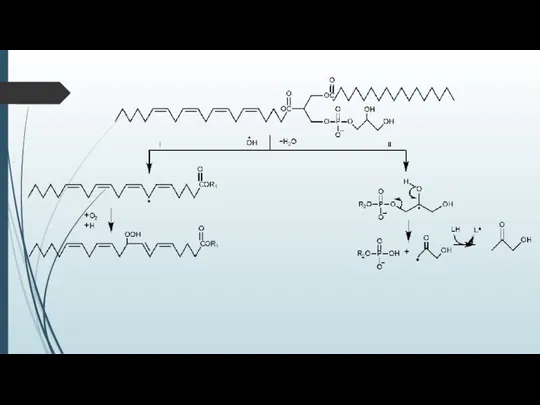
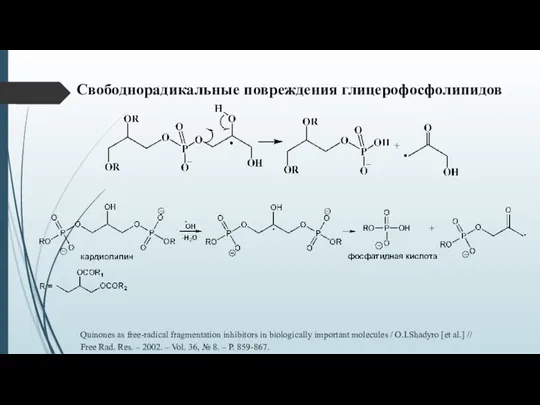
- 14. Свободнорадикальные повреждения глицерофосфолипидов Quinones as free-radical fragmentation inhibitors in biologically important molecules / O.I.Shadyro [et al.]
- 15. Масс-спектр 1,2-димиристоил-sn-глицеро-3-фосфо-rac-(1-глицерин) соли аммония [M-NH4]-
- 16. Масс-спектр 1,2-димиристоил-sn-глицеро-3-фосфат мононатриевой соли [M-Na]-
- 17. Выводы Тимохинон эффективно подавляет радиационно-индуцированные процессы дефосфорилирования глицеро-1-фосфата в эквимолярных с органическим фосфатом концентрациях (10-3 :
- 19. Скачать презентацию






![Масс-спектр 1,2-димиристоил-sn-глицеро-3-фосфо-rac-(1-глицерин) соли аммония [M-NH4]-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1407166/slide-14.jpg)
![Масс-спектр 1,2-димиристоил-sn-глицеро-3-фосфат мононатриевой соли [M-Na]-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1407166/slide-15.jpg)

 Биогенді аминдер
Биогенді аминдер Очистка воды. Лабораторная работа в домашних условиях
Очистка воды. Лабораторная работа в домашних условиях Непрерывные реакторы для гомогенных гомофазных процессов
Непрерывные реакторы для гомогенных гомофазных процессов Магний. Нахождение в природе
Магний. Нахождение в природе Эндогенная серия. Гидротермальная группа
Эндогенная серия. Гидротермальная группа «Многоатомные спирты»
«Многоатомные спирты»  Granite
Granite Презентация по Химии "«Тверда вода»" - скачать смотреть бесплатно
Презентация по Химии "«Тверда вода»" - скачать смотреть бесплатно Лекция 6. Растворы электролитов
Лекция 6. Растворы электролитов Химическая связь
Химическая связь Научные принципы химического производства. Производство аммиака
Научные принципы химического производства. Производство аммиака Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Предмет кристаллографии. Связь с другими науками. История развития
Предмет кристаллографии. Связь с другими науками. История развития Циклоалканы. Строение циклоалканов
Циклоалканы. Строение циклоалканов Алкины
Алкины Абсорбционная осушка газа
Абсорбционная осушка газа Презентация по Химии "Жуёшь, жуёшь, не пережуёшь" - скачать смотреть
Презентация по Химии "Жуёшь, жуёшь, не пережуёшь" - скачать смотреть  Типы химических реакций на примере свойств воды Автор: учитель химии, МКОУ «Касторенская СОШ №1», п.г.т. Касторн
Типы химических реакций на примере свойств воды Автор: учитель химии, МКОУ «Касторенская СОШ №1», п.г.т. Касторн Ферменттер – тіршілік негізі
Ферменттер – тіршілік негізі Методика преподавания химии
Методика преподавания химии Презентация Дисперсные системы
Презентация Дисперсные системы  С + 6 ) ) 2 4 Подготовила: учитель химии Липадкина Г.И.
С + 6 ) ) 2 4 Подготовила: учитель химии Липадкина Г.И. МЕТАЛЛЫ Подготовила: преподаватель химии и биологии Уалихановского сельскохозяйственного колледжа Сыздыкова Карлыгаш Казбеков
МЕТАЛЛЫ Подготовила: преподаватель химии и биологии Уалихановского сельскохозяйственного колледжа Сыздыкова Карлыгаш Казбеков Презентация по Химии "Природные источники углеводородов" - скачать смотреть бесплатно
Презентация по Химии "Природные источники углеводородов" - скачать смотреть бесплатно Інсектициди для захисту сливи та персеку
Інсектициди для захисту сливи та персеку Химическая связь (Лекция 3)
Химическая связь (Лекция 3) Классификация волокон и нитей
Классификация волокон и нитей Решение задач на определение массовой (объемной) доли выхода продукта реакции от теоретически возможного
Решение задач на определение массовой (объемной) доли выхода продукта реакции от теоретически возможного