Содержание
- 2. Контрольные вопросы Учение о растворах. Роль воды и растворов в жизнедеятельности 2. Физико-химическое свойства воды 3.
- 3. Пример : Вода – это растворитель, если растворить твердое вещество (глюкозу) или газ (СО2 ). А
- 4. Концентрационный гомеостаз
- 5. Содержание и распределение воды в организме человека ~ 60 % от общей массы тела человека составляет
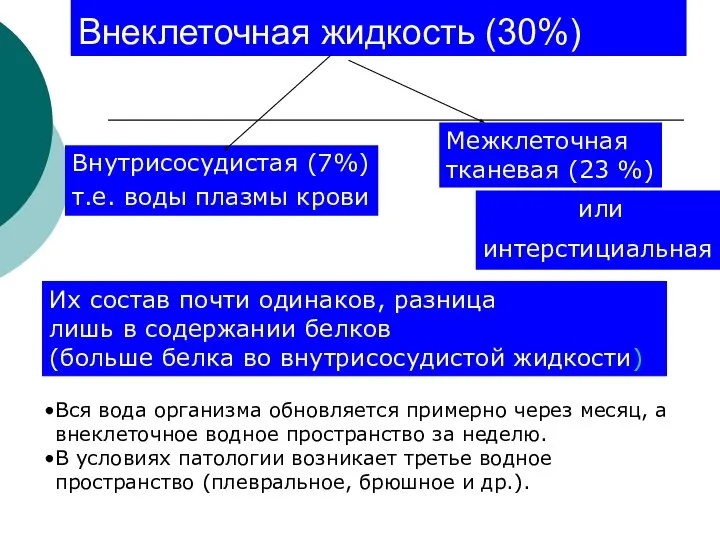
- 7. Внеклеточная жидкость (30%) Межклеточная тканевая (23 %) Внутрисосудистая (7%) т.е. воды плазмы крови или интерстициальная Их
- 8. Факторы регуляции: осмотическое, онкотическое, гидростатическое давления, проницаемость и транспорт через гистогематические барьеры, нейроэндокринная регуляция деятельности органов
- 9. В биохимических процессах вода выступает как : 1. Растворитель 2. Реагент 3. Продукт реакции 1.Вода- универсальный
- 10. 2. Вода – реагент в биохимических реакциях: кислотно-основных (автопротолиз воды) Н2О + Н2О ↔ Н3О+ +
- 11. 3. Вода- продукт биохимических реакций 57 ккал/моль 2Н2+О2? 2Н2О + Q Вывод: Н2О – универсальный растворитель,
- 12. «Вода! У тебя нет ни вкуса, ни цвета, ни запаха, тебя не опишешь, тобой наслаждаешься, не
- 13. Коллигативные свойства разбавленных растворов неэлектролитов и электролитов Свойства разбавленных растворов, зависящие только от концентрации частиц в
- 14. Осмос, осмотическое давление (πосм. Закон Вант-Гоффа Осмос – процесс односторонней диффузии растворителя сквозь полупроницаемую перегородку от
- 15. Осмотическое давление крови человека довольно постоянно и при температуре 310 К (37оС) составляет 740-780 кПа (7,4-7,8
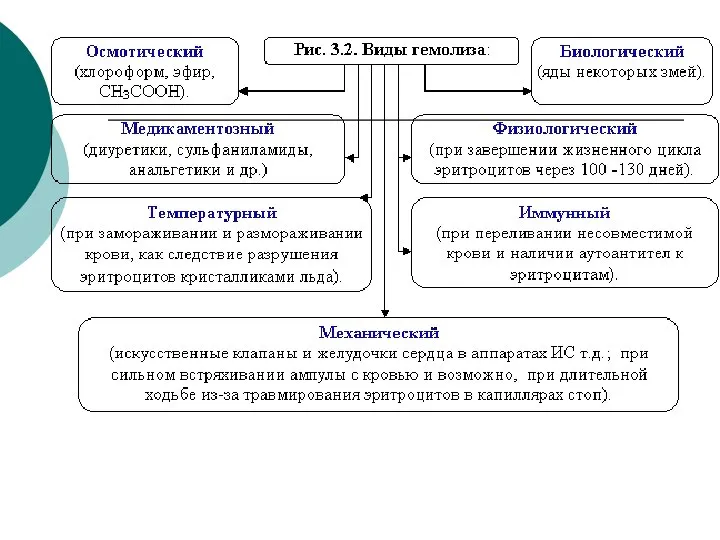
- 16. Наблюдение явлений плазмолиза и гемолиза эритроцитов (см. рисунки 3.1 и 3.2)
- 17. Плазмолиз– это сжатие и сморщивание оболочки клетки, так как в результате экзоосмоса вода диффундирует из клетки
- 18. Гемолиз – это разрыв оболочки эритроцитов и выход гемоглобина в плазму, т.к. в результате эндосмоса вода
- 19. Например, если внутривенно ввести раствор, гипотонический по отношению к крови, то наблюдается "осмотический шок" и вследствие
- 21. Онкотическое давление – это часть осмотического давление, создаваемое за счет содержания крупномолекулярных соединений (белков плазмы) в
- 22. Онкотическое давление влияет на образование тканевой жидкости, лимфы, мочи и всасывание воды в кишечнике. Поэтому кровезамещающие
- 23. Гипо–, гипер– и изотонические растворы Если два раствора различных веществ обладают одинаковым (осмотическим давлением) при одинаковой
- 24. Если раствор по сравнению с другим имеет более высокое , то его называют гипертоническим, а с
- 25. Расчетные формулы. Вант Гофф предложил эмпирическое уравнение для расчета осмотического давления разбавленных растворов Где: См –
- 26. Осмотическое давление идеального раствора равно тому давлению, которое оказывало бы растворенное вещество, если бы при данной
- 27. Поправочный (изотонический) коэффициент (i) Изотонический коэффициент показывает, во сколько раз возрастает концентрация ионов за счет диссоциации
- 28. Причем: Ассоциация молекул вещества – причина понижения значений коллигативных свойств по сравнению с вычисленными значениями
- 29. Значение его увеличивается по мере разбавления электролита, приближаясь к определенному пределу для каждого отдельного электролита. В
- 30. При вычислении степени диссоциации сильных электролитов говорят не об истинной, а о «кажущейся» степени диссоциации вещества
- 31. Степень диссоциации зависит от:
- 32. Осмолярная и осмоляльная концентрация Осмолярная концентрация раствора характеризует содержание подвижных частиц в миллиосмолях в 1 л
- 33. внутри и вне клетки одинаково, т.е. осмоляльность внутриклеточной жидкости равна осмоляльности плазмы крови. крови человека соответствует
- 34. Давление пара разбавленных растворов. Закон Рауля 2.1.Давление насыщенного пара растворителя Давление пара над раствором нелетучего вещества
- 35. Па.
- 36. - молярная доля растворенного вещества (Х), которая определяется по формуле:
- 37. Температура кипения и замерзания растворителя и раствора (II закон Рауля) Изучая кипение и замерзание растворов, Рауль
- 39. Постоянные константы и не зависят от природы растворенного вещества, а характеризуют лишь растворитель.
- 40. На измерениях температур кипения и замерзания основаны эбуллиоскопический и криоскопический методы определения молекулярных масс веществ:
- 41. Второй закон Рауля иногда называют следствием первого Ряд ученых подразделяют все закономерности, установленные Раулем на три
- 43. Скачать презентацию






































 Аттестационная работа. Мыловарение. Создание мыла своими руками
Аттестационная работа. Мыловарение. Создание мыла своими руками Современные области применения изотопной продукции
Современные области применения изотопной продукции Презентация по Химии "Исследование содержания глюкозы в различных соках" - скачать смотреть
Презентация по Химии "Исследование содержания глюкозы в различных соках" - скачать смотреть  Строение атома
Строение атома Аттестационная работа. Методическая разработка по выполнению проекта Краски из природных материалов
Аттестационная работа. Методическая разработка по выполнению проекта Краски из природных материалов Окисно-відновні реакції, процеси окиснення і відновлення, окисники і відновники
Окисно-відновні реакції, процеси окиснення і відновлення, окисники і відновники Водород- зеленое топливо
Водород- зеленое топливо Основные понятия и законы химии
Основные понятия и законы химии Дисперсные системы. Поверхностная энергия
Дисперсные системы. Поверхностная энергия Состав, строение и свойства натурального каучука
Состав, строение и свойства натурального каучука Оксиды. Номенклатура, классификация, свойства
Оксиды. Номенклатура, классификация, свойства Презентация по Химии "Химический КВН" - скачать смотреть
Презентация по Химии "Химический КВН" - скачать смотреть  Промежуточный обмен
Промежуточный обмен Химические уравнения
Химические уравнения 1.При растворении в воде гидроксид-ионы образует вещество, формула которого: 1.При растворении в воде гидроксид-ионы образует ве
1.При растворении в воде гидроксид-ионы образует вещество, формула которого: 1.При растворении в воде гидроксид-ионы образует ве Соединительная ткань. Биохимия межклеточного матрикса. (Тема 8)
Соединительная ткань. Биохимия межклеточного матрикса. (Тема 8) Серная кислота. Физические свойства
Серная кислота. Физические свойства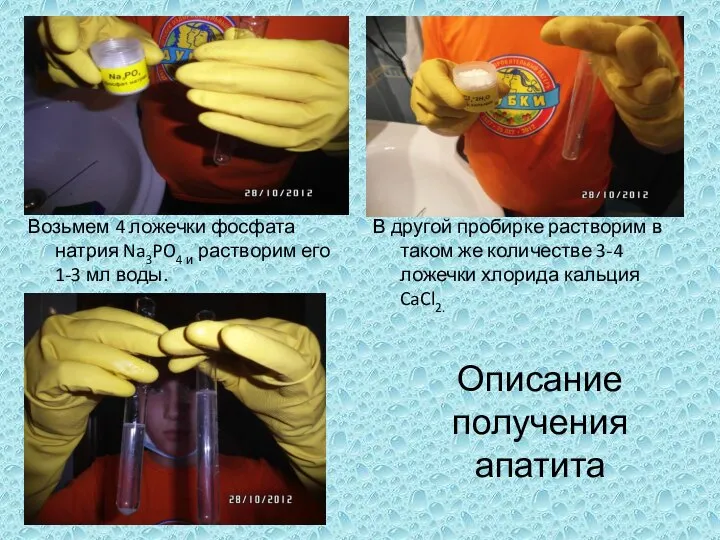 Возьмем 4 ложечки фосфата натрия Na3PO4 и растворим его 1-3 мл воды.
Возьмем 4 ложечки фосфата натрия Na3PO4 и растворим его 1-3 мл воды. Учение об агрегатных состояниях вещества. Газообразное состояние
Учение об агрегатных состояниях вещества. Газообразное состояние История одного открытия
История одного открытия  Состав краски
Состав краски Средства борьбы с вредителями растений. Инсектициды и акарициды. (Лекция 6)
Средства борьбы с вредителями растений. Инсектициды и акарициды. (Лекция 6) Валентність
Валентність  Химия и проблемы охраны окружающей среды (11 класс)
Химия и проблемы охраны окружающей среды (11 класс) Дисперсті жүйелердің оптикалық әдістері
Дисперсті жүйелердің оптикалық әдістері Реакции замещения. Электрохимический ряд напряжений.
Реакции замещения. Электрохимический ряд напряжений. Генетическая связь между классами неорганических соединений
Генетическая связь между классами неорганических соединений Алкины 10 класс - Презентация_
Алкины 10 класс - Презентация_