Содержание
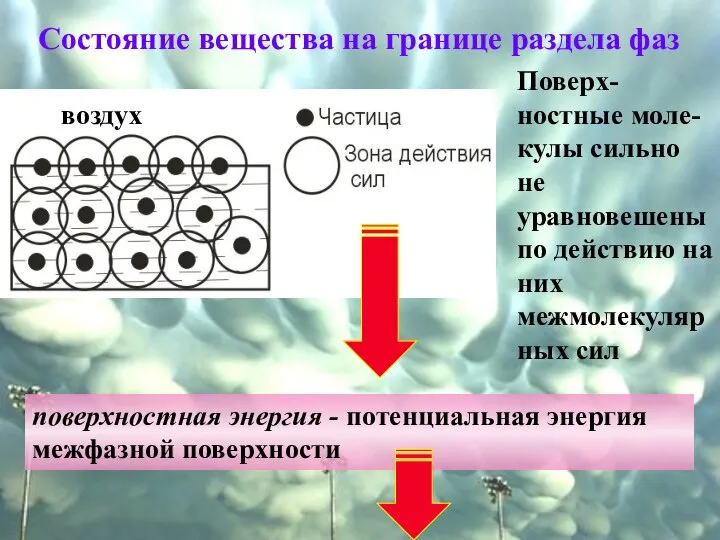
- 2. Состояние вещества на границе раздела фаз воздух Поверх- ностные моле-кулы сильно не уравновешены по действию на
- 3. ΔGпов = ΔHпов - TΔSпов = σF ΔGпов – изменение энергии Гиббса при образовании поверхности, ΔHпов
- 4. Шарообразные капли
- 5. Все самопроизвольные процессы происходят в направлении уменьшения ΔG !!! Измельчение вещества F ↑ и ΔGпов ↑
- 6. Как уменьшить ΔG? ↓F ↓σ туманы и дождевые обла-ка проливают-ся дождем, эмульсии рас-слаиваются, коллоидные ра-створы разде-ляются
- 7. Моющее действие ПАВ заключается в том, что ПАВ постепенно вытесняют с твердой поверхности жирные загрязнения, окружая
- 8. Если молекулы растворенного вещества вытесняются из поверхностного слоя внутрь раствора, то их присутствие увеличивает неуравновешенность молекул
- 9. Мыльный пузырь — тонкая пленка мыльной воды, которая формирует шар с переливчатой поверхностью.
- 10. Пленка пузыря состоит из тонкого слоя воды, заключенного между двумя слоями молекул, чаще всего мыла. Эти
- 11. Пузырь существует потому, что поверхность любой жидкости (в данном случае воды) имеет некоторое поверхностное натяжение, которое
- 12. Еще примеры действия поверхностного натяжения Скрепка на воде водомерка
- 13. Дисперсные системы – гетерогенные системы, которые образуются в результате распределения одного вещества в состоянии тонкого измельчения
- 14. вода сахар Истинный раствор– гомогенная система вода мел взвесь Гетерогенная система Необходимое условие: Взаимная нерастворимость дисперсной
- 15. Количественная характеристика дисперсности (раздробленности) вещества - степень дисперсности: D = 1/l, l – размер дисперсной частицы.
- 16. Классификация дисперсных систем по агрегатному состоянию
- 18. Система газ – твердое: дым пыль В земных условиях чаще всего - воздух Высокодисперсные аэрозоли (частицы
- 19. Дымы естественные и искуственные: Дымовые шашки CCl4 + 2Zn→ 2ZnCl2 + C → конденсация газа →
- 20. Система газ – жидкость: туман облака аэрозоль
- 21. Облака – взвешенные в атмосфере капли воды и кристаллы льда Образуются при пересыщении воздуха парами Н2О
- 22. АЭРОЗОЛИ: Малый размер частиц, развитая межфазная поверхность Высокая химическая активность Аэрозоли взрывоопасны!!! Угольная пыль, пыль сахара,
- 23. Для аэрозолей характерны особенности, связанные с газообразной дисперсионной средой: перемещение аэрозоля из области с более высокой
- 24. Система жидкое – газообразное: Пены - Самые устойчивые пены содержат ПАВ! высококонцентрированные гетерогенные системы - еще
- 25. Система жидкое – жидкое: эмульсии молоко - Эмульсия жира в воде Водоэмульсионные краски Эмульгаторы стабилизируют эмульсии
- 26. Система жидкое – твердое: Суспензии паста эмали Коллоидные растворы
- 27. Магнитная жидкость - коллоидная система однодоменных магнитных частиц (дисперсная фаза), диспергированных в жидкости (дисперсионная среда): частицы
- 28. к магнитной жидкости подносится магнит и при достаточном воздействии его поля на поверхности возникает «ёжик» Внешнее
- 29. Система твердое – газообразное: Твердые пены «воздушный» шоколад поролон кирпич пемза
- 30. Система твердое – жидкое: гели крема Жемчуг – Н2О в СаСО3
- 31. Система твердое – твердое: Минералы, цветные стекла, сплавы агаты
- 32. В высокодисперсных системах удельная поверхность и поверхностная энергия Гиббса чрезвычайно велики. Поэтому все явления в таких
- 33. Степень дисперсность влияет на все основные свойства дисперсных систем: молекулярно-кинетические, реологические, оптические, каталитические, электрокинетические:
- 34. Молекулярно-кинетические свойства дисперсных систем проявляются в явлениях: броуновское движение, диффузия, осмотическое давление, седиментация (оседание).
- 36. Самое интересное свойство – опалесценция и эффект Тиндаля: рассеяние видимого диапазона света частицами дисперсной фазы вначале
- 37. Сумеречные лучи Эффект Тиндаля в природе Окраска облаков на закате
- 38. Электрокинетические свойства коллоидных растворов обусловлены особым строением коллоидных частиц - мицелл: 1 – ядро (твердая частица,
- 39. Золь AgCl AgNO3(избыток) + HCl = AgCl↓ + H+ + NO3─ + Ag+ Потенциал образующие ионы
- 40. Гранула электрически заряжена Может направленно перемещаться в электрическом поле Электрокинетические явления: электроосмос и электрофорез Перемещение частиц
- 41. Устойчивость коллоидных систем - постоянство во времени их состояния и основных свойств. Основные факторы устойчивости: 1)
- 42. Отсутствие факторов устойчивости Коллоидные р-ры разрушаются: коагулируют и оседают (седиментация) Седиментация – оседание ч-ц дисперсной фазы
- 43. Факторы, вызывающие коагуляцию: 1) Изменение температуры; 2) механическое воздействие (интенсивное встряхивание, перемешивание); 3) действие электрических разрядов;
- 44. Методы получения дисперсных систем диспергирование конденсация Работа (энергия) на измельчение материала, равна сумме работы деформации твердого
- 45. 1. Испарение и конденсация. При сварке стали под водой в зоне сварки образуется красно-коричневое облако –
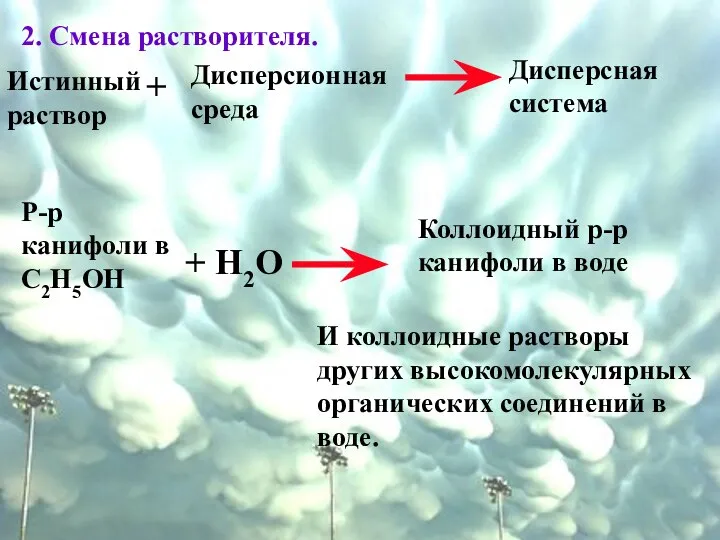
- 46. 2. Смена растворителя. Истинный раствор + Дисперсионная среда Дисперсная система Р-р канифоли в С2Н5ОН + Н2О
- 47. 3H2O + FeCl3 → Fe(OH)3↓ + 3HCl 3. Химические реакции с образованием малорастворимых в дисперсионной среде
- 48. Реакция восстановления золота: NaAuO2 + HCOH + Na2CO3 → Au↓ + HCOONa + H2O Золь красного
- 49. Нанотехнологии: в сферу этой деятельности попадают объекты с характерными размерами (хотя бы вдоль одной координаты), измеряемыми
- 50. размер наночастицы влияет на: Тпл, Т полиморфного превращения, растворимость, сдвиг химического равновесия. Характерное свойство наночастиц -
- 51. обычно Ag не реагирует с разбавленными кислотами (кроме HNO3). Однако совсем маленькие наночастицы серебра (не более
- 52. Иллюстрация Science обычный нанокластер Au субнанокластер (пикокластер) При размере наночастиц 3-5 нм реакция протекает очень резво:
- 53. Вместе с уменьшением размеров уменьшается и характерное время протекания разнообразных процессов в наносистеме, т.е. возрастает ее
- 54. Получение наночастиц. Диспергирование Методы конденсации подход «сверху»: механохими-ческое дробление, плазмохимические методы. подход «снизу»: в контролируемых условиях
- 55. Наночастицы обладают высокой поверхностной ΔG Для предотвращения обратной кристаллизации добавляют стабилизаторы (молекулярный раствор белков, полимеров или
- 56. Некоторые наночастицы могут быть стабильны сами по себе. Например, для щелочных металлов устойчивы частицы с числом
- 57. Измельчение вещества в наночастицы взрыванием металлической нити мощным импульсом тока :
- 58. Конденсационные методы: 1) Химическое восстановление. Для стабилизации наночастиц используют четвертичную соль дисульфида аммония: AgNO3 + Na[BH4]
- 59. Стабилизация наночастиц золота модифицированным декстраном (DexPNI). Декстран – природный полисахарид, часто используемый в биомедицинских целях. Его
- 60. За счет того, что наночастицы окружены макромолекулами DexPNI, они демонстрируют длительную стабильность при нагревании, высокой концентрации
- 61. Фото- и радиационно-химические восстановление: на химическую систему воздействуют либо световым излучением либо радиацией и генерируют высокоактивные
- 62. В кавитирующую жидкость опускают электроды и вызывают между ними пробой, что приводит к образованию относительно стабильной
- 63. Через колонку, заполненную пористым Al2O3 пропускают коллоидный раствор Au с размером частиц 14 нм. При этом
- 64. Трёхмерные наночастицы оксидов металлов, полученных под воздействием микроволнового излучения. Polshettiwar, Baruwati & Varma, ACS Nano, 3,
- 65. Нанокомпозит - многокомпонентный твердый материал, в котором один из компонентов в одном, двух или трех измерениях
- 67. Скачать презентацию





























































 Radiation dosimetry
Radiation dosimetry Биоэнергетика. Часть первая
Биоэнергетика. Часть первая Валентность. Порядок действий при составлении химической формулы
Валентность. Порядок действий при составлении химической формулы Липиды. Классификация липидов
Липиды. Классификация липидов Класифікація вуглеводнів. Утворення ковалентних карбон-карбонових зв’язків у органічних сполуках. Види гібридизації електро
Класифікація вуглеводнів. Утворення ковалентних карбон-карбонових зв’язків у органічних сполуках. Види гібридизації електро Кислород
Кислород Фазовые диаграммы трехкомпонентных систем
Фазовые диаграммы трехкомпонентных систем Будова атома
Будова атома Переработка гидроминерального сырья
Переработка гидроминерального сырья Процессы нитрования
Процессы нитрования Карбонові кислоти. Насичені карбонові кислоти
Карбонові кислоти. Насичені карбонові кислоти Геохимия стабильных изотопов, Радиоуглеродный метод
Геохимия стабильных изотопов, Радиоуглеродный метод Презентация Угольная кислота
Презентация Угольная кислота Дисахариды, моносахариды
Дисахариды, моносахариды «Фосфор как элемент и вещество» урок химии 9 класс Мотайло М.В. учитель химии и биологии МОУ «Головчинская СОШ с УИОП» Белгородска
«Фосфор как элемент и вещество» урок химии 9 класс Мотайло М.В. учитель химии и биологии МОУ «Головчинская СОШ с УИОП» Белгородска Атомдар мен молекулалар
Атомдар мен молекулалар Понятие электрохимии. Процессы на границе металл – раствор. Электродные потенциалы. Гальванические элементы. Уравнение Нернста
Понятие электрохимии. Процессы на границе металл – раствор. Электродные потенциалы. Гальванические элементы. Уравнение Нернста Железо
Железо Предельные углеводороды
Предельные углеводороды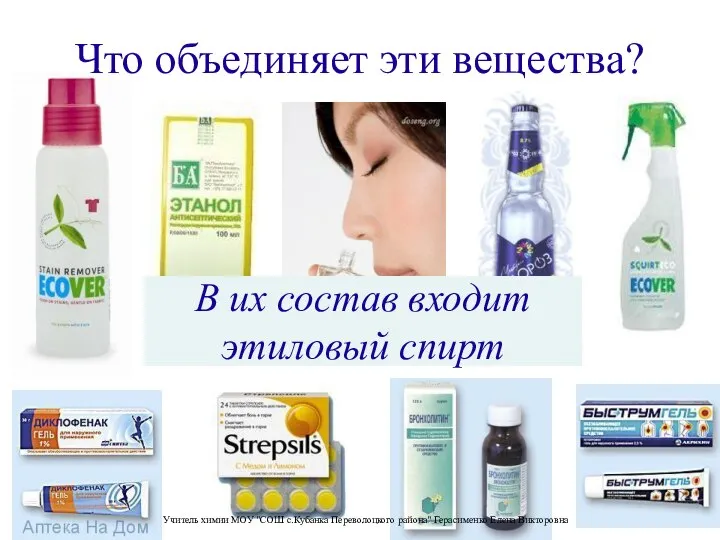 Что объединяет эти вещества?
Что объединяет эти вещества?  Презентация "Основания"
Презентация "Основания" Антибиотики. Действие антибиотиков
Антибиотики. Действие антибиотиков Важнейшие минералы
Важнейшие минералы Размерные эффекты. Причины и различные проявления размерных эффектов. Определение размерных эффектов
Размерные эффекты. Причины и различные проявления размерных эффектов. Определение размерных эффектов Хозяйственный механизм НГХК
Хозяйственный механизм НГХК Гліцерин (Гліцерол)
Гліцерин (Гліцерол) Классификация автомобильных масел
Классификация автомобильных масел Неорганические и органические основания.
Неорганические и органические основания.