Содержание
- 2. Содержание Основные понятия химии…………………………………. 3 Состав веществ. Изменение веществ………………… 8 Основные законы химии......................................... 24 Обозначения, названия
- 3. Основные понятия химии.
- 4. Химия – это наука о составе, строении, свойствах и превращениях веществ. Вещество – один из видов
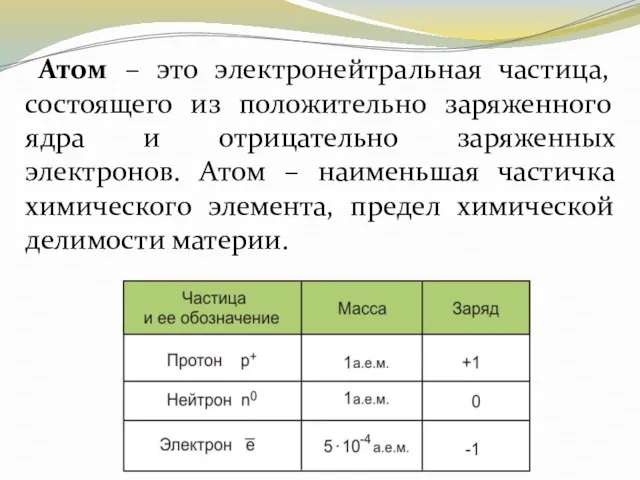
- 5. Атом – это электронейтральная частица, состоящего из положительно заряженного ядра и отрицательно заряженных электронов. Атом –
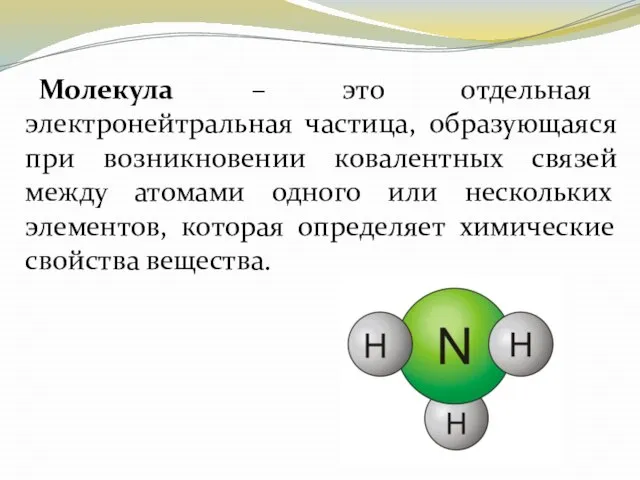
- 6. Молекула – это отдельная электронейтральная частица, образующаяся при возникновении ковалентных связей между атомами одного или нескольких
- 7. Химический элемент – это совокупность атомов с одинаковым зарядом ядра. Вещества, образованные одним химическим элементом, называют
- 8. Состав веществ. Изменение веществ.
- 9. Простые вещества – это вещества, образованные одним химическим элементом. Вещества, образованные из двух и более химических
- 10. Различают качественный и количественный состав веществ. Качественный состав – это совокупность химических элементов и (или) атомных
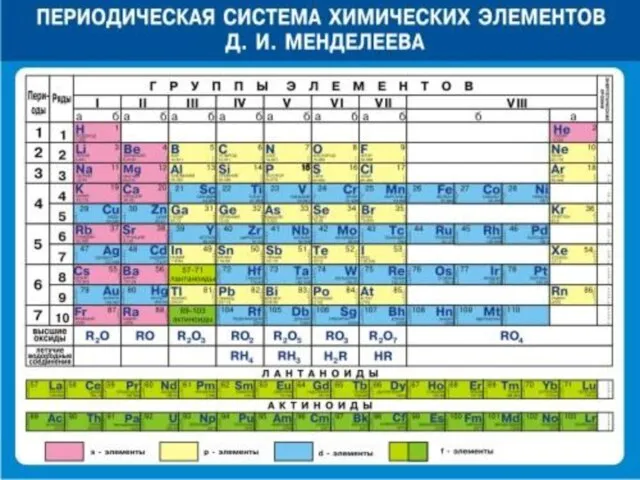
- 11. Период – горизонтальный ряд химических элементов, расположенных в порядке возрастания относительной атомной массы (Аr). Начинается каждый
- 13. Периодов семь. 1-3 - малые периоды (в них не более 8 химических элементов) 4-7 - большие
- 14. Группа - вертикальный ряд химических элементов. Групп - восемь. Содержит элементы больших и малых периодов. Ме
- 16. Химический элемент – это определённый вид атома. Каждый химический элемент обозначают собственным химическим знаком (символом).
- 17. Йёнс Якоб Берцелиус (шведский химик) предложил в качестве химического символа начальные буквы латинских названий химических элементов.
- 19. Можно выделить пять источников - этимологических начал - происхождения названий химических элементов. 1. Важнейшие свойства элементов:
- 20. 2. Мифы древних греков. тантал – любимый сын Зевса.
- 21. 3. Географические начала а) государств: германий франций рутений (Россия) полоний (Польша) б) частей света: америций, европий
- 22. 4. Астрономические начала селен (луна) теллур (земля) уран нептуний (Нептун) плутоний (Плутон)
- 23. 5. Имена великих ученых: кюрий (Кюри) энштейний (Энштейн) менделевий (Менделеев)
- 24. Выучить Неметаллы (неМе) 1. H (аш) – водород 2. O (о) – кислород 3. C (це)
- 25. Неметаллы (неМе) 8. I (иод) – иод 9. F (фтор) – фтор 10. Cl (хлор) –
- 26. Металлы (Ме). 1. Cu (купрум) – медь 2. Fe (феррум) – железо 3. Ag (аргентум) –
- 27. 8. Li (литий) – литий 9. Na (натрий) – натрий 10. K (калий) – калий 11.
- 28. Химический знак (символ) – несет значительную информацию. Он обозначает название элемента, один его атом, один моль
- 29. Химическая формула – это способ отображения химического состава вещества. Она обозначает название вещества, одну молекулу его,
- 30. Формулы вещества составляют на основании еще одного важнейшего понятия в химии – валентности. Валентность – это
- 31. Широко используются несколько видов химических формул: Простейшая (эмпирическая) формула показывает качественный состав и соотношения, в которых
- 32. Относительная атомная масса ( ) химического элемента – это величина, показывающая отношение средней массы атома природной
- 33. Относительная атомная масса – одна из основных характеристик химического элемента. Относительная молекулярная масса ( ) равна
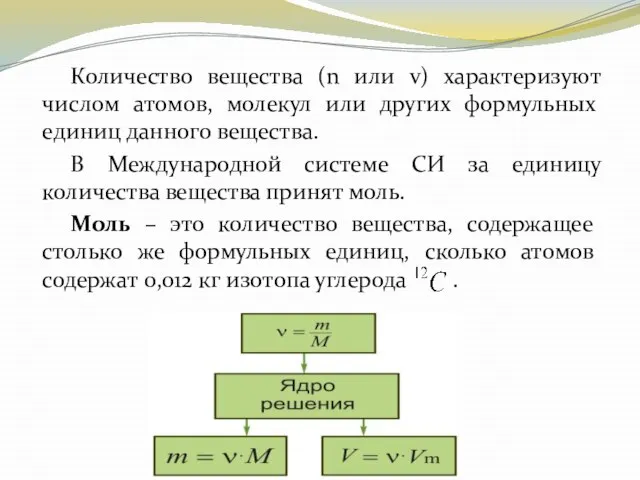
- 34. Количество вещества (n или v) характеризуют числом атомов, молекул или других формульных единиц данного вещества. В
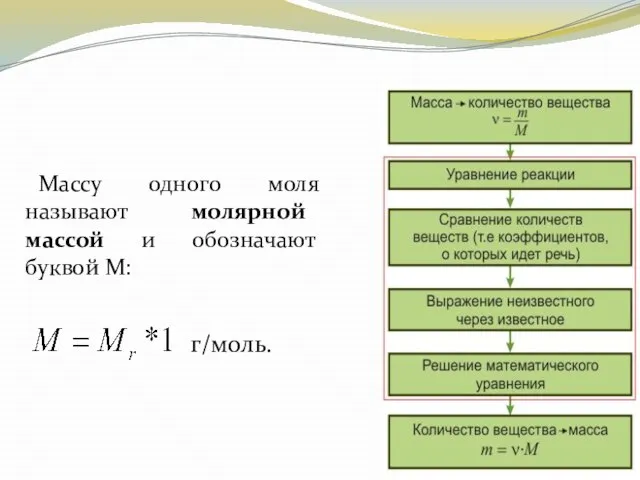
- 36. Массу одного моля называют молярной массой и обозначают буквой М:
- 38. Молярная масса может быть выражена через число молекул (или атомов) в одном моле вещества ( )
- 39. Из этого выражения можно определить число молекул или атомов, содержащихся в одном месте любого вещества, которое
- 40. Основные законы химии
- 41. Закон сохранения массы. Был открыт М. В. Ломоносовым и сформулирован А. Лавуазье: Масса веществ, вступивших в
- 42. Закон постоянства состава вещества. Сформулирован Ж.-Л. Прустом в 1799 г.: Всякое чистое вещество независимо от способа
- 43. Современная формулировка закона постоянства состава вещества такова: Состав соединений молекулярной структуры является постоянным независимо от способа
- 44. Вещества постоянного состава называют дальтонидами в честь английского физика и химика Дж. Дальтона, а вещества переменного
- 45. Закон Авогадро. Сформулирован А. Авогадро в результате проведения многочисленных экспериментов: В равных объемах различных газов при
- 46. Из закона Авогадро вытекают 2 следствия: Один моль любого газа при одинаковых условиях занимает один и
- 47. Массы двух разных газов, занимающих одинаковый объем при одинаковых условиях, относятся между собой как их молярные
- 48. Уравнение состояния идеального газа (уравнение Менделеева-Клапейрона). или где p – давление; V – объем газа; m
- 49. Основные законы химии
- 50. Найдите относительные молекулярные массы веществ, состав которых описывается формулами: Рассчитайте относительные молекулярные массы медного купороса и
- 51. Сколько молекул содержится в 32 г сернистого газа ? Какова масса молекул аммиака ? Какова масса
- 53. Скачать презентацию












































 Химия. Атомы, молекулы и ионы
Химия. Атомы, молекулы и ионы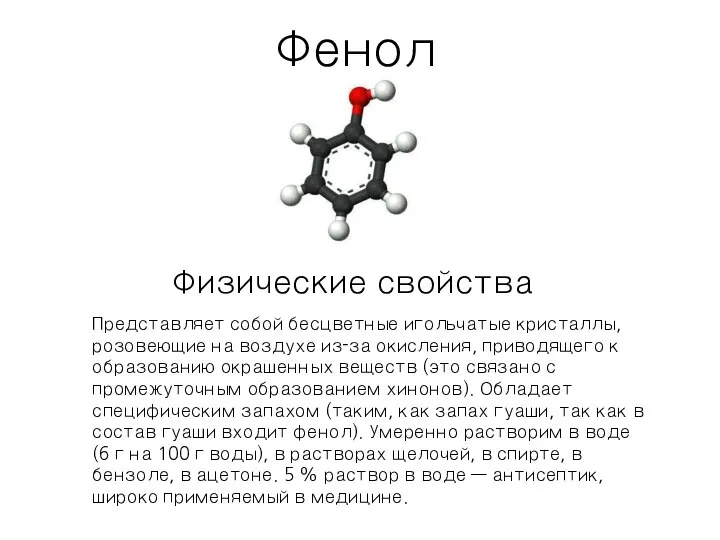 Свойства фенола
Свойства фенола Природный газ, его добыча и применение
Природный газ, его добыча и применение Биогенные р-элементы-органогены и физиологически активные галогены
Биогенные р-элементы-органогены и физиологически активные галогены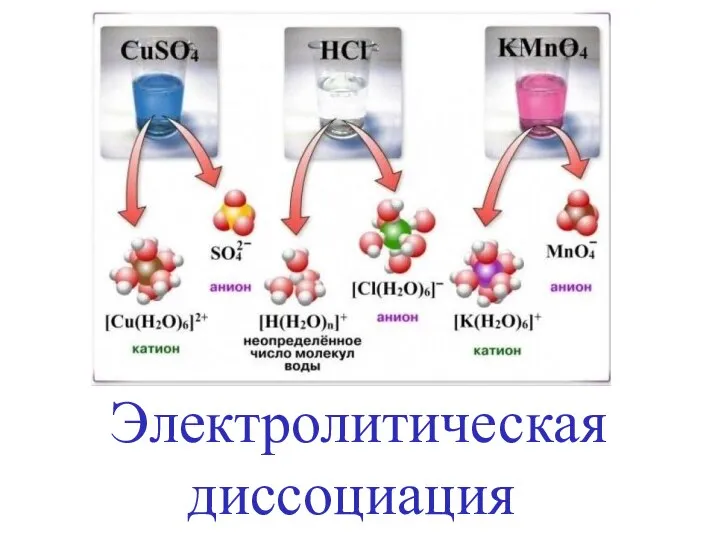 Электролитическая диссоциация
Электролитическая диссоциация Таблица взаимодействия с металлами
Таблица взаимодействия с металлами Ионообменные материалы для сорбции биологически активных веществ
Ионообменные материалы для сорбции биологически активных веществ Фосфор. Открытие фосфора
Фосфор. Открытие фосфора Лекарственные растения и сырье, содержащие алкалоиды. (Лекция 15.1)
Лекарственные растения и сырье, содержащие алкалоиды. (Лекция 15.1) Нафта Походження,переробка, використання
Нафта Походження,переробка, використання  Процессы подготовки газа к транспорту
Процессы подготовки газа к транспорту Анализ карбоновых кислот и их производных
Анализ карбоновых кислот и их производных Азот қышқылы
Азот қышқылы Газохроматографический анализ летучих ядов
Газохроматографический анализ летучих ядов Способы получения металлов
Способы получения металлов Состав раствора количественно характеризуется величинами концентраций
Состав раствора количественно характеризуется величинами концентраций Дифузія у побуті
Дифузія у побуті Методы исследования химического состава нефти и продуктов ее переработки
Методы исследования химического состава нефти и продуктов ее переработки Особенности выбора связующих и наполнителей для производства деталей машин из ПКМ
Особенности выбора связующих и наполнителей для производства деталей машин из ПКМ Химия элементов семейства Fe Co Ni
Химия элементов семейства Fe Co Ni Хімічні зв’язки Алмакаева 8-Б
Хімічні зв’язки Алмакаева 8-Б  Гетероциклдік қосылыстар
Гетероциклдік қосылыстар Расчет ректификационной колонны
Расчет ректификационной колонны Химические реакции с участием макромолекул
Химические реакции с участием макромолекул Презентация по Химии "Использование проектного метода при изучении химии" - скачать смотреть
Презентация по Химии "Использование проектного метода при изучении химии" - скачать смотреть  Презентация по Химии "Коррозия металлов" - скачать смотреть
Презентация по Химии "Коррозия металлов" - скачать смотреть  Презентация по Химии "Кругообіг Нітрогену" - скачать смотреть бесплатно
Презентация по Химии "Кругообіг Нітрогену" - скачать смотреть бесплатно Спирти. Класифікація спиртів
Спирти. Класифікація спиртів