Содержание
- 2. Химическая связь – сильное химическое взаимодействие ядерно-электронного характера, которое обеспечивает устойчивость молекулы или кристалла как единого
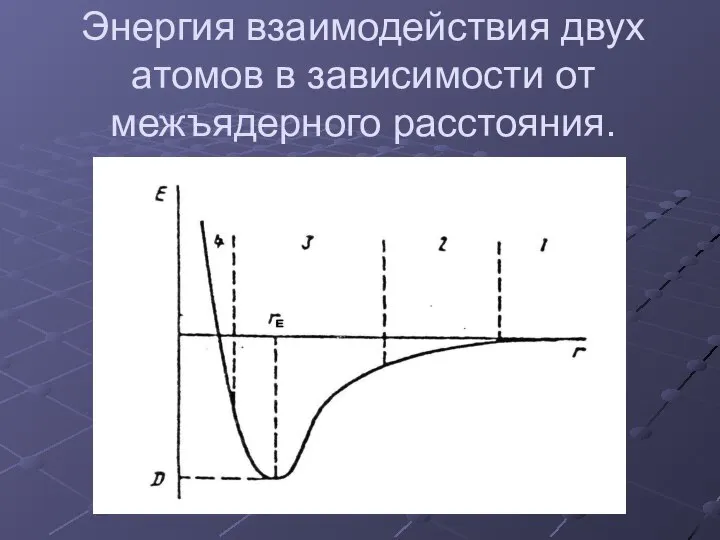
- 3. Энергия взаимодействия двух атомов в зависимости от межъядерного расстояния.
- 4. Атомы образуют химические связи в результате потери, присоединения или обобществления такого количества электронов, чтобы приобрести электронную
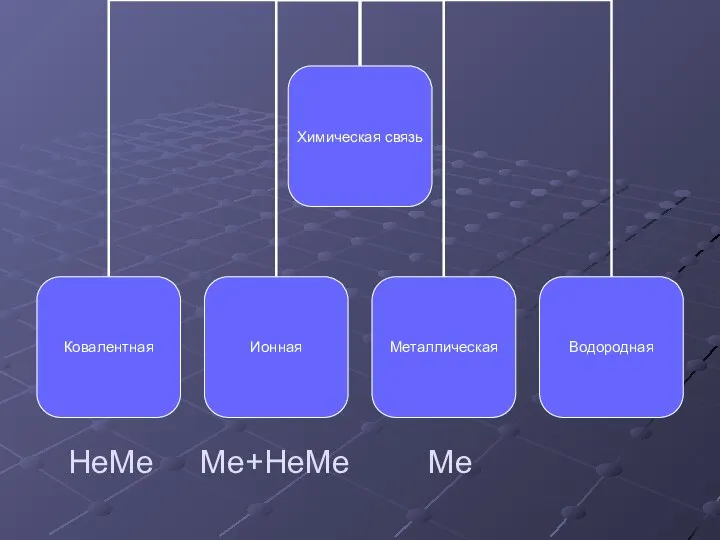
- 5. НеМе Ме+НеМе Ме
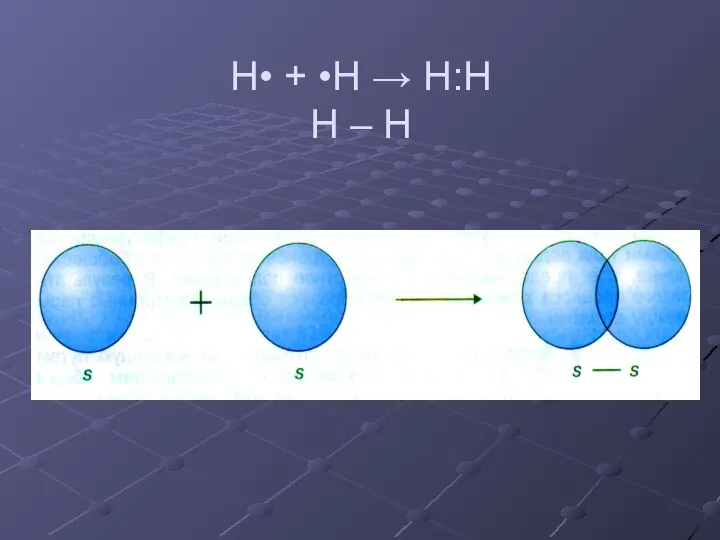
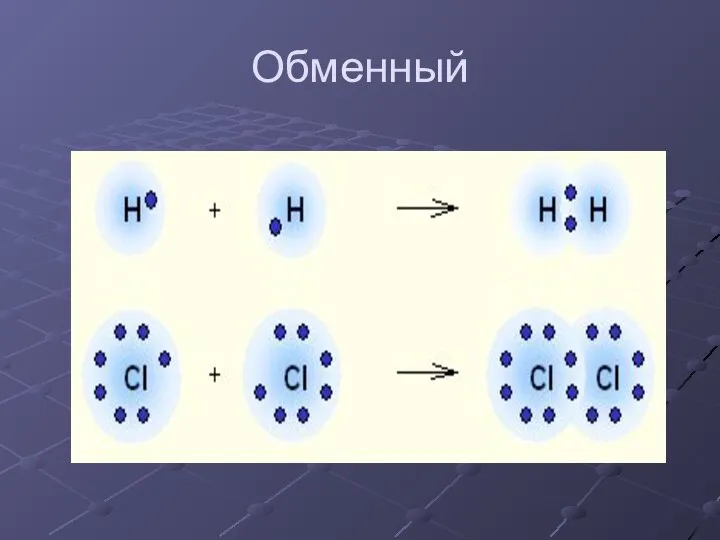
- 6. H• + •H → H:H H – H
- 7. Ковалентная связь Неполярная Атомы одного НеМе (Одинаковая ОЭО) H2;O2;Cl2;N2 Полярная Атомы разных НеМе (Различная ОЭО) HCl;CS2;NH3
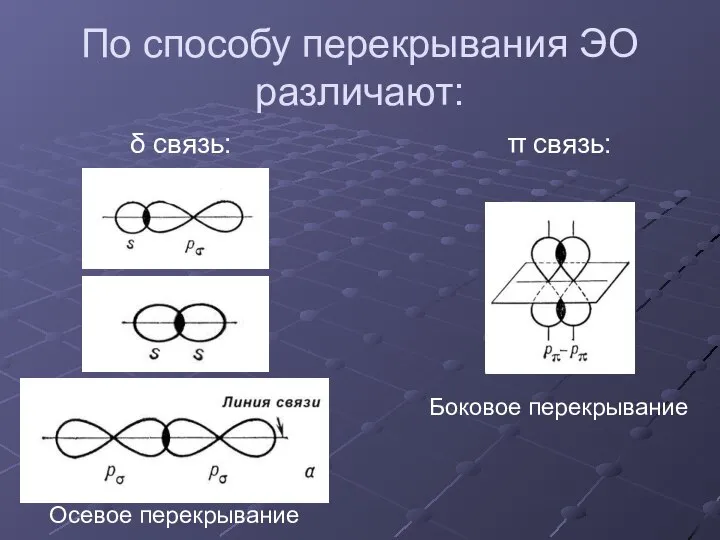
- 8. По способу перекрывания ЭО различают: δ связь: π связь: Осевое перекрывание Боковое перекрывание
- 9. Кратность связи Одинарная связь (1 общая пара электронов) Cl–Cl Двойная связь (2 общих пары электронов) O=O
- 10. Механизмы образования ковалентной связи
- 11. Обменный
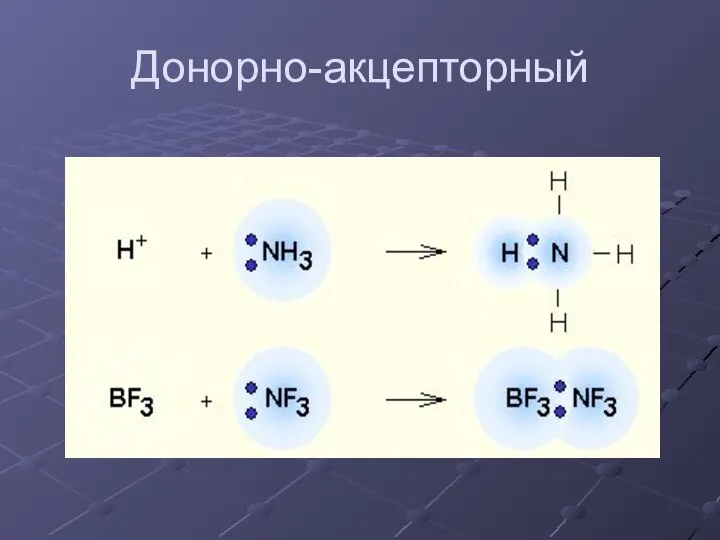
- 12. Донорно-акцепторный
- 14. Скачать презентацию





 Скорость реакции и температура. (Лекция 10)
Скорость реакции и температура. (Лекция 10) Химия биогенных элементов
Химия биогенных элементов Химические элементы в быту
Химические элементы в быту Углеводороды. Структура и функции биолекул
Углеводороды. Структура и функции биолекул Полисилоксаны. Классификация полимеров
Полисилоксаны. Классификация полимеров Методы познания химии
Методы познания химии Высокомолекулярные соединения (ВМС) или полимеры
Высокомолекулярные соединения (ВМС) или полимеры Используя оксид ртути (II) напишите уравнения реакций при которых возможны следующие превращения: Используя оксид ртути (II) напишит
Используя оксид ртути (II) напишите уравнения реакций при которых возможны следующие превращения: Используя оксид ртути (II) напишит Ювелирное дело. Империя самоцветов
Ювелирное дело. Империя самоцветов Алкандар. (қаныққан көмірсутектер. Парафиндер.)
Алкандар. (қаныққан көмірсутектер. Парафиндер.) Определение подлинности лекарственных веществ
Определение подлинности лекарственных веществ Пестициды. Применение пестицидов
Пестициды. Применение пестицидов Строение твердого вещества
Строение твердого вещества Золото. Свойство золота
Золото. Свойство золота Сверхразветвленные полимеры: типы, получение, применение
Сверхразветвленные полимеры: типы, получение, применение Арены. Бензол
Арены. Бензол В гостях у Хозяйки Медной горы. Покровская сельская библиотека
В гостях у Хозяйки Медной горы. Покровская сельская библиотека Рождающий воду
Рождающий воду Химическая связь
Химическая связь Газообразные вещества
Газообразные вещества Ртуть. Нахождение в природе. Применение
Ртуть. Нахождение в природе. Применение Изомерия комплексных соединений
Изомерия комплексных соединений Жесткость воды и способы ее устранения
Жесткость воды и способы ее устранения Вспомогательные вещества. Флюсы и их применение. Кислоты, соли, щёлочи применяемые в ювелирном деле. (Лекция 3)
Вспомогательные вещества. Флюсы и их применение. Кислоты, соли, щёлочи применяемые в ювелирном деле. (Лекция 3) Производство синтетических моющих средств
Производство синтетических моющих средств Поверхностно-активные вещества (ПАВ). Классификация ПАВ по степени влияния на окружающую среду
Поверхностно-активные вещества (ПАВ). Классификация ПАВ по степени влияния на окружающую среду Твердофазное восстановление металлов и образование карбидов из хромовых концентратов Аганозерского месторождения
Твердофазное восстановление металлов и образование карбидов из хромовых концентратов Аганозерского месторождения Простейшие операции с веществом (химический практикум)
Простейшие операции с веществом (химический практикум)