Вуглеводні. Насичені, ненасичені та ароматичні вуглеводні: їх склад, будова, фізичні та хімічні властивості
Содержание
- 2. Мета. Поглибити уявлення про гомологічні ряди вуглеводнів – алкани, алкени, алкіни, арени. Ознайомити з природою кратного
- 3. Види сполучень атомів Карбону між собою 1. Сполучення простими ковалентними зв’язками: – С – С –
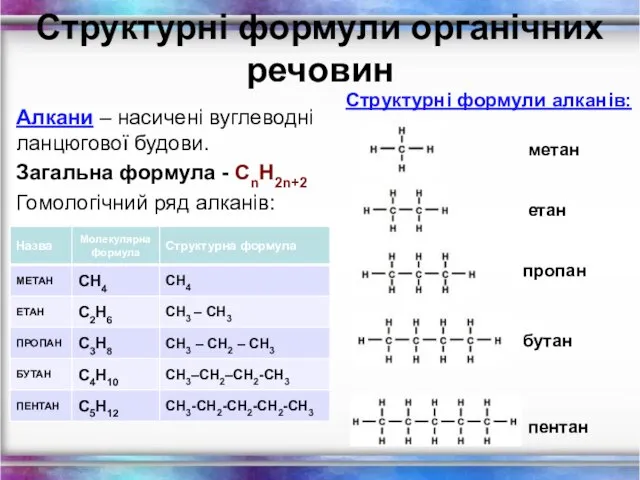
- 4. Структурні формули органічних речовин Алкани – насичені вуглеводні ланцюгової будови. Загальна формула - СnH2n+2 Гомологічний ряд
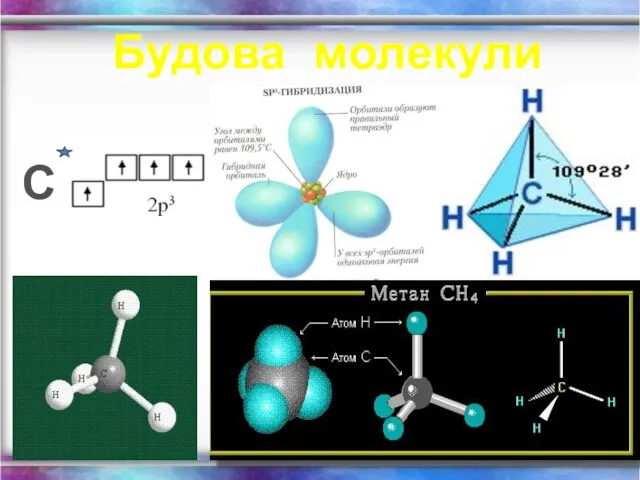
- 5. Будова молекули С
- 6. Фізичні властивості метану: Метан (СН4) - газ; без кольору; без запаху; майже не розчиняється у воді;
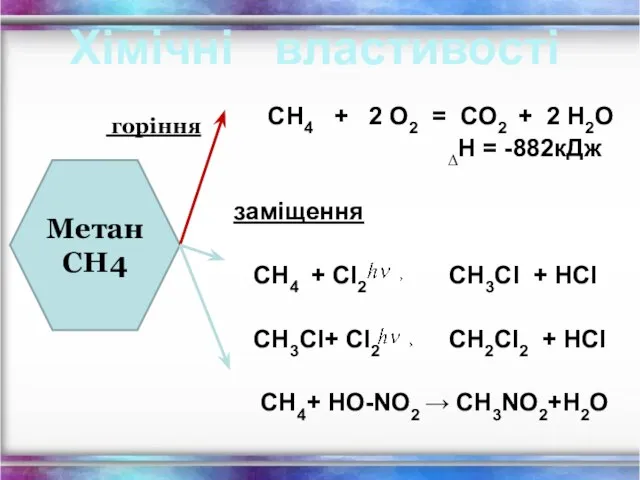
- 7. СН4 + 2 О2 = СО2 + 2 Н2О ∆Н = -882кДж заміщення СН4 + Cl2
- 8. Ненасичені вуглеводні – органічні сполуки, що мають кратні зв’язки між атомами Карбону (подвійні – С =
- 9. загальна формула кратні зв'язки тип гібридизації кут між напрямами зв'язку Алкени Алкіни CnH2n CnH2n-2 sp2 sp
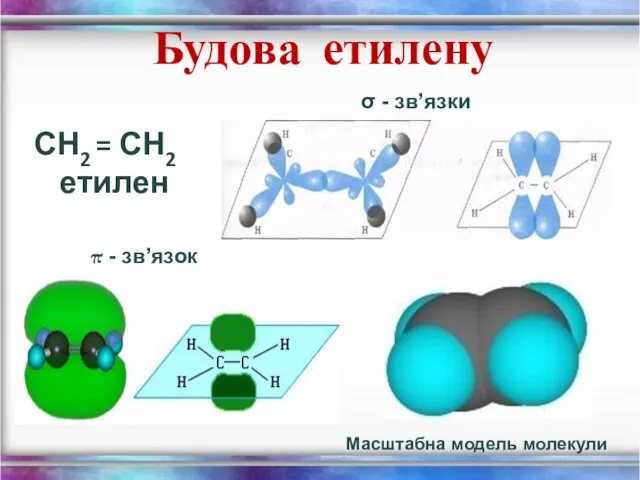
- 10. Будова етилену СН2 = СН2 етилен σ - зв’язки π - зв’язок Масштабна модель молекули
- 11. Фізичні властивості етилену С2Н4 безбарвний газ; добре розчинний в органічних розчинниках; tплавл = - 169,2 ̊С;
- 12. Хімічні властивості етилену Горіння (з виділенням великої кількості теплоти): С2Н4 + 3O2 → 2СО2 +2Н2О 2.
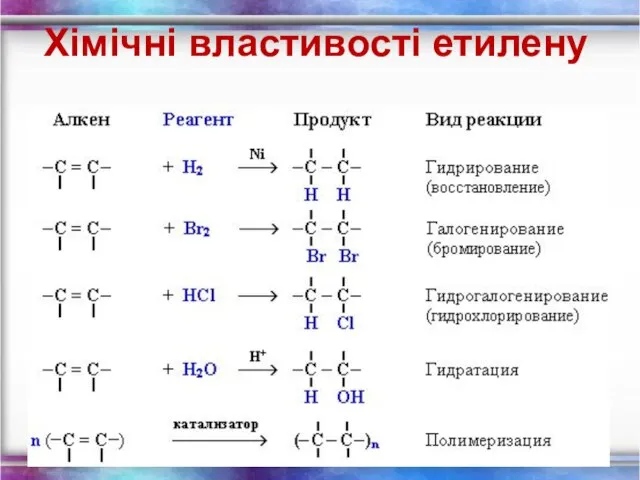
- 13. Хімічні властивості етилену
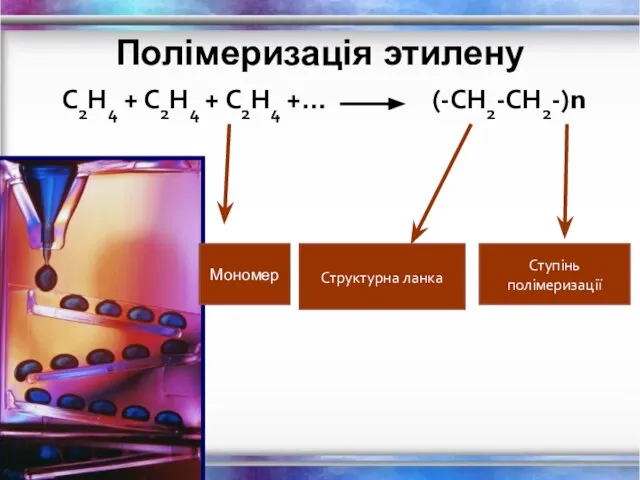
- 14. Полімеризація этилену С2Н4 + С2Н4 + С2Н4 +… (-СН2-СН2-)n Структурна ланка Ступінь полімеризації Мономер
- 15. Будова ацетилену С2Н2 СН ≡ СН Просторова будова молекули
- 16. Фізичні властивості С2Н2 безбарвний газ; майже без запаху; малорозчинний у воді, але під тиском добре розчиняється
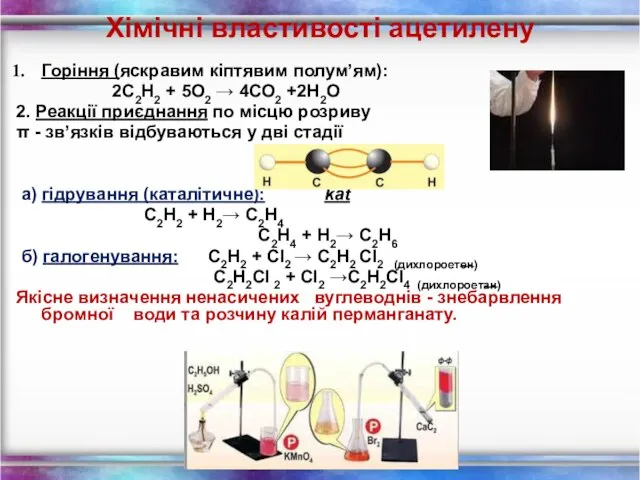
- 17. Хімічні властивості ацетилену Горіння (яскравим кіптявим полум’ям): 2С2Н2 + 5O2 → 4СО2 +2Н2О 2. Реакції приєднання
- 18. Порівняльна таблиця
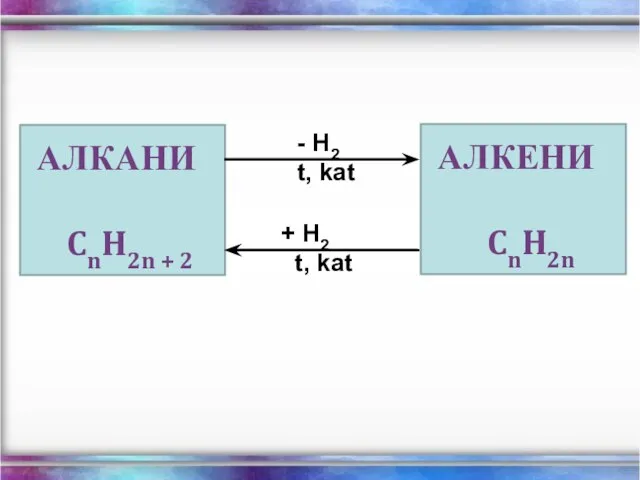
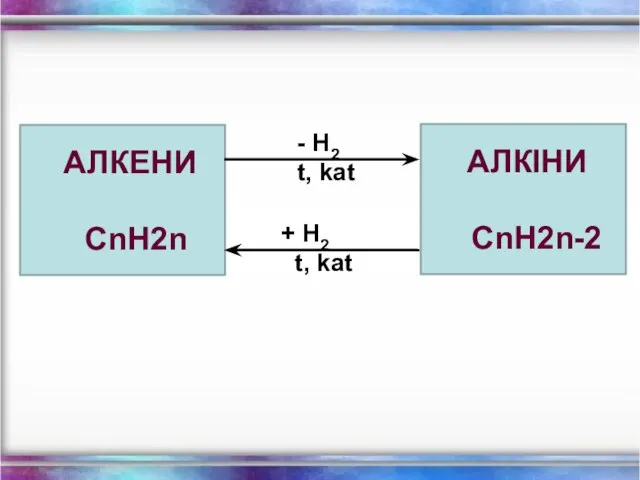
- 19. АЛКАНИ CnH2n + 2 H2 t, kat + H2 t, kat АЛКЕНИ CnH2n
- 20. АЛКЕНИ СnH2n H2 t, kat + H2 t, kat АЛКІНИ СnH2n-2
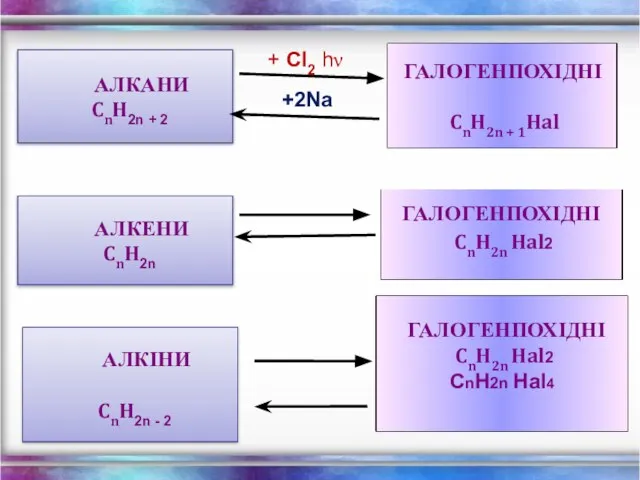
- 21. АЛКАНИ CnH2n + 2 + Cl2 hν +2Na АЛКЕНИ CnH2n АЛКІНИ CnH2n - 2
- 22. Структурна формула бензену Арени – ненасичені вуглеводні із загальною формулою CnH2n-6, молекули яких, містять бензольне кільце.
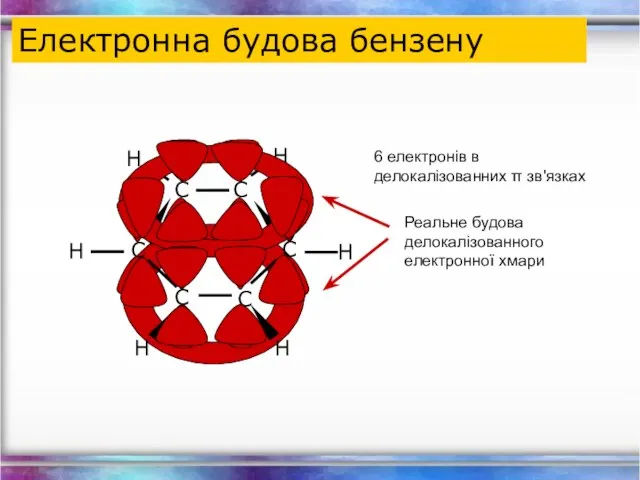
- 23. Електронна будова бензену 6 електронів в делокалізованних π зв'язках
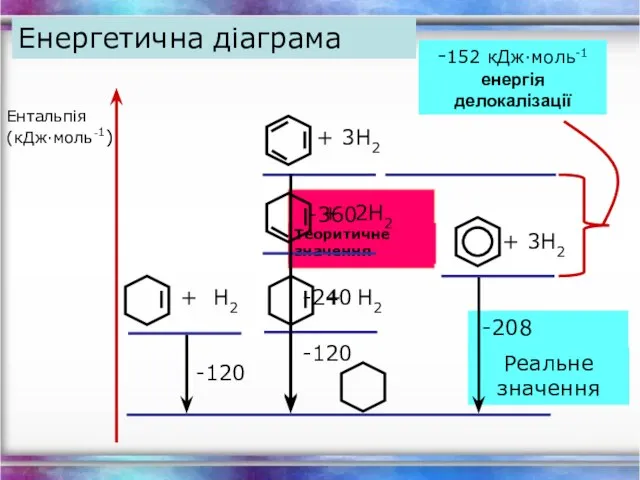
- 24. Енергетична діаграма Ентальпія (кДж∙моль-1) -120 -208 -152 кДж∙моль-1 енергія делокалізації
- 25. Гомологи бензену.
- 26. Отримання бензену. Бензен є першим представником аренів. Його можна отримати трімерізаціей ацетилену. Бензол отримують при переробці
- 27. Физические свойства бензола. Бензен: безбарвна рідина, з різким характерним запахом, легше води, розчиняється у воді, розчинний
- 28. Бензол горить. Полум'я бензолу кіптяве з-за високого вмісту карбону в молекулі. Химические свойства бензола. Через особливого
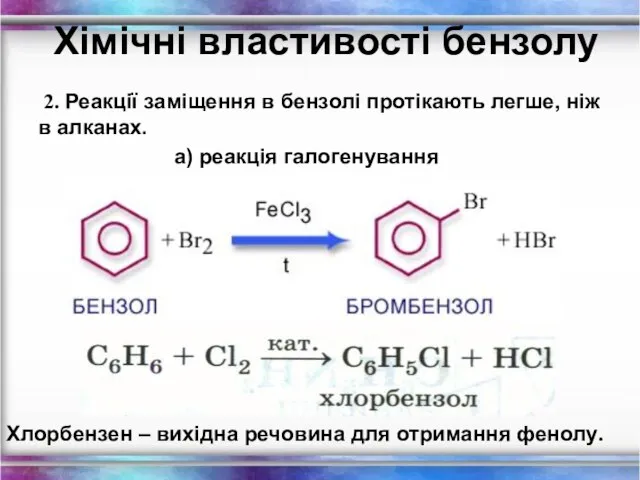
- 29. Хімічні властивості бензолу 2. Реакції заміщення в бензолі протікають легше, ніж в алканах. а) реакція галогенування
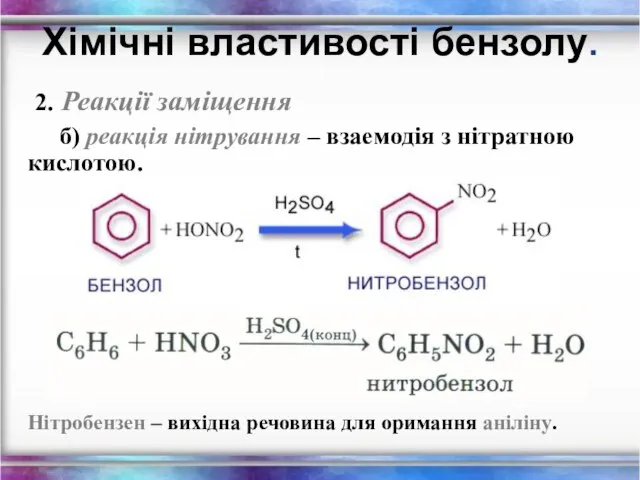
- 30. 2. Реакції заміщення б) реакція нітрування – взаемодія з нітратною кислотою. Хімічні властивості бензолу. Нітробензен –
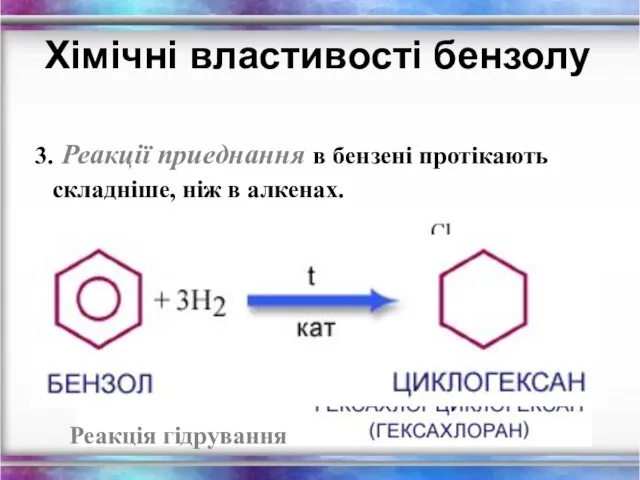
- 31. Хімічні властивості бензолу 3. Реакції приеднання в бензені протікають складніше, ніж в алкенах. Реакція гідрування
- 32. Хімічні властивості бензолу Незважаючи на високу ненасиченість молекули бензолу (за складом), він не дає характерних, якісних
- 33. Застосування бензену 1-добавка до бензину; виробництво 2-розчинників; 3-ацетону; 4-аніліну; 5-фенолу; 6-пестицидів; 7-ліків; 8-фенолформальдегідних пластмас.
- 34. ЗАВДАННЯ (І РІВЕНЬ) 1. Розподіліть по класам і назвіть речовини: а) С2Н2; б) С3Н8; в) С6Н12;
- 35. ЗАВДАННЯ (ІI РІВЕНЬ) 1. Визначіть речовини, встановіть клас сполук, складіть їх структурні формули: а) б) в)
- 36. ЗАВДАННЯ (ІII РІВЕНЬ) 1. Розподіліть по класам і назвіть речовини: а) б) С3Н8; в) г) С3Н4;
- 38. Скачать презентацию




















 Опасные химикаты
Опасные химикаты Катализаторы
Катализаторы Експерементально - дослідницький проект “Дослідження якості плавлених сирків” Підготували учасники хімічного гуртка “Безпека харчування” під керівництвом вчителя хімії та біології Караваєнко Е.Б.
Експерементально - дослідницький проект “Дослідження якості плавлених сирків” Підготували учасники хімічного гуртка “Безпека харчування” під керівництвом вчителя хімії та біології Караваєнко Е.Б. Металлы. Урок – обобщения
Металлы. Урок – обобщения Підготував Учень 10-а класу СШ№28 Прядко Андрій
Підготував Учень 10-а класу СШ№28 Прядко Андрій  Водородный показатель - рН
Водородный показатель - рН Натрий. Роль натрия в организме
Натрий. Роль натрия в организме Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Электролитическая диссоциация
Электролитическая диссоциация Минерал как химическое соединение
Минерал как химическое соединение Положение металлов в ПСХЭ Д.И. Менделеева. Общие физические свойства металлов
Положение металлов в ПСХЭ Д.И. Менделеева. Общие физические свойства металлов Презентация по Химии "кпк" - скачать смотреть бесплатно
Презентация по Химии "кпк" - скачать смотреть бесплатно Анод + Катод = Электролиз Выполнил: ученик 11М класса МОУ лицея №6 Аббязов Эрик
Анод + Катод = Электролиз Выполнил: ученик 11М класса МОУ лицея №6 Аббязов Эрик Гемоглобин. Структура и свойства молекулы гемоглобина
Гемоглобин. Структура и свойства молекулы гемоглобина Обмен липидов
Обмен липидов Химиялық реакцияның жылдамдығы. Катализ
Химиялық реакцияның жылдамдығы. Катализ Факторы, определяющие развитие отравлений
Факторы, определяющие развитие отравлений Показатель концентрации водородных ионов (лекция 6)
Показатель концентрации водородных ионов (лекция 6) Оборудование для дистилляции мисцеллы
Оборудование для дистилляции мисцеллы Химические формулы
Химические формулы Ароматичні речовини
Ароматичні речовини Ди- және полисахаридтер
Ди- және полисахаридтер Вода. Физические и химические свойства
Вода. Физические и химические свойства Фосфор и его соединения
Фосфор и его соединения Неорганические вещества клетки
Неорганические вещества клетки Презентация по Химии "ВУГЛЕВОДИ" - скачать смотреть бесплатно
Презентация по Химии "ВУГЛЕВОДИ" - скачать смотреть бесплатно Химические свойства оксидов
Химические свойства оксидов Гормоны коркового вещества надпочечников кортикостероиды
Гормоны коркового вещества надпочечников кортикостероиды