Содержание
- 2. Введение в общую химию Основные понятия химии
- 3. Структура дисциплины Общее количество часов 48 Аудиторные занятия – 10 часов В том числе практическое занятие
- 4. Содержание дисциплины Основные законы химии Химические реакции Химическая кинетика Растворы. Способы выражения концентрации растворов Метода качественного
- 5. Химия – это наука о веществах, их свойствах и превращениях, а также о явлениях, которые сопровождают
- 6. Атомно – молекулярное учение 1. Большинство известных в настоящее время веществ состоят из молекул. Молекула –
- 7. 2. Молекулы состоят из атомов. Атом – электронейтральная динамическая система, состоящая из ядра, образованного протонами и
- 9. 3. Молекулы и атомы находятся в непрерывном движении. 4. При протекании химических реакций из одних веществ
- 10. Химический элемент – совокупность атомов с одинаковым положительным зарядом ядра. Например, элемент «сера» включает атомы S,
- 11. Вещество – совокупность атомов, ионов или молекул, состоящее из одного или нескольких химических элементов.
- 12. Вещества Простые – образованы атомами одного химического элемента (O2,N2); Сложные – образованы атомами разных химических элементов
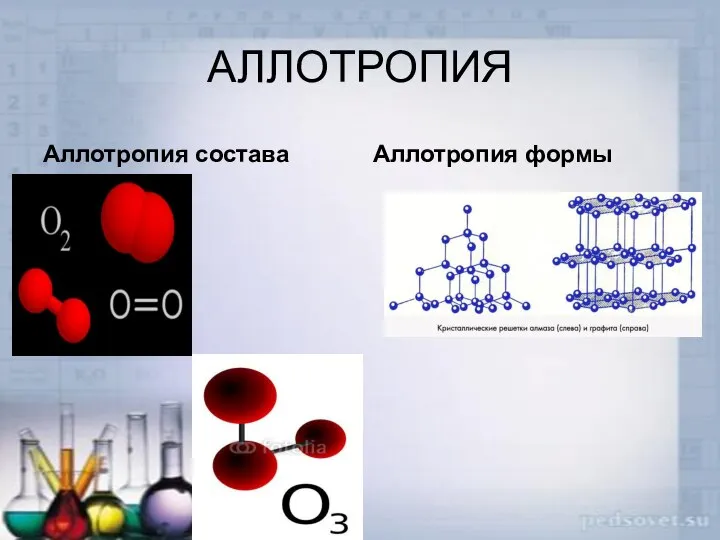
- 13. Аллотропия Существование двух и более простых веществ одного и того же химического элемента, различных по строению
- 14. АЛЛОТРОПИЯ Аллотропия состава Аллотропия формы
- 15. Относительная атомная масса (Ar) – безразмерная величина, равная отношению средней массы атома элемента к 1/12 массы
- 16. Относительная молекулярная масса (Mr) - безразмерная величина, равная отношению массы молекулы к 1/12 массы атома углерода
- 17. Например Рассчитаем относительную молекулярную массу молекулы серной кислоты: Мr (H2SO4) = 2Ar H + 1Ar S
- 18. Выполним задания Рассчитайте Mr молекулы уксусной кислоты (CH3COOH) Рассчитайте истинную массу молекулы фосфорной кислоты (H3PO4) Рассчитайте
- 19. Количество вещества. Моль. Молярная масса Моль – единица количества вещества. Моль – это количество вещества, содержащее
- 20. 1 моль любого вещества содержит 6,02*1023 структурных единиц 6,02*1023 - ПОСТОЯННАЯ АВОГАДРО (NA) Размерность моль -1
- 21. Масса одного моля вещества (молярная масса М), выраженная в граммах, численно равна относительной молекулярной массе. Единица
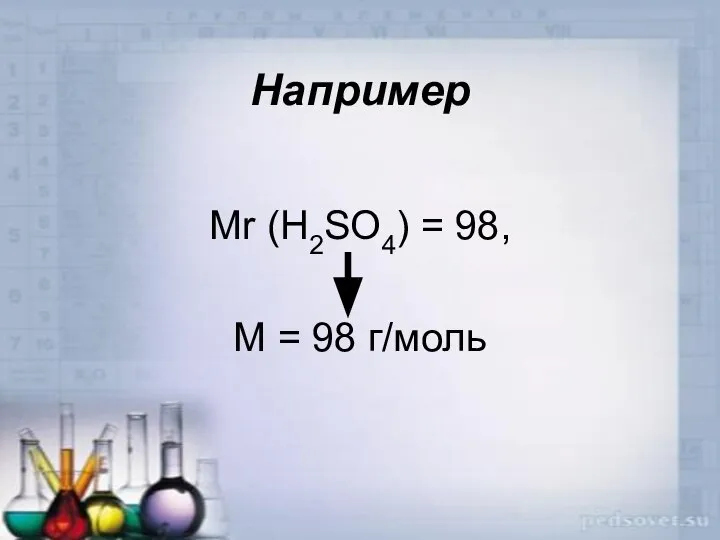
- 22. Например Mr (H2SO4) = 98, М = 98 г/моль
- 23. Количество вещества (n) n = N/NA где N – общее число структурных единиц, NA – число
- 24. Решим задачи Вычислите количество вещества цинка в образце массой 2,6 г. Вычислите количество вещества магния в
- 25. Вычислите количество вещества цинка в образце массой 2,6 г. Дано: m (Zn) = 2,6г Решение: Записываем
- 26. Рассчитайте число молекул Br2 в броме массой 6,4г. Дано: M (Br2) = 6,4г N = ?
- 27. Химическая формула – условная запись состава вещества с помощью химических знаков и индексов Химическая формула показывает
- 29. Скачать презентацию
























 Водород в космосе
Водород в космосе Структурная организация биополимеров. ДНК и РНК
Структурная организация биополимеров. ДНК и РНК Презентация по Химии "Кто хочет стать отличником" - скачать смотреть
Презентация по Химии "Кто хочет стать отличником" - скачать смотреть  Электрохимические процессы
Электрохимические процессы Витамины и авитаминоз - презентация_
Витамины и авитаминоз - презентация_ Презентация по Химии "Пероксид водорода" - скачать смотреть
Презентация по Химии "Пероксид водорода" - скачать смотреть  Кислоты. (8 класс.)
Кислоты. (8 класс.) Теоретическая электрохимия, часть 1
Теоретическая электрохимия, часть 1 Композиционные материалы
Композиционные материалы Технология адсорбционной осушки газа
Технология адсорбционной осушки газа Русские ученые-химики
Русские ученые-химики Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Лекарственное растительное сырье, содержащее производные антрацена
Лекарственное растительное сырье, содержащее производные антрацена Органические вещества
Органические вещества Основания как электролиты
Основания как электролиты 8 класс
8 класс  Алканы. Свойства. Строение и применение
Алканы. Свойства. Строение и применение Неорганические вещества
Неорганические вещества Углеводы. Общая характеристика углеводов
Углеводы. Общая характеристика углеводов Kristālisku vielu uzbūve
Kristālisku vielu uzbūve Симметрия в химии. Кристаллы
Симметрия в химии. Кристаллы Аттестационная работа. Образовательная программа элективного курса по химии
Аттестационная работа. Образовательная программа элективного курса по химии Минерал клинохлор. Месторождения
Минерал клинохлор. Месторождения Полимеры. Пластмассы. Волокна. Цели: - узнать что такое пластмассы, волокна их отличие от полимеров; - изучить классификацию пл
Полимеры. Пластмассы. Волокна. Цели: - узнать что такое пластмассы, волокна их отличие от полимеров; - изучить классификацию пл Липиды - жиры и жироподобные органические соединения, практически нерастворимые в воде
Липиды - жиры и жироподобные органические соединения, практически нерастворимые в воде Металлы; их классификация, строения и свойства
Металлы; их классификация, строения и свойства Геолого-промышленные типы месторождений полезных ископаемых
Геолого-промышленные типы месторождений полезных ископаемых Количество вещества
Количество вещества