Содержание
- 2. Азот «открывали» несколько раз и разные люди. Его называли по-разному, приписывая едва ли не мистические свойства
- 3. Символ элемента: N. Порядковый номер: 7. Положение в таблице: 2-й период, группа - VA Химический элемент
- 4. Азот - нетоксичный газ, без цвета, без вкуса, без запаха, слабый проводник тепла и электричества.
- 5. Испаряясь, азот охлаждает очаг возгорания и вытесняет кислород, необходимый для горения, поэтому пожар прекращается. Так как
- 6. Жидкий азот способен при определенной температуре и под воздействием соответствующего давления преобразовываться в кристаллическое твердое вещество.
- 7. В лаборатории азот легко может быть получен при нагревании концентрированного нитрита аммония: NH4NO2= N2 + 2H2O.
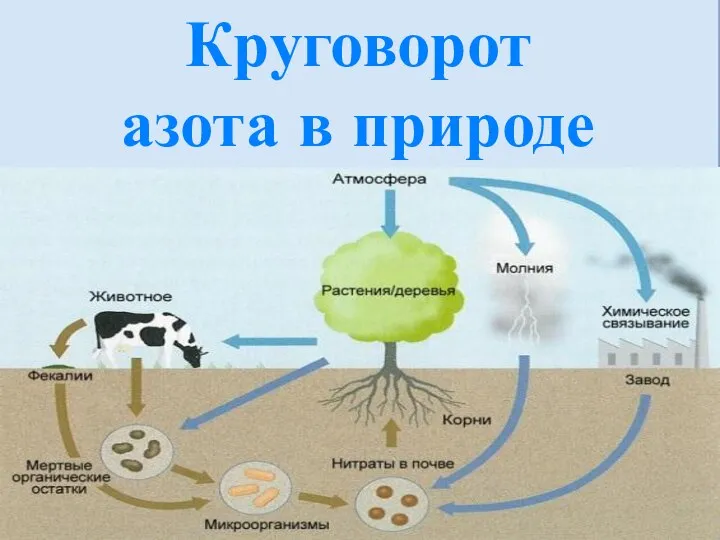
- 9. Круговорот азота в природе
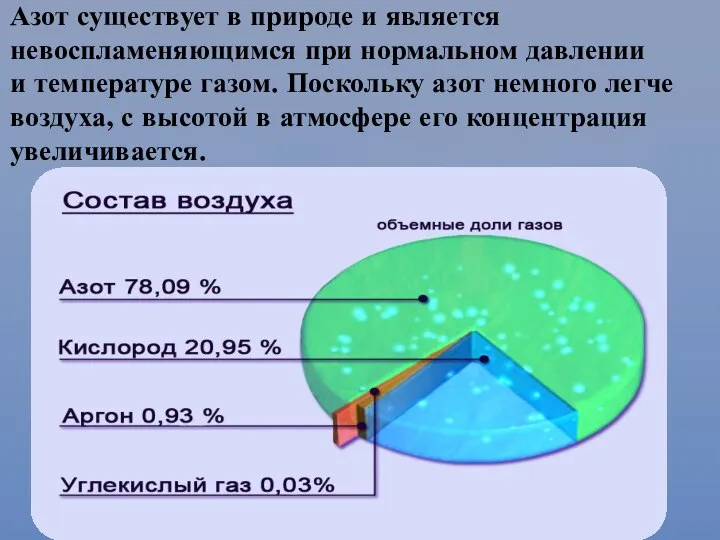
- 10. Азот существует в природе и является невоспламеняющимся при нормальном давлении и температуре газом. Поскольку азот немного
- 11. Нитраты являются необходимой частью азотного питания растений, без которых невозможны сложные биологические процессы синтеза белка. Нитраты
- 12. ОКСИДЫ АЗОТА
- 14. Оксид азота(II) - NO Физические свойства. Бесцветный газ, при низких температурах - голубая жидкость. В твердом
- 15. Химические свойства. Очень реакционноспособное вещество. Может проявлять и окислительные и восстановительные свойства. 1.При обычной температуре окисляется
- 17. Физические свойства. Это красно-бурый газ с резким запахом. При низких температурах из-за наличия у атомов азота
- 18. Химические свойства. Взаимодействие с водой: 2NO2 + H2O(хол) = HNO3 + HNO2 3NO2 + H2O(гор) =
- 20. Физические свойства. Бесцветный газ с тошнотворным cладковатым запахом, обладает анестезирующим действием. Растворим в воде. t0(плав) =
- 22. Физические свойства. Это синяя жидкость при обычных условиях. В твердом состоянии - белое или голубоватое вещество.
- 24. Оксид азота(V) - азотный ангидрид N2O5 Строение. Физические свойства. Белое кристаллическое вещество, летучее, неустойчивое. При нагревании
- 25. Химические свойства. Оксид азота(V) - кислотный оксид. 1. При растворении в воде образует азотную кислоту: N2O5
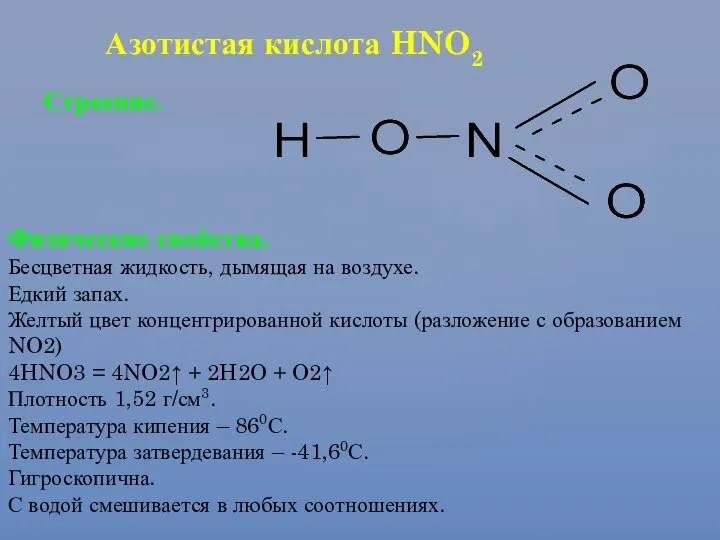
- 26. Азотистая кислота HNO2 Строение. Физические свойства. Бесцветная жидкость, дымящая на воздухе. Едкий запах. Желтый цвет концентрированной
- 27. Химические свойства. Разбавленная азотная кислота проявляет свойства, общие для всех кислот: Диссоциациация в водном растворе: HNO3
- 28. Специфические свойства – взаимодействие с металлами ЗАПОМНИ! При взаимодействии азотной кислоты любой концентрации с металлами водород
- 29. С овощами и фруктами в организм человека поступают до 70 – 80% нитратов. Сами по себе
- 30. Пути попадания нитратов в организм человека: - Основная масса нитратов попадает в организм человека с консервированными
- 32. Скачать презентацию


























 Понятие «Эффективность». Принцип Ле-Шателье
Понятие «Эффективность». Принцип Ле-Шателье Выращивание кристаллов
Выращивание кристаллов Волшебные кристалы
Волшебные кристалы Алкены
Алкены Монокристаллы InSb. Свойства, выращивание, применение
Монокристаллы InSb. Свойства, выращивание, применение Презентация по Химии "Органическая химия" - скачать смотреть
Презентация по Химии "Органическая химия" - скачать смотреть  Зависимость знака заряда белка от pH
Зависимость знака заряда белка от pH Классификация основных пород
Классификация основных пород Искусственные и трансурановые элементы
Искусственные и трансурановые элементы Жири як компоненти їжі. Їхня роль в організмі
Жири як компоненти їжі. Їхня роль в організмі  Бензол қатарының гетерофункционалды туындылары дәрілік заттар ретінде
Бензол қатарының гетерофункционалды туындылары дәрілік заттар ретінде Электролитическая диссоциация. 9 класс
Электролитическая диссоциация. 9 класс Аттестационная работа. Выращивание кристаллов. Выявить условия, позволяющие из раствора медного купороса выращивать кристаллы
Аттестационная работа. Выращивание кристаллов. Выявить условия, позволяющие из раствора медного купороса выращивать кристаллы Регуляция и патология липидного обмена
Регуляция и патология липидного обмена Жиры в питании спортсмена
Жиры в питании спортсмена Оже спектроскопия
Оже спектроскопия Legătura chimică
Legătura chimică Энтропия и уравнение состояния идеального газа
Энтропия и уравнение состояния идеального газа Стандартизація лікарської рослинної сировини
Стандартизація лікарської рослинної сировини Презентация по Химии "Металлы. Общая характеристика металлов (нахождение в природе и физические свойства)" - скачать смотреть
Презентация по Химии "Металлы. Общая характеристика металлов (нахождение в природе и физические свойства)" - скачать смотреть  Булану мен конденсация
Булану мен конденсация Презентация по Химии "Молекула в расчетных методах" - скачать смотреть
Презентация по Химии "Молекула в расчетных методах" - скачать смотреть  Материаловедение. Основы металловедения
Материаловедение. Основы металловедения ТЕМА УРОКА:
ТЕМА УРОКА: Классификация металлов
Классификация металлов Роль ученых в становлении органической химии
Роль ученых в становлении органической химии Дорогие и дешёвые лекарства: «Чем похожи и чем отличаются друг от друга?
Дорогие и дешёвые лекарства: «Чем похожи и чем отличаются друг от друга? Химия атмосферы
Химия атмосферы