Содержание
- 2. Биосфера. Круговорот биогенных элементов Раздел геохимии, изучающий химические процессы в земной коре с участием живых организмов,
- 3. Согласно В.И. Вернадскому, живые организмы принимают активное участие в перераспределении химических элементов в земной коре. В.И.
- 4. Осадочные горные породы
- 5. Меловые отложения
- 6. железо отлагается с помощью железобактерий и образует залежи лимонита
- 7. В живых организмах, в том числе и у человека можно обнаружить те же элементы, которые есть
- 8. Среднее содержание элементов в живых организмах, земной коре, атмосфере, гидросфере, в атмосфере Солнца и звезд выражается
- 9. Увеличение содержания элемента в организме по сравнению с окружающей средой называют биологическим концентрированием
- 10. Биогенными элементами называют элементы, необходимые для построения и жизнедеятельности различных клеток организма.
- 11. Из 92 встречающихся в природе элементов 81 обнаружен в организме человека. При этом 15 из них
- 12. Классификация биогенных элементов Биотики-элементы экзогенного происхождения, имеющие способность: - входить в состав структур организма; - участвовать
- 13. Классификация биогенных элементов по их функциональной роли Органогены Элементы электролитного фона Микроэлементы Ксенобиотики
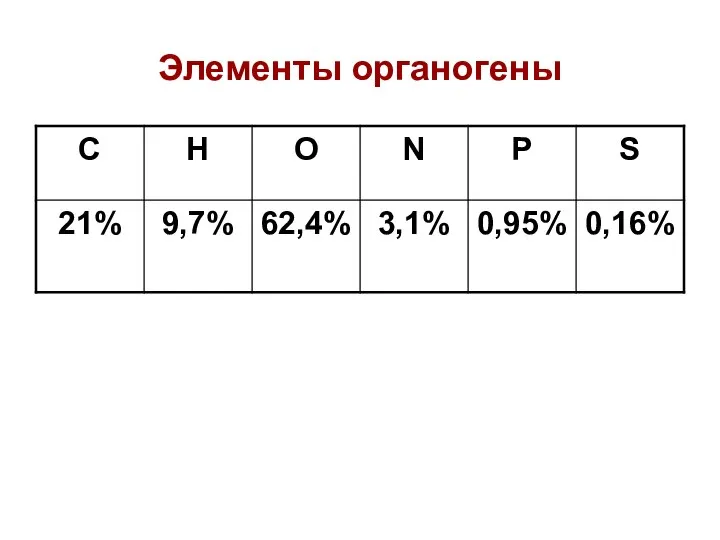
- 14. Элементы органогены
- 15. Элементы электролитного фона Na, К, Ca, Mg, Сl ионы данных металлов составляют 99% общего содержания металлов
- 16. Металлы жизни K, Na, Ca, Mg, Mn, Fe, Co, Cu, Zn, Mo
- 17. Микроэлементы I, Cu, F, Br, Ba, Co Fe, Mn, Zn,Mo входят в состав ферментов, витаминов, гормонов
- 18. Ксенобиотики (от греч. xenos - чужой и bios - жизнь), чужеродные для организмов соединения: промышленные загрязнения,
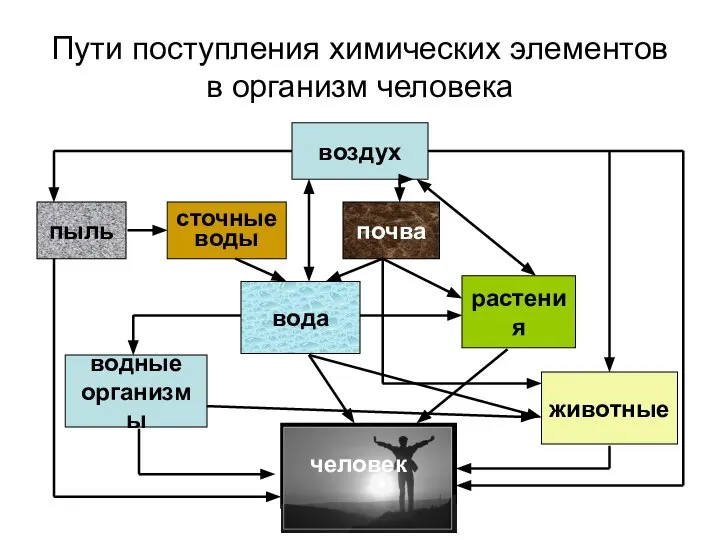
- 19. Пути поступления химических элементов в организм человека воздух водные организмы растения вода почва пыль сточные воды
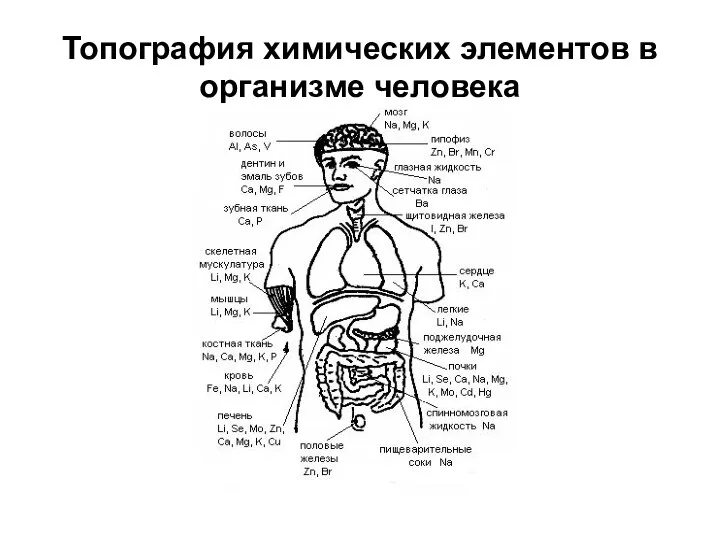
- 20. Топография химических элементов в организме человека
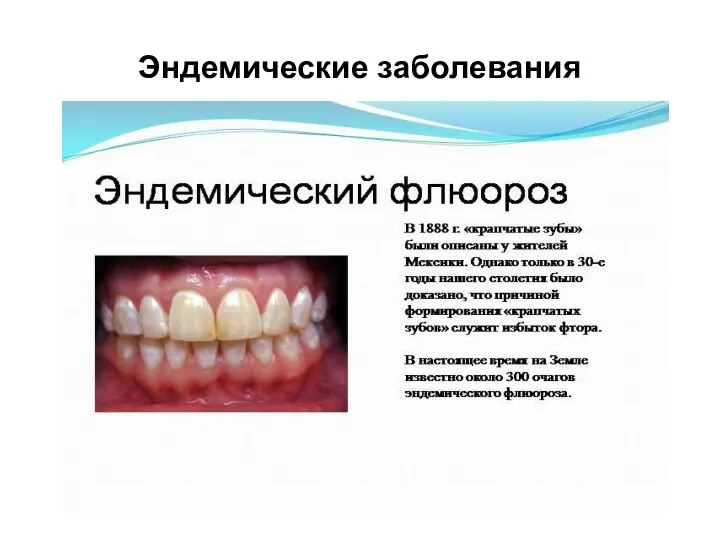
- 21. Эндемические заболевания
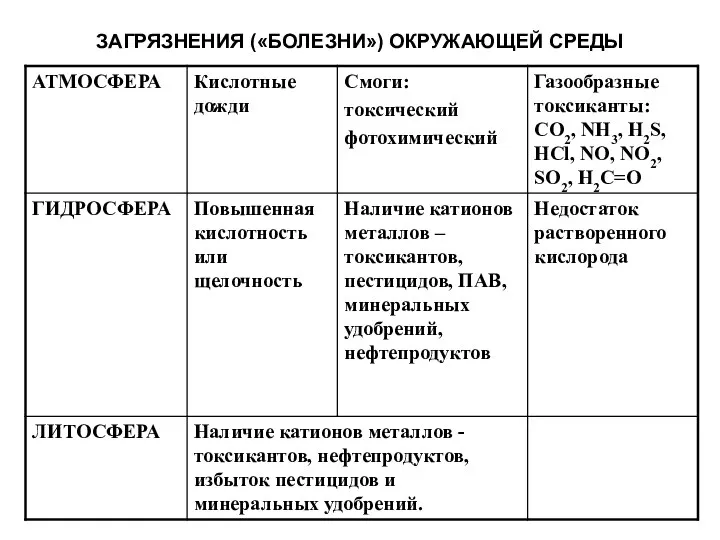
- 23. ЗАГРЯЗНЕНИЯ («БОЛЕЗНИ») ОКРУЖАЮЩЕЙ СРЕДЫ
- 24. ЛИТЕРАТУРА ДЛЯ САМОСТОЯТЕЛЬНОГО ИЗУЧЕНИЯ 1.Барковский Е.В. Введение в химию биогенных элементов. стр. 38-43, 2. Ершов Ю.А.
- 25. Составить характеристику элементов С, О, Н, N, P, S, K, Na, Ca, Mg, Mn, Fe, Cu,
- 27. ХИМИЯ ЭЛЕМЕНТОВ ПЛАН ЛЕКЦИИ (ч.2) Общая характеристика s – элементов Общая характеристика d – элементов Общая
- 28. Периодическая система химических элементов
- 29. s-элементы Конфигурация валентного уровня: ns1; ns2 Характерные степени окисления: +1; +2 Сильные восстановители Образуют соединения с
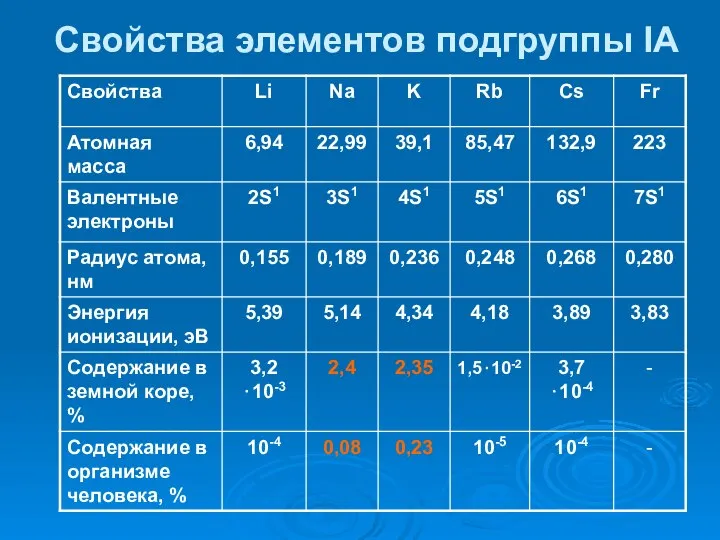
- 30. Свойства элементов подгруппы IA
- 31. Свойства элементов подгруппы IIA
- 32. Кислотно-основные свойства Кислотные свойства не проявляются, основные свойства в пределах подгруппы сверху вниз увеличиваются. Образуют гидроксиды
- 33. Комплексы s-элементов Кристаллогидраты Бура - Na2B4O7⋅10H2O, Квасцы - KAl(SO4)2⋅12H2O В водных растворах - [Mg(NH3)4]Cl2 – хлоридтетрааммин
- 34. Образование нерастворимых соединений Все соли s-элементов 1А группы растворимы. При переходе к s-элементам 2А группы растворимость
- 35. При отравлении солями бария применяют нетоксичные растворимые соли серной кислоты: BaCl2 + Na2SO4 = BaSO4↓+NaCl BaCl2
- 36. Водород символ - H расположен в 1 группе, главной п/г, первого перида ПС, порядковый № 1,
- 37. Химические свойства При нагревании реагирует с кислородом, серой, хлором и др. 2H2+O2 = 2H2O H2+Cl2 =
- 38. Нерастворимые соединения Входит в состав некоторых малорастворимых кислых солей: CaHPO4, Ca(H2PO4), нерастворимых кислот SnO2·xH2O (x=1-2), H3SbO4.
- 39. d-элементы Конфигурация валентного уровня: (n-1)dansb; n- номер уровня, а=1-10, b=1-2 Проявляют переменную степень окисления Могут быть
- 40. d – металлы являются активными комплексообразователями. Основными биолигандами являются белки, содержащие,как правило, мягкие центры: группы –SH,
- 41. Нерастворимые соединения Катионы d – элементов образуют много нерастворимых соединений (сульфиды, карбонаты, фосфаты, оксалаты, цианиды). Образование
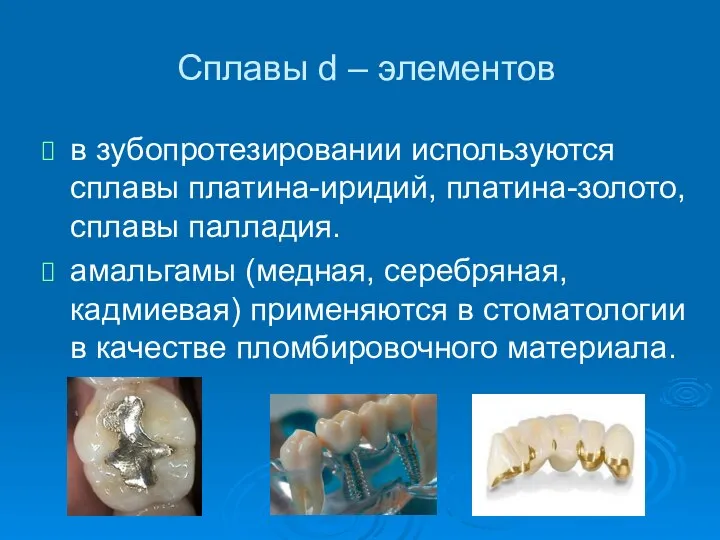
- 42. Сплавы d – элементов в зубопротезировании используются сплавы платина-иридий, платина-золото, сплавы палладия. амальгамы (медная, серебряная, кадмиевая)
- 43. Иридий в сплаве с платиной используется для изготовления электрических стимуляторов сердца.
- 44. цинк символ - Zn расположен во второй группе побочной п/г, четвертого периода, порядковый № 30, атомная
- 45. Химические свойства Металл, синевато-белый, твердый, образует сплавы, например, с медью – латунь. Цинк взаимодействуют с кислотами
- 46. В соединениях степень окисления цинка +2, проявляет восстановительные свойства Склонен к комплексообразованию, в комплексных соединениях является
- 47. Оказывает влияние на рост и развитие Препараты цинка: сульфат цинка – глазные капли хлорид цинка –
- 48. p-элементы Конфигурация валентного уровня: ns2npa; n- номер уровня, а=1- 6 Способны проявляют переменную степень окисления (S,
- 49. О-В свойства Окислительные свойства H20 + Ca0 = Ca+2H2- – гидрид кальция Восстановительные свойства Cu+2O +
- 50. Составить характеристику элементов С, О, Н, N, P, S, K, Na, Ca, Mg, Mn, Fe, Cu,
- 51. План характеристики элемента Положение в периодической системе Возможные и характерные степени окисления Физические свойства элемента, как
- 52. 5. Кислотно-основные свойства (образование гидроксидов, кислот) 6. Окислительно-восстановительные свойства 7. Склонность к комплексообразованию 8. Медико-биологическое значение
- 54. Скачать презентацию











































 Презентация Углекислый газ 9 класс
Презентация Углекислый газ 9 класс Газ ацетилен
Газ ацетилен Горные породы
Горные породы Защита полимеров от старения
Защита полимеров от старения Нефть и способы её переработки
Нефть и способы её переработки Введение в кристаллографию
Введение в кристаллографию Анаэробный обмен углеводов (Лекция №8)
Анаэробный обмен углеводов (Лекция №8) Химическая связь. (Лекция 4, 5)
Химическая связь. (Лекция 4, 5) Презентация по Химии "КОРРОЗИЯ МЕТАЛЛОВ" - скачать смотреть бесплатно
Презентация по Химии "КОРРОЗИЯ МЕТАЛЛОВ" - скачать смотреть бесплатно педагогический стаж -11 лет, год окончания вуза - 2000, вуз - Бирский государственный педагогический институт, факультет -биолого
педагогический стаж -11 лет, год окончания вуза - 2000, вуз - Бирский государственный педагогический институт, факультет -биолого Алюминий и его соединения
Алюминий и его соединения Методика решения части С2 ГИА 9 класс
Методика решения части С2 ГИА 9 класс Оксид фосфора
Оксид фосфора Хімічна промисловість
Хімічна промисловість  Виды проб. Отбор проб твердых, жидких и газообразных продуктов из различного вида тары. Хранение проб
Виды проб. Отбор проб твердых, жидких и газообразных продуктов из различного вида тары. Хранение проб Домашняя аптечка исследовательская работа Авторы: Полынникова Анастасия, Савина Мария учащиеся 9 «Б» класса Руководитель: Ма
Домашняя аптечка исследовательская работа Авторы: Полынникова Анастасия, Савина Мария учащиеся 9 «Б» класса Руководитель: Ма Конкурс проектных работ "Химия наука о чудесах!" Выполнила: ученица 8 класса МОУ гимназии № 91 имени М.В.Ломоносова Пожид
Конкурс проектных работ "Химия наука о чудесах!" Выполнила: ученица 8 класса МОУ гимназии № 91 имени М.В.Ломоносова Пожид Теория переходного состояния. Эйринг, Эванс, Поляни. (Лекция 5)
Теория переходного состояния. Эйринг, Эванс, Поляни. (Лекция 5) Застосування електролізу
Застосування електролізу Презентация по Химии "Спирт" - скачать смотреть бесплатно
Презентация по Химии "Спирт" - скачать смотреть бесплатно Каменный уголь. Химический состав каменного угля
Каменный уголь. Химический состав каменного угля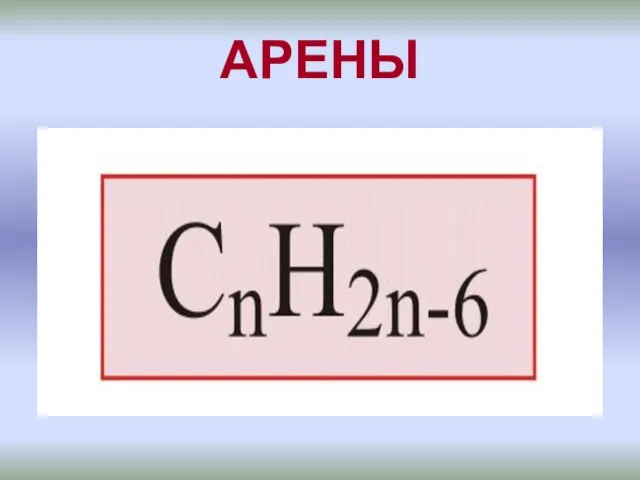 Бензоидные ароматические углеводороды - арены
Бензоидные ароматические углеводороды - арены Презентация тест по химии
Презентация тест по химии Обмен липидов
Обмен липидов Материаловедение. Текстильные волокна, пряжа и ткань
Материаловедение. Текстильные волокна, пряжа и ткань Галогены. Способы получения, применение
Галогены. Способы получения, применение Получение каталитического слоя на основе углеродных нанотрубок с наночастицами платины для водородно–воздушных топливных элеме
Получение каталитического слоя на основе углеродных нанотрубок с наночастицами платины для водородно–воздушных топливных элеме Урок – КВН «Подгруппа углерода и азота»
Урок – КВН «Подгруппа углерода и азота»