Химия Для студентов I курса специальностей: 2080165 — экология, 08040165 — товароведение и экспертиза товаров, 260800 — технология, конст
Содержание
- 2. КИСЛОРОДСОДЕРЖАЩИЕ ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ Кафедра ЭПП, к.х.н., доцент Саверченко А.Н.
- 3. Студент должен: знать строение, номенклатуру, свойства, способы получения и применение кислородсодержащих органических соединений уметь составлять названия
- 4. К кислородсодержащим органическим соединениям относят многочисленные органические соединения, как природного происхождения, так и синтетические, являющиеся производными
- 5. Остальные валентности углерода могут участвовать в образовании связи либо с углеродными атомами, либо с атомами водорода
- 6. Спирты и их производные Производные углеводородов, представляющие собой продукты замещения атома водорода в углеводородной молекуле водным
- 7. Спирты могут содержать и несколько гидроксильных групп но при разных атомах углерода. Число их характеризует атомность
- 8. Строение. Изомерия. Изомерия предельных одноатомных спиртов, общая формула которых CnH2n+1OH, обусловлена изомерией углеродного скелета и изомерией
- 9. Из бутана и изобутана могут быть произведены четыре изомерных бутиловых спирта. В зависимости от положения гидроксильной
- 10. Химические свойства Химические свойства спиртов обусловлены наличием гидроксильной группы. В разнообразных химических превращениях спиртов особая роль
- 11. Кислотные свойства спиртов. Атомы водорода гидроксильных групп в спиртах проявляют определённую подвижность. Подобно воде, спирты реагируют
- 12. По мере увеличения числа углеродных атомов в углеводородных радикалах спиртов активность последних в этой реакции всё
- 13. Окисление спиртов. Кислород воздуха окисляет спирты только при высокой температуре; при этом они горят. В результате
- 14. Большая склонность спиртов к окислению по сравнению с углеводородами объясняется влиянием имеющейся в их молекулах гидроксильной
- 15. При окислении первичных спиртов образуются альдегиды, вторичных – кетоны, окисление третичных спиртов сопровождается разрывом углеродной цепи.
- 16. Дегидратация спиртов. Дегидратация (отнятие воды от молекулы спирта) приводит к образованию этиленовых углеводородов или простых эфиров.
- 17. Внутримолекулярная дегидратация, т.е. за счёт одной молекулы спирта, приводит к образованию этиленового углеводорода:
- 18. Образование сложных эфиров. Взаимодействие спиртов с кислотами (органическими и неорганическими) приводит к образованию производных кислот, называемых
- 19. Способы получения Гидролиз галогеналканов. При действии на галогеналкилы воды в присутствии щелочей происходит реакция гидролиза, в
- 20. Реакция протекает при каталитическом участии образуемых щелочами ионов OH - . В присутствии щелочей галогеноводородная кислота
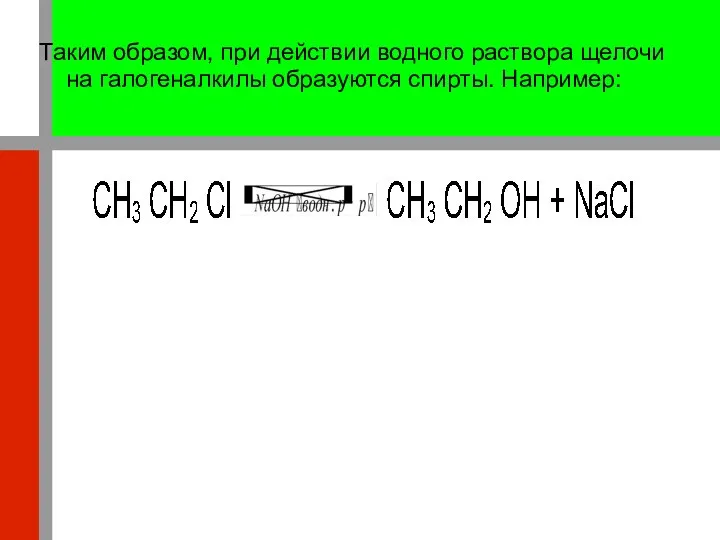
- 21. Таким образом, при действии водного раствора щелочи на галогеналкилы образуются спирты. Например:
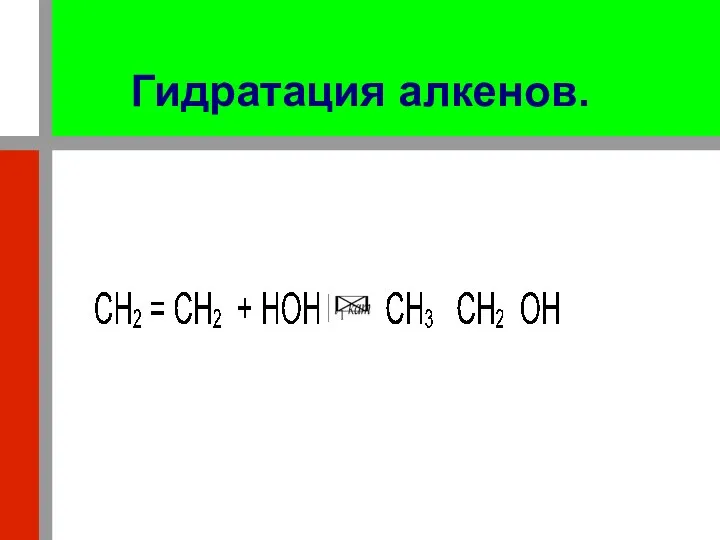
- 22. Гидратация алкенов. При нагревании в присутствии катализаторов (хлорид цинка, серная кислота) элементы воды (водород и гидроксил)
- 23. С гомологоми этилена реакция протекает по правилу Марковникова. Например:
- 24. Восстановление альдегидов и кетонов. При действии водорода в момент выделения (H) на карбонильные соединения альдегиды восстанавливаются
- 25. Специфические способы получения спиртов. Некоторые спирты получают характерными только для них способами. Так, метанол в промышленности
- 26. Синтез газ получают при пропускании паров воды над раскаленным углем: Этанол (этиловый спирт) в промышленности получают
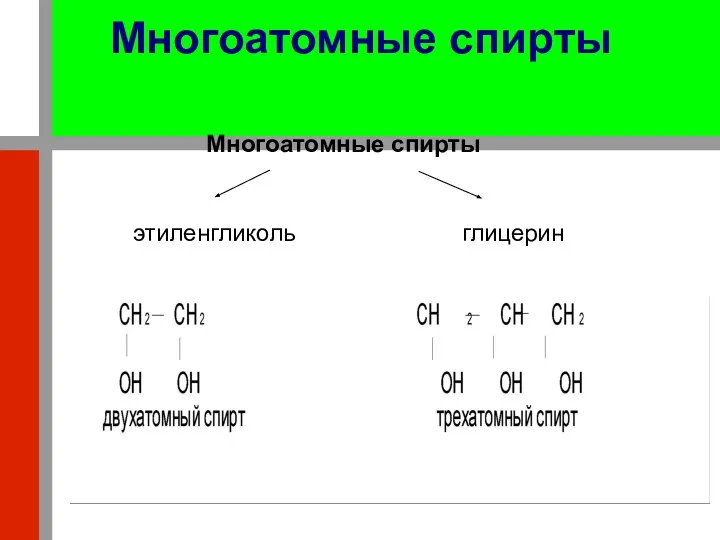
- 27. Многоатомные спирты Многоатомные спирты этиленгликоль глицерин
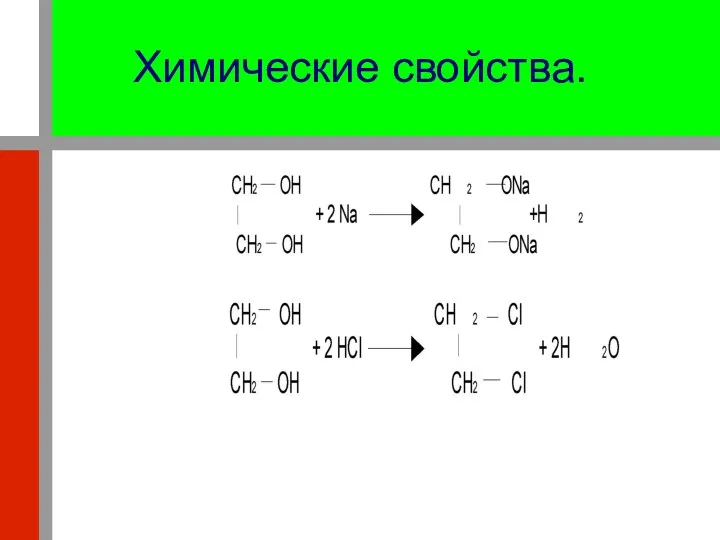
- 28. Химические свойства. 1. Реагируют со щелочными металлами: 2. Реагируют с галогеноводородами:
- 29. 3. Реагируют с кислотами, образуя сложные эфиры: 4. Реагируют с гидроксидом меди (II) – качественная реакция
- 31. Скачать презентацию
























 Нахимичили? Теперь убираем… Работу выполнил ученик 11А класса МОУСОШ №4 г Маркса Тарасов Антон Руководитель РЯБОВА О.Е. 0 учитель химии
Нахимичили? Теперь убираем… Работу выполнил ученик 11А класса МОУСОШ №4 г Маркса Тарасов Антон Руководитель РЯБОВА О.Е. 0 учитель химии Окислительно-восстановительные процессы
Окислительно-восстановительные процессы Определение воды по Фишеру. Кислотное число, число омыления. Определение аминного азота
Определение воды по Фишеру. Кислотное число, число омыления. Определение аминного азота Гетерофункциональные органические соединения
Гетерофункциональные органические соединения Технология получения многослойного и малослойного графена
Технология получения многослойного и малослойного графена Государственные лаборатории по контролю качества лекарственных средств. Основные элементы надлежащей лабораторной практики
Государственные лаборатории по контролю качества лекарственных средств. Основные элементы надлежащей лабораторной практики Презентация по Химии "Группа веществ, изолируемых из биологического материала дистилляцией («Летучие яды»)" - скачать смотрет
Презентация по Химии "Группа веществ, изолируемых из биологического материала дистилляцией («Летучие яды»)" - скачать смотрет Горение и медленное окисление. Тепловой эффект химической реакции
Горение и медленное окисление. Тепловой эффект химической реакции Химические и физические явления в жизни человека
Химические и физические явления в жизни человека Основания. Гидроксид алюминия
Основания. Гидроксид алюминия Общая химическая технология
Общая химическая технология Предмет физиологии центральной нервной системы
Предмет физиологии центральной нервной системы Властивості етанової (оцтової) кислоти
Властивості етанової (оцтової) кислоти Почва. Интегрированный урок по химии и географии
Почва. Интегрированный урок по химии и географии Гели. Удельная вязкость
Гели. Удельная вязкость Минеральные компоненты молока и молочных продуктов. Макроэлементы
Минеральные компоненты молока и молочных продуктов. Макроэлементы :Химиялық реакциялардың кинетикалық жіктелуі.Ферментті катализ.Ферменттердің әсер ету ерекшеліктері
:Химиялық реакциялардың кинетикалық жіктелуі.Ферментті катализ.Ферменттердің әсер ету ерекшеліктері Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства
Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства Тепловой баланс котла
Тепловой баланс котла Металлические яды, изоляция минерализацией. Применение металлов и их соединений в клинической фармации
Металлические яды, изоляция минерализацией. Применение металлов и их соединений в клинической фармации Области применения серной, соляной, азотной, и уксусной кислот
Области применения серной, соляной, азотной, и уксусной кислот Анаэробный обмен углеводов (Лекция №8)
Анаэробный обмен углеводов (Лекция №8) Купрум. Знаходження в періодичній системі
Купрум. Знаходження в періодичній системі Розчини
Розчини Знатоки химии. Кроссворд
Знатоки химии. Кроссворд Основы минералогии. Характеристика минералов
Основы минералогии. Характеристика минералов Пуриновые основания
Пуриновые основания Цинк
Цинк