Содержание
- 2. КОНСУЛЬТАЦИЯ: 11 января 2017 г. в К2 в 16-00 ЭКЗАМЕН (в K2 в 9-00) ХЕБО-13-16 13
- 3. ПЛАН ЛЕКЦИИ Химия элементов VIA-группы. 1. Общая характеристика халькогенов. Свойства простых веществ. 2. Соединения халькогенов с
- 4. Ливерморий Polonium - Польша Халькогены – «рождающие руду» χαλκος - руда γεννάω - рождать ύξός –
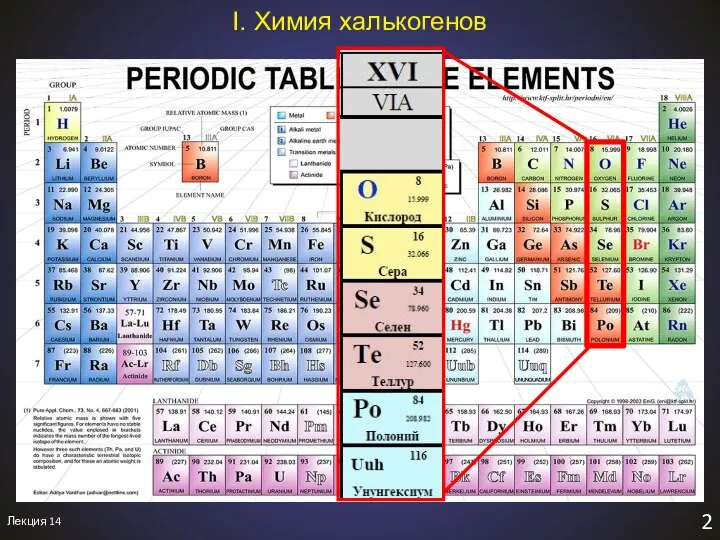
- 5. Лекция 14 3 I. Халькогены. Общая характеристика 1. Общая характеристика элементов 1.1. Строение атома (электронное). 1.2
- 6. Лекция 14 4 II. Химия халькогенов. Общая характеристика 1.1. Строение атома (валентные подуровни). XVI (VIA) O,
- 7. Лекция 14 5 1.2. Физико-химические свойства простых веществ II. Химия халькогенов. Общая характеристика S8 tпл =
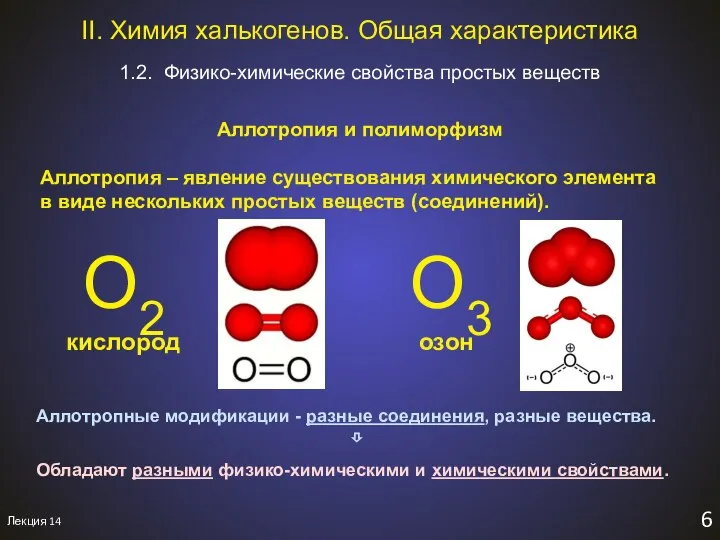
- 8. Лекция 14 6 1.2. Физико-химические свойства простых веществ II. Химия халькогенов. Общая характеристика Aллотропия и полиморфизм
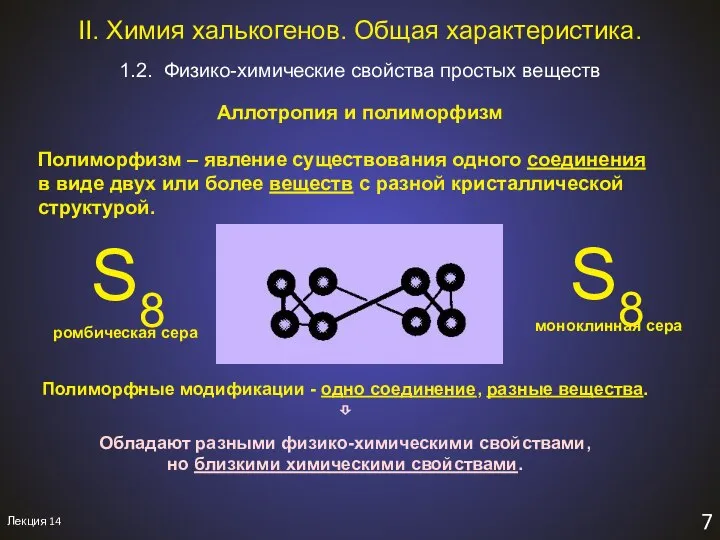
- 9. Лекция 14 7 Полиморфизм – явление существования одного соединения в виде двух или более веществ с
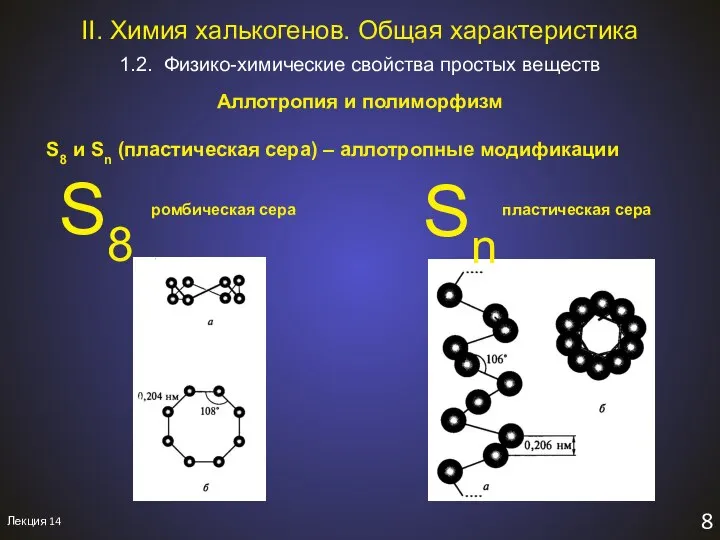
- 10. Лекция 14 8 1.2. Физико-химические свойства простых веществ II. Химия халькогенов. Общая характеристика Aллотропия и полиморфизм
- 11. Лекция 14 9 1.2. Физико-химические свойства простых веществ II. Химия халькогенов. Общая характеристика Электроотрицательность – условная
- 12. Лекция 14 10 II. Химия халькогенов. Общая характеристика 1.3. Химические свойства, общие для всех элементов групп
- 13. Лекция 3 11 В). Кислотные свойства растворов халькогеноводородов (S, Se, Te) H2Э + H2O ⮀ HЭ-
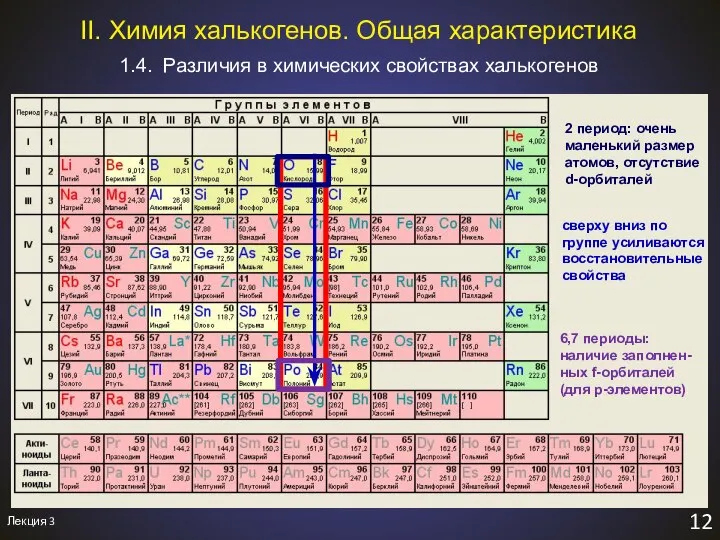
- 14. 2 период: очень маленький размер атомов, отсутствие d-орбиталей сверху вниз по группе усиливаются восстановительные свойства Лекция
- 15. Лекция 3 13 1.4. Различия в химических свойствах халькогенов II. Химия халькогенов. Общая характеристика A). Очень
- 16. Лекция 14 14 1.4. Различия в химических свойствах халькогенов II. Химия халькогенов. Общая характеристика Б). Увеличение
- 17. Лекция 14 15 1.5. Химические свойства простых веществ II. Химия халькогенов. Общая характеристика А). С водой
- 18. Лекция 14 16 1.6. Нахождение в природе II. Химия халькогенов. Общая характеристика КИСЛОРОД: 47.2% – самый
- 19. Лекция 14 17 1.6. Нахождение в природе II. Химия халькогенов. Общая характеристика СЕРА: 0.05% Встречается в
- 20. Лекция 14 18 1.6. Нахождение в природе II. Химия халькогенов. Общая характеристика СЕЛЕН: 6.0·10-5 %, редкий
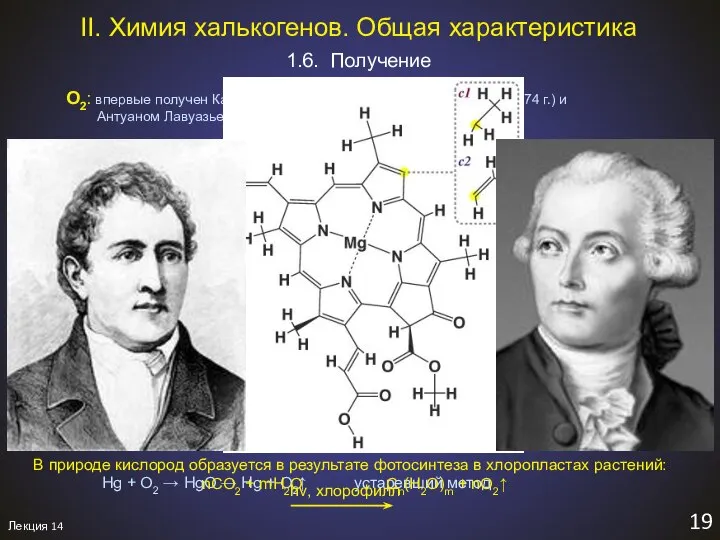
- 21. Лекция 14 19 1.6. Получение II. Химия халькогенов. Общая характеристика
- 22. Лекция 14 20 O3: впервые получен Шёнбейном в 1840 г. öζω - пахну Современные методы получения:
- 23. Лекция 14 21 1.6. Получение II. Химия халькогенов. Общая характеристика S8 известна с древнейших времён. Современные
- 24. Лекция 14 22 1.6. Получение II. Химия халькогенов. Общая характеристика Se: открыт Йёнсом Якобом Берцелиусом в
- 25. Лекция 3 23 1.6. Получение II. Химия халькогенов. Общая характеристика Po: открыт Марией Склодовской-Кюри и Пьером
- 26. Лекция 14 24 1.7. Применение II. Химия галогенов. Общая характеристика O: ● дыхание растений и животных
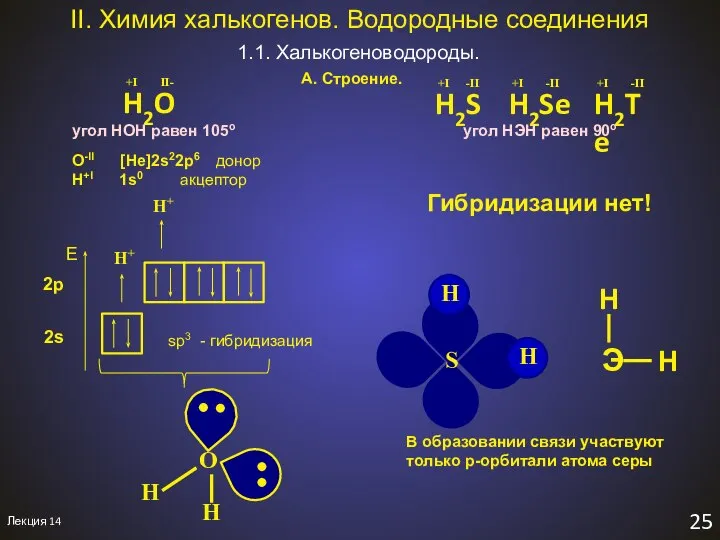
- 27. Лекция 14 25 II. Химия халькогенов. Водородные соединения 1.1. Халькогеноводороды. A. Строение. O-II [He]2s22p6 донор H+I
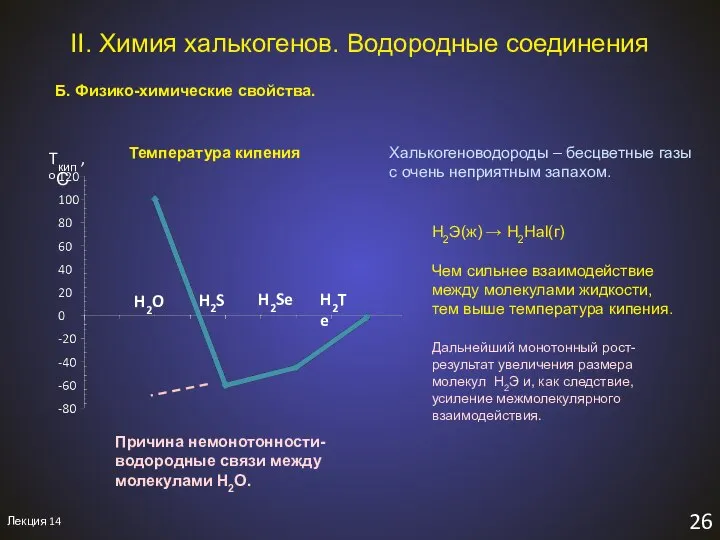
- 28. Лекция 14 26 II. Химия халькогенов. Водородные соединения Б. Физико-химические свойства. Причина немонотонности- водородные связи между
- 29. H2S 1. Промышленный методы: побочный продукт очистки нефти, природных и промышленных газов 2. Лабораторные методы: FeS2
- 30. Лекция 14 28 В. Химические свойства. I. Химия халькогенов. Водородные соединения 1) .Протолиз: H2Э + H2O
- 31. Лекция 14 29 В. Химические свойства (продолжение). II. Химия халькогенов. Водородные соединения 2). Сильные восстановительные свойства
- 32. Лекция 14 30 II. Химия халькогенов. Сульфиды. 1.2. Сульфиды А. Получение Fe + S = FeS
- 33. Лекция 14 31 II. Химия халькогенов. Сульфиды. 1.2. Сульфиды Задача 1. Рассчитайте молярную концентрацию сероводорода в
- 34. Лекция 14 32 II. Химия халькогенов. Сульфиды. В. Гидролиз Обратимый гидролиз: Na2S = 2Na+ + S2-
- 35. Лекция 14 33 II. Химия халькогенов. Водородные соединения 1.3. Сульфаны и полисульфиды. H2Sn n = 1÷23
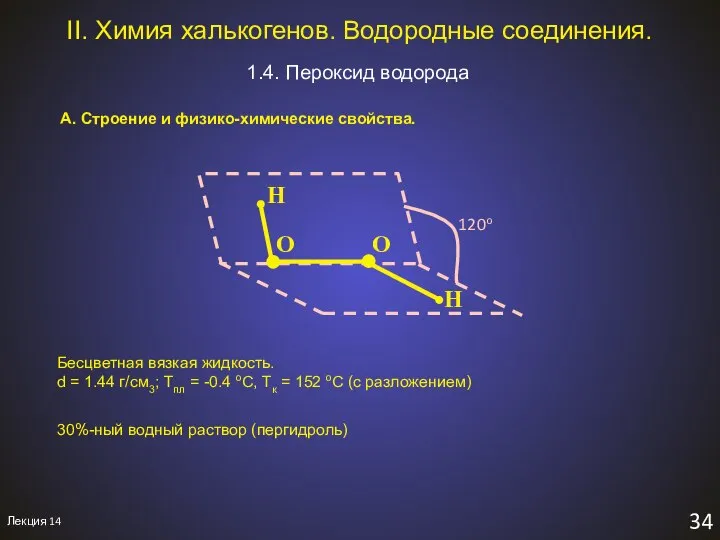
- 36. Лекция 14 34 II. Химия халькогенов. Водородные соединения. 1.4. Пероксид водорода A. Строение и физико-химические свойства.
- 37. Лекция 14 35 II. Химия халькогенов. Пероксид водорода. Б. Получение. Промышленные методы: 1). Окисление гидрохинонов кислородом
- 38. Лекция 14 36 II. Химия халькогенов. Пероксид водорода. В. Химические свойства. 2). Окислительные свойства: 3). Восстановительные
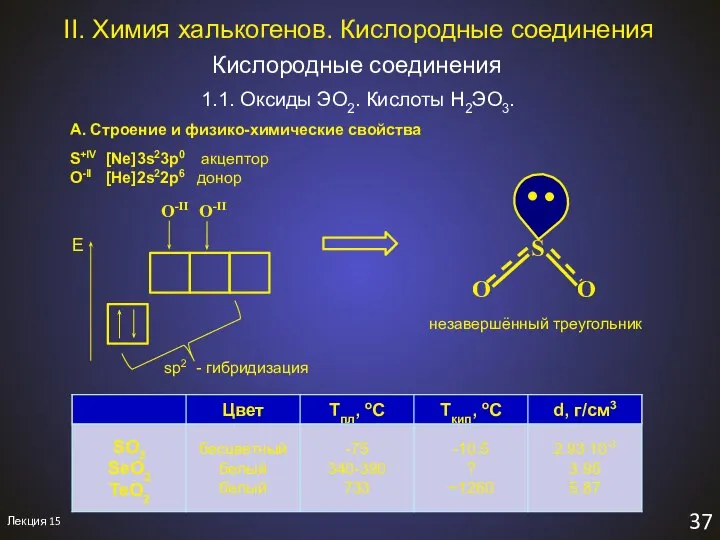
- 39. Лекция 15 37 II. Химия халькогенов. Кислородные соединения Кислородные соединения 1.1. Оксиды ЭO2. Кислоты H2ЭO3. А.
- 40. Лекция 3 37 Б. Получение II. Химия халькогенов. Оксиды ЭO2 t t
- 41. Лекция 2 38 В. Химические свойства 1). Взаимодействие с водой: SO2 + H2O ⮀ SO2∙H2O SO2
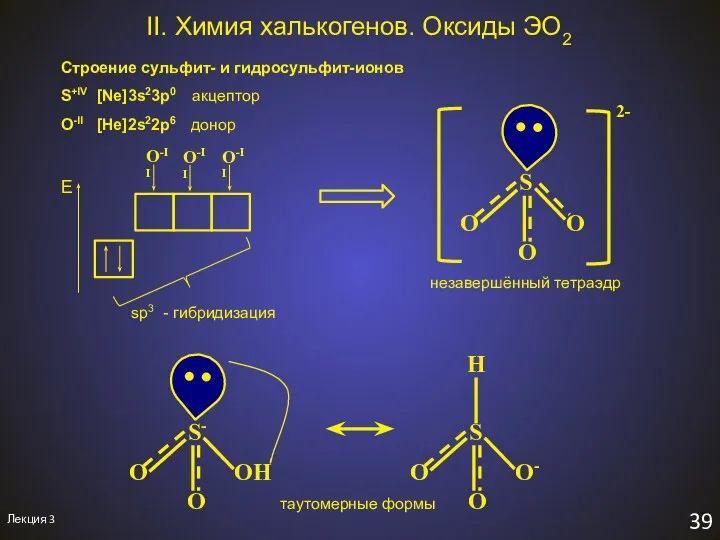
- 42. Лекция 3 39 Строение сульфит- и гидросульфит-ионов II. Химия халькогенов. Оксиды ЭO2 S+IV [Ne]3s23p0 акцептор O-II
- 43. Лекция 3 40 В. Химические свойства (продолжение) 3). Восстановительные свойства: II. Химия халькогенов. Оксиды ЭO2 5SO2
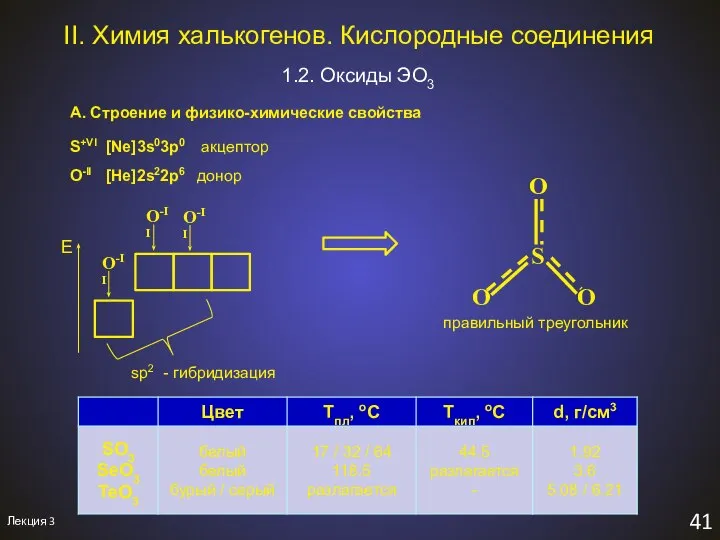
- 44. Лекция 3 41 II. Химия халькогенов. Кислородные соединения 1.2. Оксиды ЭO3 S+VI [Ne]3s03p0 акцептор O-II [He]2s22p6
- 45. Лекция 3 42 II. Химия халькогенов. Оксиды ЭO3 Б. Получение 1. В промышленности: 2SO2(г) + O2(г)
- 46. Лекция 3 43 II. Химия халькогенов. Оксиды ЭO3 В. Химические свойства 2). Взаимодействие с водой: SO3
- 47. Лекция 3 44 II. Химия халькогенов. Оксиды ЭO3 В. Химические свойства (продолжение) 3). Кислотные свойства: SO3
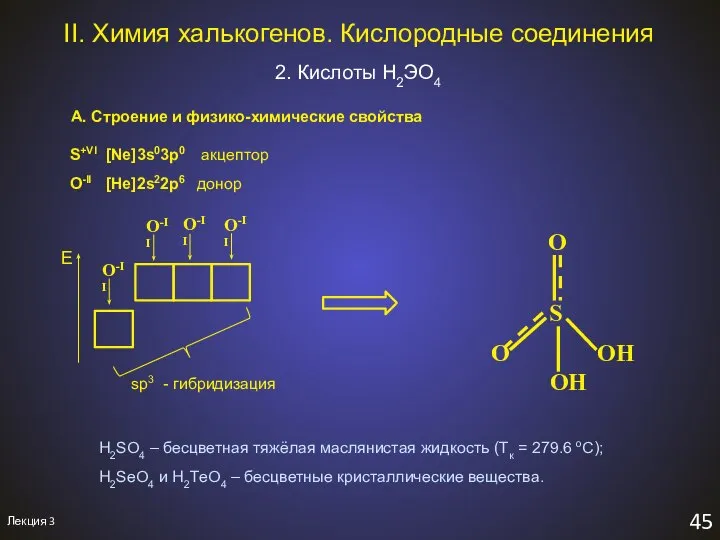
- 48. Лекция 3 45 II. Химия халькогенов. Кислородные соединения 2. Кислоты H2ЭO4 А. Строение и физико-химические свойства
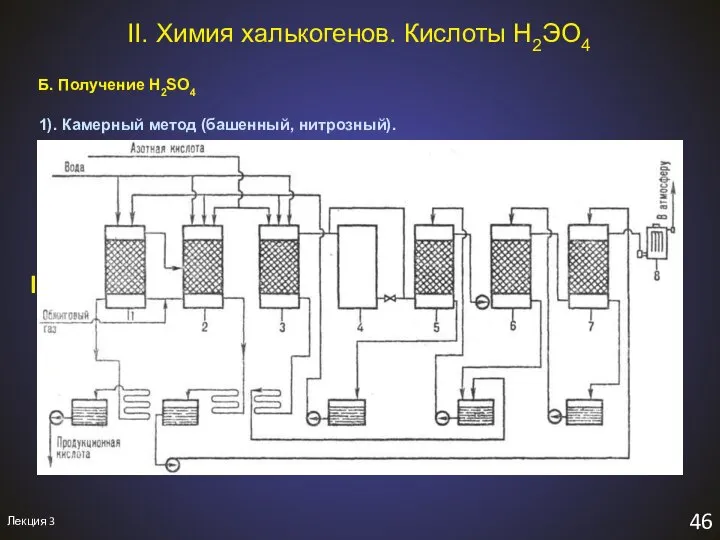
- 49. Лекция 3 46 II. Химия халькогенов. Кислоты H2ЭO4 Б. Получение H2SO4 1). Камерный метод (башенный, нитрозный).
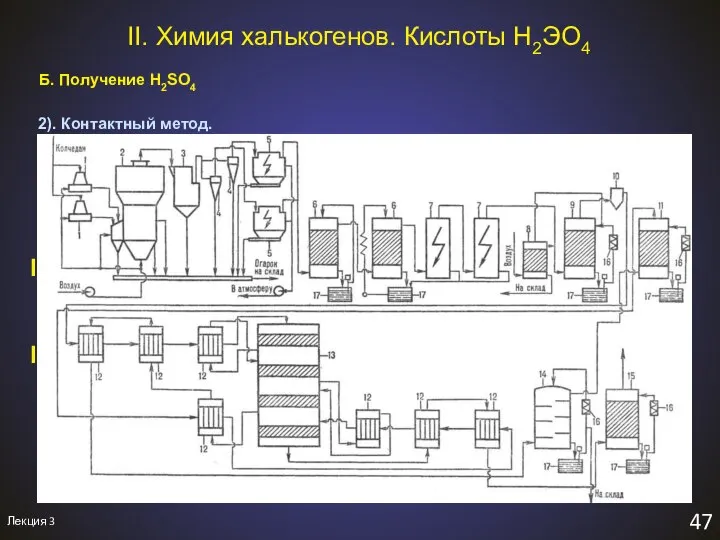
- 50. Лекция 3 47 II. Химия халькогенов. Кислоты H2ЭO4 Б. Получение H2SO4 2). Контактный метод. I. 2FeS2
- 51. Лекция 3 48 II. Химия халькогенов. Кислоты H2ЭO4 Б. Получение H2SO4 3). Купоросный метод FeSO4∙7H2O =
- 52. Лекция 3 49 II. Химия халькогенов. Кислоты H2ЭO4 Г. Химические свойства 1). Протолиз: H2ЭO4 + 2H2O
- 53. Лекция 3 50 II. Химия халькогенов. Кислоты H2ЭO4 Г. Химические свойства 3). Окислительные свойства: 2H2SO4(конц) +
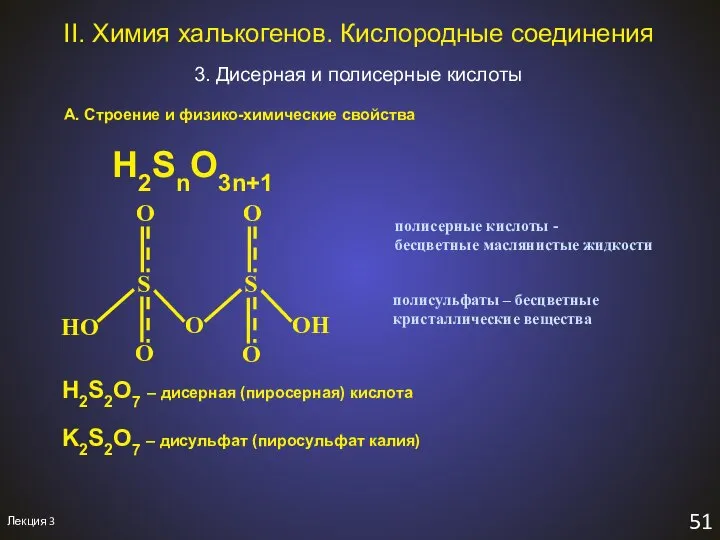
- 54. Лекция 3 51 II. Химия халькогенов. Кислородные соединения 3. Дисерная и полисерные кислоты А. Строение и
- 55. Лекция 1 52 Б. Получение II. Химия халькогенов. Кислородные соединения Дисерная кислота и дисульфаты H2SO4(конц) +
- 56. Московский государственный университет тонких химических технологий им. М.В. Ломоносова ХИМИЯ ЭЛЕМЕНТОВ 16 (VIA) группы Лектор: доц.,
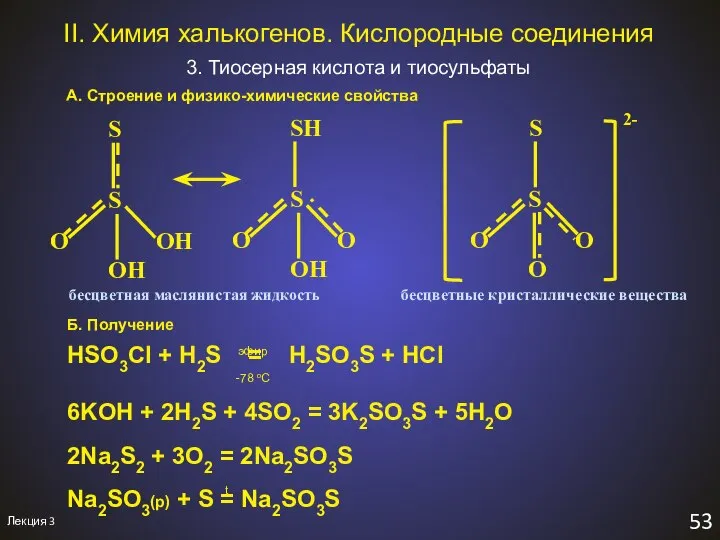
- 57. Лекция 3 53 II. Химия халькогенов. Кислородные соединения 3. Тиосерная кислота и тиосульфаты А. Строение и
- 58. Лекция 3 54 II. Химия халькогенов. Тиосульфаты В. Химические свойства 1). Термическое разложение 2). Раложение в
- 59. Лекция 3 54 II. Химия халькогенов. Тиосульфаты В. Химические свойства 4). Комплексообразующие свойства AgI (т) +
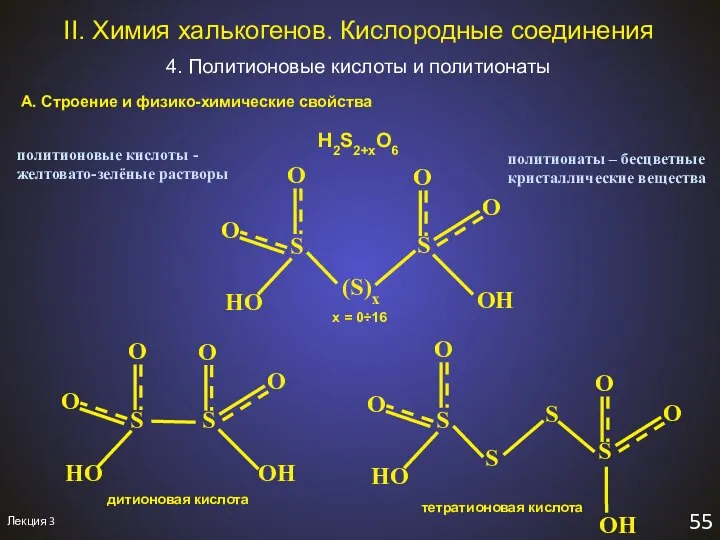
- 60. Лекция 3 55 II. Химия халькогенов. Кислородные соединения 4. Политионовые кислоты и политионаты А. Строение и
- 61. Лекция 1 56 II. Химия халькогенов. Политионаты Б. Получение H2Sx + 2SO3 = H2S2+xO6 эфир -78
- 62. Лекция 2 57 II. Химия халькогенов. Политионаты В. Химические свойства Na2S2O6 = Na2SO4 + SO2↑ 1).
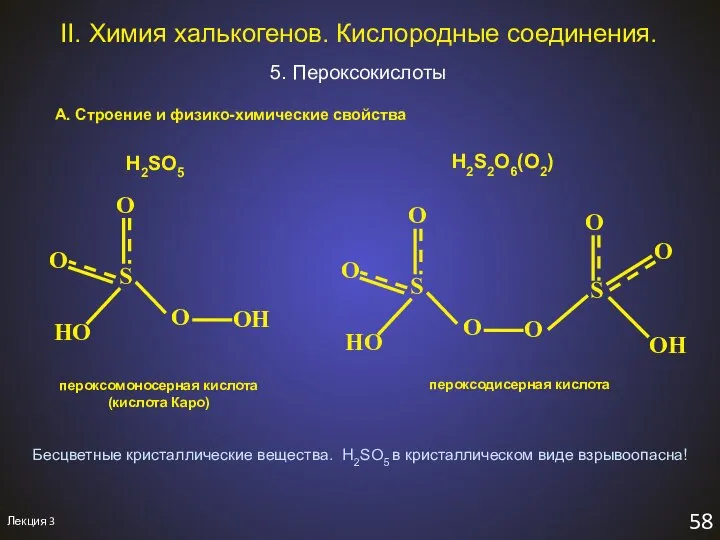
- 63. Лекция 3 58 II. Химия халькогенов. Кислородные соединения. 5. Пероксокислоты А. Строение и физико-химические свойства пероксомоносерная
- 64. Лекция 3 59 II. Химия халькогенов. Пероксокислоты. Б. Получение катод: 2H3O+ + 2ē = H2 +
- 65. Лекция 3 60 II. Химия халькогенов. Пероксокислоты. В. Химические свойства 3). Взаимодействие с водой H2S2O8 +
- 66. Лекция 3 61 II. Химия халькогенов. Пероксокислоты В. Химические свойства (продолжение) 4). Окислительные свойства 5K2S2O8 +
- 68. Скачать презентацию














































 Биологически важные реакции монофункциональных соединений. Реакционная способность альдегидов, кетонов, карбоновых кислот
Биологически важные реакции монофункциональных соединений. Реакционная способность альдегидов, кетонов, карбоновых кислот Биохимические механизмы нарушения обмена углеводов и липидов
Биохимические механизмы нарушения обмена углеводов и липидов Группа щелочных габброидов
Группа щелочных габброидов Материаловедение. Строение и основные свойства металлов
Материаловедение. Строение и основные свойства металлов Химические методы определения U, Pu, Th
Химические методы определения U, Pu, Th Аминокислоты. Общая формула
Аминокислоты. Общая формула Презентация по Химии "Михайло Ломоносов "Письмо о пользе стекла"" - скачать смотреть
Презентация по Химии "Михайло Ломоносов "Письмо о пользе стекла"" - скачать смотреть  Великие иконописцы XIV-XV веков
Великие иконописцы XIV-XV веков Хроматографические методы анализа. Метод газовой хроматографии
Хроматографические методы анализа. Метод газовой хроматографии Откуда берутся кристаллы
Откуда берутся кристаллы Презентация по химии Синтетические каучуки, строение, свойства, применение.
Презентация по химии Синтетические каучуки, строение, свойства, применение.  Турнир "Наследники Менделеева". Отборочный тур
Турнир "Наследники Менделеева". Отборочный тур Электролитическая диссоциация. 9 класс
Электролитическая диссоциация. 9 класс Генетическая связь между классами органических веществ
Генетическая связь между классами органических веществ Электролитическая диссоциация
Электролитическая диссоциация Химическая связь
Химическая связь “РОЗЧИННИК”
“РОЗЧИННИК”  Нуклеопротеиды. Структура и функция нуклеиновых кислот. (Лекция 4)
Нуклеопротеиды. Структура и функция нуклеиновых кислот. (Лекция 4) Минерал хромдиопсид. Месторождения
Минерал хромдиопсид. Месторождения Ғажайып химия
Ғажайып химия Изоаллоксазин туындылары (В2 тобының витаминдері)
Изоаллоксазин туындылары (В2 тобының витаминдері) Ионообменная хроматография и ее применение
Ионообменная хроматография и ее применение Сложные эфиры
Сложные эфиры Классификация неорганических веществ. Оксиды. Автор: Калитина Тамара Михайловна Место работы: МОУ СОШ №3 с.Александров-Гай
Классификация неорганических веществ. Оксиды. Автор: Калитина Тамара Михайловна Место работы: МОУ СОШ №3 с.Александров-Гай  Способы количественного определения белка
Способы количественного определения белка Алкандар. Алкенес. Алкинес
Алкандар. Алкенес. Алкинес Химиялық байланыс және заттардың құрылымдық түрлі сатылары
Химиялық байланыс және заттардың құрылымдық түрлі сатылары Значение воды. Изучение биологических свойств воды
Значение воды. Изучение биологических свойств воды