Содержание
- 2. История открытия хлора В 1774 году шведский химик Карл Вильгельм Шееле (1742 – 1786) провел опыт,
- 3. Положение хлора в ПСХЭ Д.И. Менделеева. Строение атома. период группа порядковый номер Cl неметалл 17 3
- 4. Нахождение в природе По распространенности в природе хлор занимает 11-е место. Хлор образует следующие важнейшие минералы:
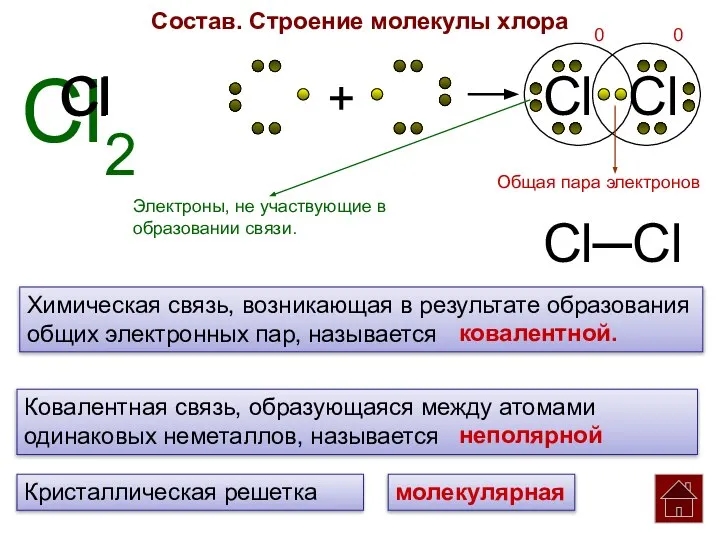
- 5. Cl2 Cl Cl + Cl Cl Состав. Строение молекулы хлора Химическая связь, возникающая в результате образования
- 6. Получение хлора В лаборатории: 2KMnO4+16HCl=2MnCl2+2KCl+5Cl2+8H2O В промышленности хлор получают электролизом раствора или расплава хлорида натрия. 2NaCl
- 7. Химические свойства хлора Взаимодействие с простыми веществами: а) металлами б) неметаллами 2. Взаимодействие со сложными веществами
- 8. Взаимодействие с простыми веществами (металлами): а)Наиболее энергично хлор реагирует с металлами, причем с некоторыми из них
- 9. Взаимодействие хлора с фосфором Составьте уравнение реакции. Рассмотрите с т.зр. ОВР. Взаимодействие с простыми веществами (неметаллами)
- 10. Взаимодействие хлора с водородом Составьте уравнение реакции взаимодействия хлора с водородом. Рассмотрите с т. зр. ОВР
- 11. Взаимодействие со сложными веществами F2 Cl2 Br2 I 2 уменьшение окислительных свойств увеличение восстановительных свойств Хлор
- 12. Хлор вступает в реакции с органическими веществами
- 13. Взаимодействие хлора с органическими растворителями Растворение хлора в воде сопровождается и химическим взаимодействием. Cl2 + H2O
- 14. Кислородные соединения хлора Хлор непосредственно с кислородом не взаимодействует, однако этот галоген образует достаточно много кислородных
- 15. Применение хлора 1. Хлорирование воды 3. Средства защиты растений 6. Растворители 7. Красители 8. Отбеливание ткани
- 16. Cl2 1 2 3 4 5 6 7 8
- 18. Скачать презентацию














 Химические Недотроги
Химические Недотроги  Гетероциклические соединения. Шестичленные гетероциклы с одним гетероатомом
Гетероциклические соединения. Шестичленные гетероциклы с одним гетероатомом Биохимия соединительной ткани
Биохимия соединительной ткани Силикаты. Классификация силикатов
Силикаты. Классификация силикатов Выполнила: Смирнова Маргарита Ученица: 9-а класса
Выполнила: Смирнова Маргарита Ученица: 9-а класса Презентация по Химии "«Подгруппа углерода»" - скачать смотреть
Презентация по Химии "«Подгруппа углерода»" - скачать смотреть  Презентация по Химии "Химия в разных науках" - скачать смотреть
Презентация по Химии "Химия в разных науках" - скачать смотреть  Неорганические вещества
Неорганические вещества Методы количественного определения «металлических» ядов в минерализате (деструктате)
Методы количественного определения «металлических» ядов в минерализате (деструктате) Кислотно-основное титрование в неводных средах
Кислотно-основное титрование в неводных средах Amino acid and protein metabolism II
Amino acid and protein metabolism II Презентация по химии Ученика 10 «А» класса Амелина Станислава
Презентация по химии Ученика 10 «А» класса Амелина Станислава Минералы соединения ртути
Минералы соединения ртути Муниципальное общеобразовательное учреждение Средняя общеобразовательная школа № 73» Тема проекта: Гидролиз органических веще
Муниципальное общеобразовательное учреждение Средняя общеобразовательная школа № 73» Тема проекта: Гидролиз органических веще Химические реакции спиртов
Химические реакции спиртов Повышение эффективности процесса сополимеризации бутадиена и α-метилстирола. Производительность 83000 т/год
Повышение эффективности процесса сополимеризации бутадиена и α-метилстирола. Производительность 83000 т/год Химия вокруг нас
Химия вокруг нас c4bf82f888b84ff1b75efb1a64c84b0f
c4bf82f888b84ff1b75efb1a64c84b0f Кислотно-основное титрование. 4 лекция. Часть 2
Кислотно-основное титрование. 4 лекция. Часть 2 Презентація з хімії 11 клас «Ізомерія»
Презентація з хімії 11 клас «Ізомерія»  Химическая кинетика
Химическая кинетика Горіння твердих речовин
Горіння твердих речовин ФОСФОР «СВЕТОНОСНЫЙ»
ФОСФОР «СВЕТОНОСНЫЙ» Химические элементы в организме человека Выполнил ученик 9 «Г» класса МОУ «сош №50» Жадан Михаил
Химические элементы в организме человека Выполнил ученик 9 «Г» класса МОУ «сош №50» Жадан Михаил Экологический проект Тема: Лабораторное исследование химического состава чипсов Работу выполнила Купавцева Татьяна
Экологический проект Тема: Лабораторное исследование химического состава чипсов Работу выполнила Купавцева Татьяна  Типы химических реакций на примере свойств воды.
Типы химических реакций на примере свойств воды.  Презентация по Химии "Золото" - скачать смотреть бесплатно
Презентация по Химии "Золото" - скачать смотреть бесплатно Каталітичний крекінг. Основні етапи становлення технології каталітичного крекінгу. Каталізатор крекінгу
Каталітичний крекінг. Основні етапи становлення технології каталітичного крекінгу. Каталізатор крекінгу