Содержание
- 2. Неметали Неметали – прості речовини, які не мають властивостей металів, а саме: металічного блиску, непридатні для
- 3. Фосфор Сірка Углерод
- 4. Азот Азот Сіліцій Бром гелій
- 6. Все це - чистий карбон
- 7. Фізичні властивості алмазу і графіту. Алмаз Прозорий, безбарвний. Не проводить електричний струм, оскільки немає вільних електронів.
- 8. Сірка Сірка може безпосередньо реагувати майже з усіма металами (за винятком благородних), але переважно при нагріванні.
- 9. Загальна інформація про водень Н 2 — газ водень — безколірний, без запаху і смаку газ,
- 10. Фулерен?! Що це? Фулерени - молекулярні з'єднання, що належать класу алотропних форм вуглецю (інші - алмаз,
- 12. Скачать презентацию
Неметали
Неметали – прості речовини, які не мають властивостей металів, а саме:
Неметали
Неметали – прості речовини, які не мають властивостей металів, а саме:
У хімічних реакціях атоми неметалів, як правило, одержують електрони.
До типових неметалів зараховують 22 елементи: водень (гідроґен), азот, кисень (оксиґен), флуор, хлор, інертні гази, бром, карбон, фосфор, сулфур, селен, йод, астат, телур, бор.
Типові оксиди неметалів є ангідридами.
Різкої межі між металами, металоїдами та неметалами немає.
Фосфор
Сірка
Углерод
Фосфор
Сірка
Углерод
Азот
Азот
Сіліцій
Бром
гелій
Азот
Азот
Сіліцій
Бром
гелій
Все це - чистий карбон
Все це - чистий карбон
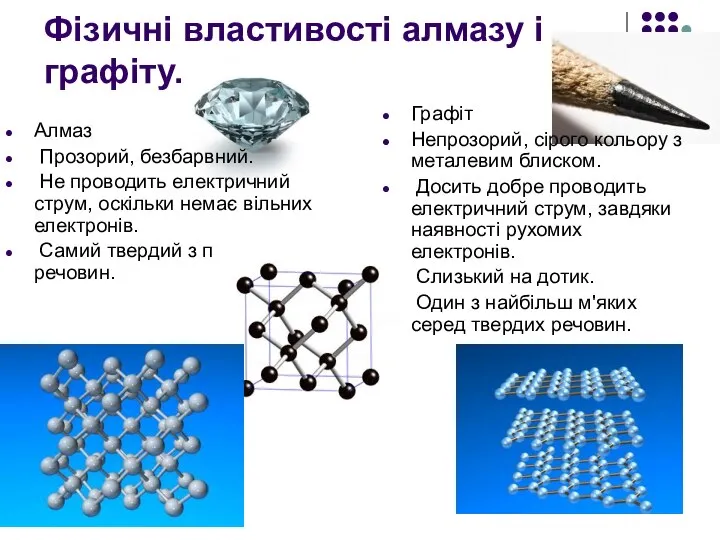
Фізичні властивості алмазу і графіту.
Алмаз
Прозорий, безбарвний.
Не проводить
Фізичні властивості алмазу і графіту.
Алмаз
Прозорий, безбарвний.
Не проводить
Самий твердий з природних речовин.
Графіт
Непрозорий, сірого кольору з металевим блиском.
Досить добре проводить електричний струм, завдяки наявності рухомих електронів.
Слизький на дотик.
Один з найбільш м'яких серед твердих речовин.
Сірка
Сірка може безпосередньо реагувати майже з усіма металами (за винятком благородних),
Сірка
Сірка може безпосередньо реагувати майже з усіма металами (за винятком благородних),
Сірка широко застосовується у різних галузях народного господарства, переважно у хімічній промисловості для виробництва Сульфатної кислоти H2SO4, деяких барвників, і інших хімічних продуктів. Значні кількості сірки споживає гумова промисловість для вулканізації каучуку,тобто для перетворення каучуку в гуму. Сірку використовують також у сірниковому виробництві, в піротехніці, у виробництві чорного пороху тощо. У медицині сірка йде для виготовлення сіркової мазі, при лікуванні шкіряних хвороб. У сільському господарстві сірковий цвіт застосовують для боротьби з шкідниками бавовнику, і виноградної, лози.
Загальна інформація про водень
Н 2 — газ водень — безколірний, без
Загальна інформація про водень Н 2 — газ водень — безколірний, без
Лавуазьє дав назву hydrogene (від грец. ὕδωρ — вода та γενναω — народжую) — «той, що народжує воду». Українська назва елементу також відображає входження елементу до складу води. Російська назва «водород» — дослівний переклад латинської назви hydrogenium.
Застосування Гідруванням природних рослинних олій отримують твердий жир — маргарин. Рідкий водень застосовується як ракетне паливо та як охолоджувач, оскільки має найвищу теплопровідність з усіх газів. Суміш кисню з воднем використовують при зварюванні. Дуже перспективним напрямком є використання водня як палива для двигунів нового типу, так званих паливних елементів. У США та в Європі вже існують водневі заправні станції, які забезпечують воднем автомобілі та автобуси, що на ньому працюють.
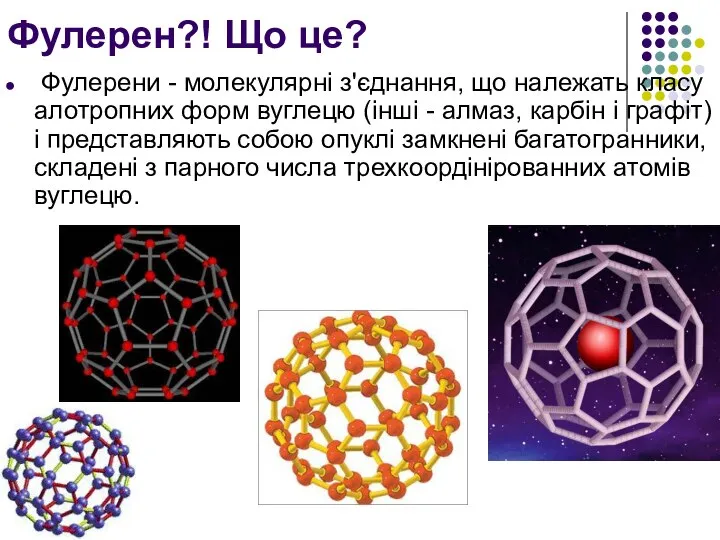
Фулерен?! Що це?
Фулерени - молекулярні з'єднання, що належать класу алотропних
Фулерен?! Що це?
Фулерени - молекулярні з'єднання, що належать класу алотропних







 Автоматизация производства жидкой углекислоты
Автоматизация производства жидкой углекислоты Plastics. General characteristics. Classification. Composition. The main types of plastics, their appointment
Plastics. General characteristics. Classification. Composition. The main types of plastics, their appointment Дисперсные системы
Дисперсные системы Презентация по Химии "Неорганические кислоты" - скачать смотреть
Презентация по Химии "Неорганические кислоты" - скачать смотреть  Превращение (S)-бутанол-2 в другие соединения
Превращение (S)-бутанол-2 в другие соединения Влияние условий на скорость химической реакции
Влияние условий на скорость химической реакции Оксиды Na
Оксиды Na Презентация по Химии "Формы Выделения минералов" - скачать смотреть
Презентация по Химии "Формы Выделения минералов" - скачать смотреть  Современные средства поражений Их краткая характеристика Поражающие факторы
Современные средства поражений Их краткая характеристика Поражающие факторы  Обобщение и систематизация знаний по теме Спирты и фенолы
Обобщение и систематизация знаний по теме Спирты и фенолы Коррозия, как источник загрязнения окружающей среды
Коррозия, как источник загрязнения окружающей среды Хімічні формули
Хімічні формули Исследование состава и свойств молока
Исследование состава и свойств молока Минералдар және олардың агрегаттарының морфологиясы. Минералдарды жүйелеуінің негізі
Минералдар және олардың агрегаттарының морфологиясы. Минералдарды жүйелеуінің негізі Периодический закон Д.И. Менделеева (лекция 3)
Периодический закон Д.И. Менделеева (лекция 3) Тесты для самопроверки
Тесты для самопроверки Индикаторный метод титрования
Индикаторный метод титрования Побутові хімікати
Побутові хімікати Углерод и его соединения
Углерод и его соединения Вуглеводи
Вуглеводи Газоанализаторы. Измерительный прибор для определения качественного и количественного состава смесей газов
Газоанализаторы. Измерительный прибор для определения качественного и количественного состава смесей газов Предмет органической химии. Основные понятия. Лекция 1
Предмет органической химии. Основные понятия. Лекция 1 Химические свойства солей
Химические свойства солей Презентация по Химии "Ковалентная неполярная связь" - скачать смотреть
Презентация по Химии "Ковалентная неполярная связь" - скачать смотреть  Оборотні і необоротні реакції. Хімічна рівновага
Оборотні і необоротні реакції. Хімічна рівновага Лекарственные средства, производные пиримидина, производные барбитуровой кислоты. (Тема 4)
Лекарственные средства, производные пиримидина, производные барбитуровой кислоты. (Тема 4) Презентация по Химии "Презентация Золото" - скачать смотреть
Презентация по Химии "Презентация Золото" - скачать смотреть  Презентация по химии ХИМИЧЕСКАЯ СВЯЗЬ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ
Презентация по химии ХИМИЧЕСКАЯ СВЯЗЬ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ