Содержание
- 2. Элемент - неметалл № 6 в периодической системе C IV группа главная подгруппа Возможные степени окисления:
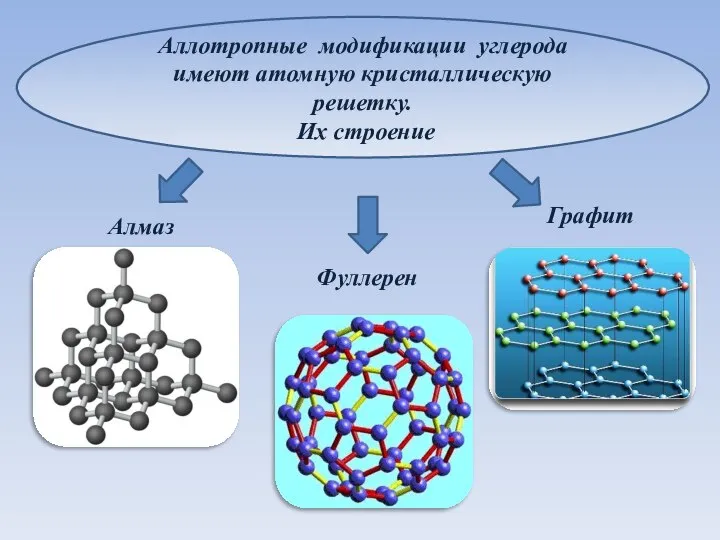
- 3. Аллотропные модификации углерода имеют атомную кристаллическую решетку. Их строение Алмаз Графит Фуллерен
- 4. Алмаз Применяется в: Обрабатывающей промышленности Электротехнике Горной промышленности Ювелирном производстве …это самое твердое вещество на Земле,
- 5. Графит …это мягкое серо-черное вещество, тугоплавкое , являющееся полупроводником со слоистой структурой. Применяется в: Графитовых стержнях-электродах
- 6. Фуллерен Фуллерены планируют использовать: 1. Для создания фотоприемников 2. Для создания сверхпроводящих материалов 3. В качестве
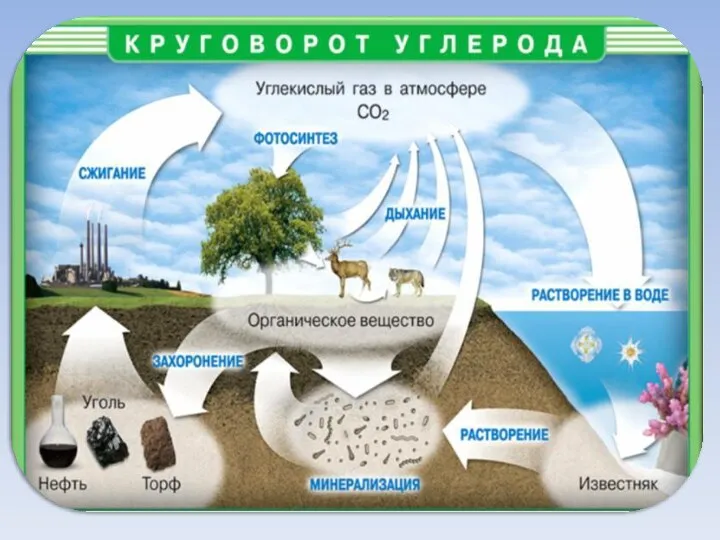
- 7. Нахождение в природе Мел, известняк, мрамор CaCO3 Магнезит MgCO3 Сидерит FeCO3 В самородном виде: алмаз и
- 9. В составе растений и животных (~18 %). В организме человека достигает около 21 % (15 кг
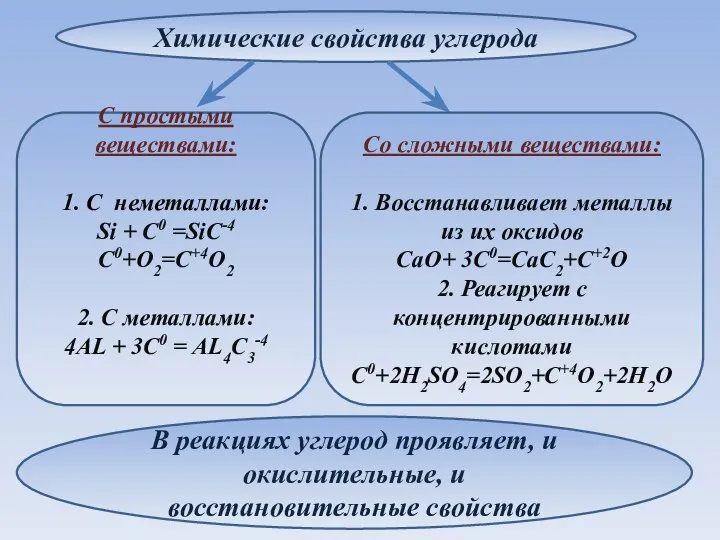
- 10. Химические свойства углерода Со сложными веществами: 1. Восстанавливает металлы из их оксидов CaO+ 3C0=CaC2+C+2O 2. Реагирует
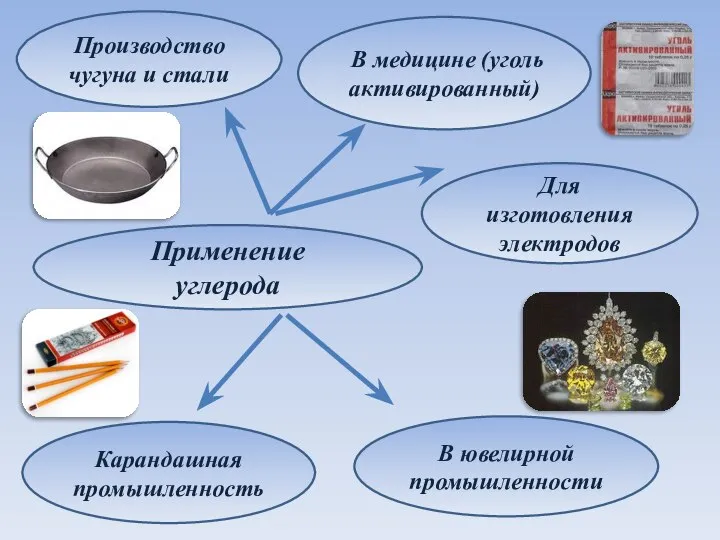
- 11. Применение углерода Производство чугуна и стали В медицине (уголь активированный) Карандашная промышленность Для изготовления электродов В
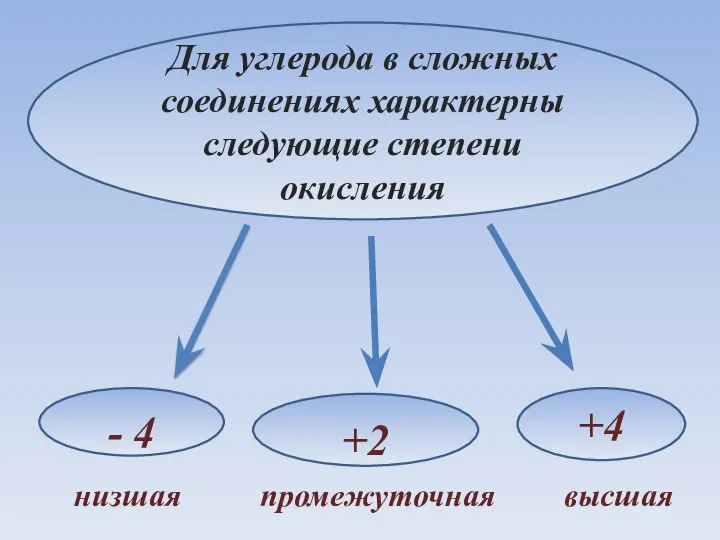
- 12. Для углерода в сложных соединениях характерны следующие степени окисления - 4 +4 +2 низшая промежуточная высшая
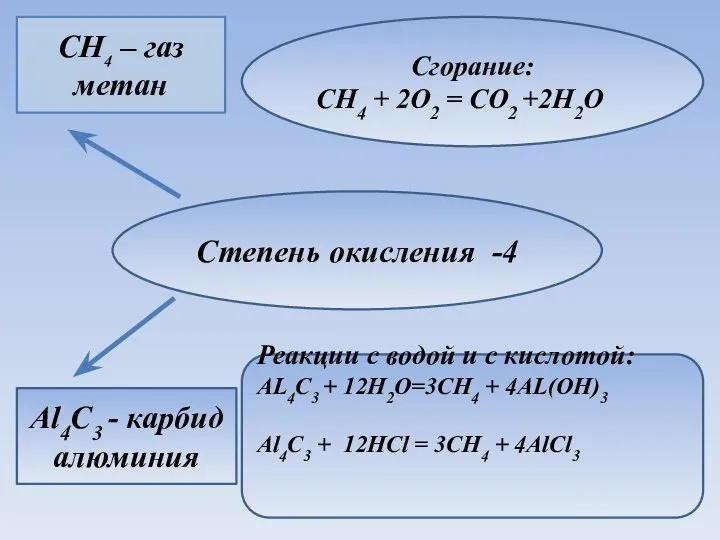
- 13. Степень окисления -4 CH4 – газ метан Al4C3 - карбид алюминия Сгорание: CH4 + 2O2 =
- 14. Степень окисления +2 CO - угарный газ сильный яд, опасный для жизни и здоровья человека (несолеобразующий
- 15. Степень окисления +4 H2CO3-угольная кислота Соли угольной кислоты (например K2CO3-карбонат калия) CO2-углекислый газ
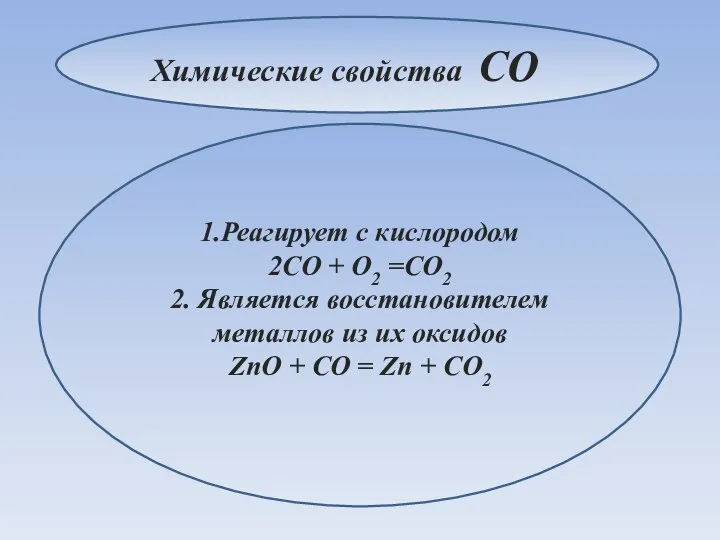
- 16. 1.Реагирует с кислородом 2CO + O2 =CO2 2. Является восстановителем металлов из их оксидов ZnO +
- 17. Химические свойства CO2- (кислотный оксид) 1.Реагирует с водой CO2 + H2O = H2CO3 2.Реагирует с основными
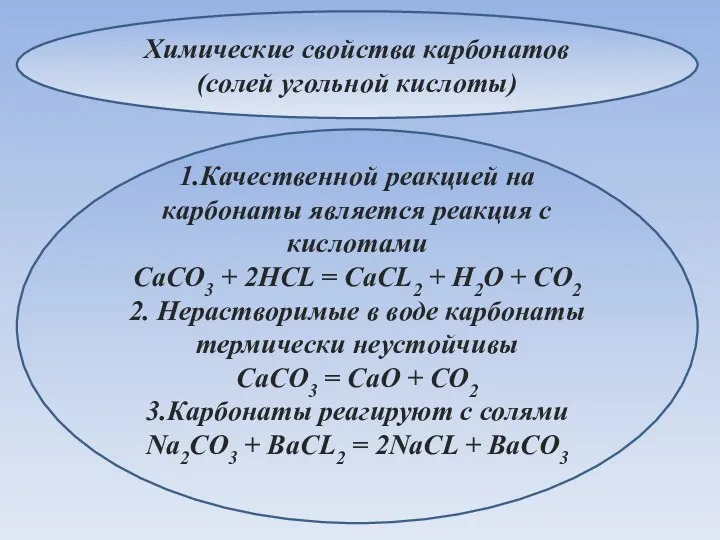
- 18. Химические свойства карбонатов (солей угольной кислоты) 1.Качественной реакцией на карбонаты является реакция с кислотами CaCO3 +
- 19. Углекислотный огнетушитель Сухой лед (хладагент) Сода Моющие средства Лимонады Соединения углерода вокруг нас
- 20. http://urbanjewelers.biz/wp-content/uploads/2010/10/diamonds-e1288016603994.jpg http://www.jabinesban.com/wp-content/uploads/2010/09/fullereno_fullereno.jpg http://s58.radikal.ru/i160/1012/ff/2e7639eb01bc.jpg http://www.rmnt.ru/pub/uploads/glass_cutter_0511_3.jpg http://www.students.by/articles/19/1001931/PH04503.jpg http://art-market.com.ua/media/catalog/product/cache/17/image/9df78eab33525d08d6e5fb8d27136e95/1/1/111111111111111_2.jpg http://im5-tub-ru.yandex.net/i?id=42457246-63-72&n=21 Ссылки на источники информации и изображения: И.И.Новошинский Н.С.Новошинская Химия
- 22. Скачать презентацию










 Физико-химия поверхностных явлений. Основы адсорбционной терапии
Физико-химия поверхностных явлений. Основы адсорбционной терапии Класифікація неорганічних сполук
Класифікація неорганічних сполук Уроки зельеварения. Задача 6
Уроки зельеварения. Задача 6 Предмет, задачи, понятия, законы химии
Предмет, задачи, понятия, законы химии Термодинамические свойства газов
Термодинамические свойства газов Химическое равновесие. Необратимые и обратимые реакции
Химическое равновесие. Необратимые и обратимые реакции Морфология тел полезных ископаемых
Морфология тел полезных ископаемых Презентация по Химии "Белки" - скачать смотреть бесплатно_
Презентация по Химии "Белки" - скачать смотреть бесплатно_ Применение аммиака и солей аммония
Применение аммиака и солей аммония Кислотно-основные равновесия
Кислотно-основные равновесия Поверхностное упрочнение деталей. (Лекция 11)
Поверхностное упрочнение деталей. (Лекция 11) Презентация по химии на тему: «Применение кислорода»
Презентация по химии на тему: «Применение кислорода» Перманганат калия
Перманганат калия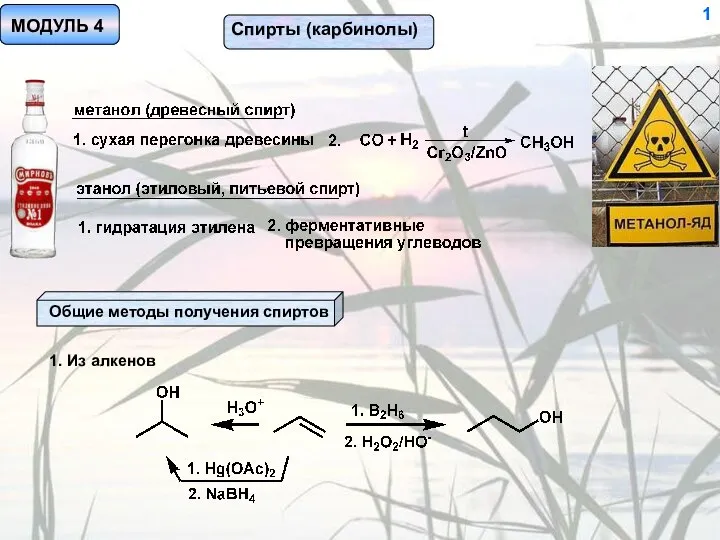 Спирты (карбинолы)
Спирты (карбинолы) Методы исследования наносистем и наноматериалов. Классификация физико-химических методов исследования
Методы исследования наносистем и наноматериалов. Классификация физико-химических методов исследования Отраслевые стандарты качества лекарственных средств: GMP, GLP, GSP, GDP, GPP, GCP и другие
Отраслевые стандарты качества лекарственных средств: GMP, GLP, GSP, GDP, GPP, GCP и другие Обмен веществ. Метаболизм и его функции
Обмен веществ. Метаболизм и его функции Идентификация органических веществ
Идентификация органических веществ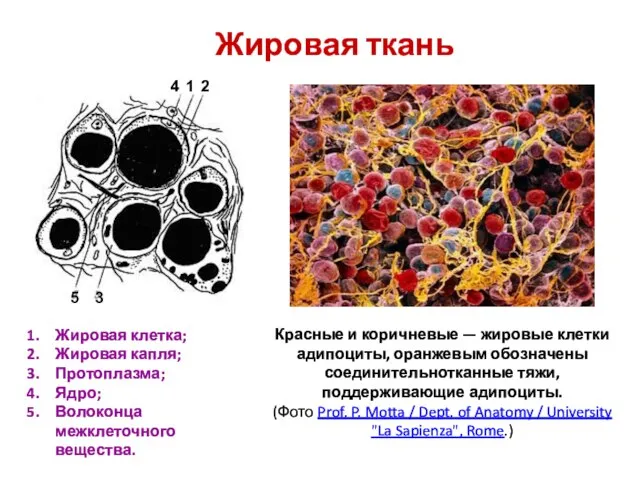 Жировая ткань
Жировая ткань Презентация по Химии "Анализ тенденций развития химии" - скачать смотреть
Презентация по Химии "Анализ тенденций развития химии" - скачать смотреть  Ауылшаруашылық дақылдарының тұқымдарын фунгецидтермен улау және химиялық қорғау тәсілдерінің биологиялық
Ауылшаруашылық дақылдарының тұқымдарын фунгецидтермен улау және химиялық қорғау тәсілдерінің биологиялық Кольорові метали
Кольорові метали 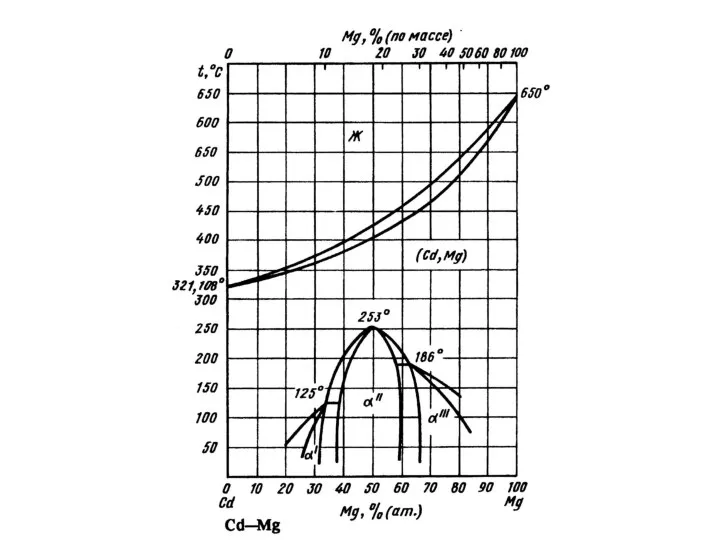 Промежуточные фазы
Промежуточные фазы Смеси и растворы
Смеси и растворы Липидтердің метаболизмі
Липидтердің метаболизмі Аттестационная работа. Образовательная программа элективного курса Химия вокруг нас
Аттестационная работа. Образовательная программа элективного курса Химия вокруг нас В таблиці я ― відомий елемент, Та літеру зміни з одного боку, Переконаєшся в один момент, Що я не елемент вже, а протока. Метаграми
В таблиці я ― відомий елемент, Та літеру зміни з одного боку, Переконаєшся в один момент, Що я не елемент вже, а протока. Метаграми  ЕГЭ по химии
ЕГЭ по химии