Содержание
- 2. Знать: определение химического уравнения; химический смысл закона сохранения массы; значение индексов и коэффициентов в формулах веществ
- 3. Данный закон позднее (1789 г.) подтвердил французский химик А. Лавуазье ЗАКОН СОХРАНЕНИЯ МАССЫ ВЕЩЕСТВ Все перемены
- 4. Масса веществ, вступивших в химическую реакцию, равна массе веществ, получившихся в результате ее. Современная формулировка закона:
- 5. хА + уВ = сАВ ВСПОМНИ! Химическая формула – условная запись состава вещества с помощью химических
- 6. Алгоритм составления уравнений реакций и расстановки коэффициентов методом подбора: 1. В левой части уравнения пишут формулы
- 7. Проверь свои знания: найди ответы под соответствующими буквами и расставь их в правильном порядке. а/ 2,
- 8. 1) Оксид ртути (ll) ртуть + кислород 2) Железо + хлор хлорид железа (lll) 3) Натрий
- 10. Скачать презентацию







 Презентация по Химии "Мы изучаем химию" - скачать смотреть
Презентация по Химии "Мы изучаем химию" - скачать смотреть  Наноматериалы
Наноматериалы Алюминий и его сплавы
Алюминий и его сплавы Общие сведения о полезных ископаемых. (Лекция 2)
Общие сведения о полезных ископаемых. (Лекция 2) Оксиды. Определение
Оксиды. Определение Кальций (Ca)
Кальций (Ca) Природній та супутній нафтові гази, їх склад, використання
Природній та супутній нафтові гази, їх склад, використання Воздушные вяжущие вещества. Технология производства гипсовых вяжущих. Свойства и их хранение. Ангидритовые вяжущие. (Лекция 2)
Воздушные вяжущие вещества. Технология производства гипсовых вяжущих. Свойства и их хранение. Ангидритовые вяжущие. (Лекция 2) Карбоновые кислоты
Карбоновые кислоты Калій. Знаходження в періодичній системі і основні характеристики
Калій. Знаходження в періодичній системі і основні характеристики Презентация по Химии "Стероиды" - скачать смотреть
Презентация по Химии "Стероиды" - скачать смотреть  Углерод и кремний
Углерод и кремний Круговорот азота в природе
Круговорот азота в природе Оксиды. Химические свойства оксидов
Оксиды. Химические свойства оксидов Теория строения органических соединений
Теория строения органических соединений Дисциплина: Химия. Лекция 1. Растворы
Дисциплина: Химия. Лекция 1. Растворы Соединения магния и щелочноземельных металлов, их применение
Соединения магния и щелочноземельных металлов, их применение Изменения свойств химических элементов и их соединений в группах и периодах
Изменения свойств химических элементов и их соединений в группах и периодах Алканы. Пропан
Алканы. Пропан Радиоуглеродный анализ
Радиоуглеродный анализ Выполнила: Здановская Карина 9 А класс
Выполнила: Здановская Карина 9 А класс 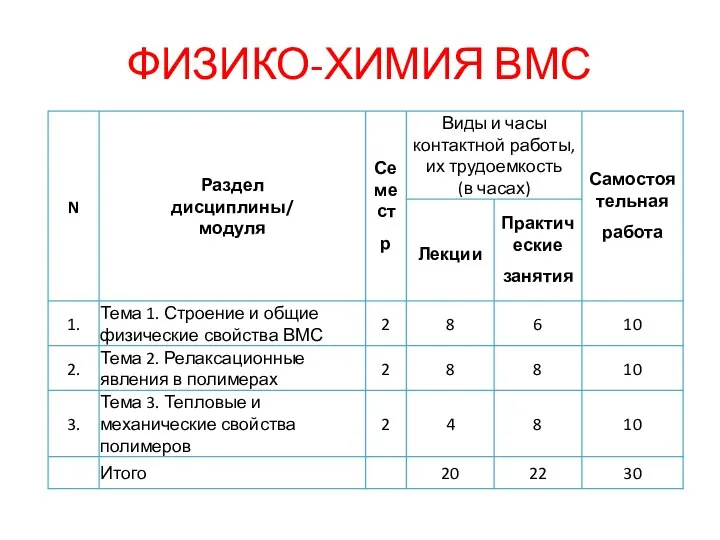 Строение и общие физические свойства ВМС. Релаксационные явления в полимерах. Тепловые и механические свойства полимеров
Строение и общие физические свойства ВМС. Релаксационные явления в полимерах. Тепловые и механические свойства полимеров Кислород. Историческая справка
Кислород. Историческая справка Оцтова кислота Презентація підготовлена ученицею 9 класу Лук'яновою Іриною
Оцтова кислота Презентація підготовлена ученицею 9 класу Лук'яновою Іриною  Аттестационная работа. Образовательная программа внеурочной деятельности «Химия и физика с детства». (1-4 класс)
Аттестационная работа. Образовательная программа внеурочной деятельности «Химия и физика с детства». (1-4 класс) Гидроксилпроизводные углеводородов
Гидроксилпроизводные углеводородов Полимеры
Полимеры 11 хб
11 хб