Содержание
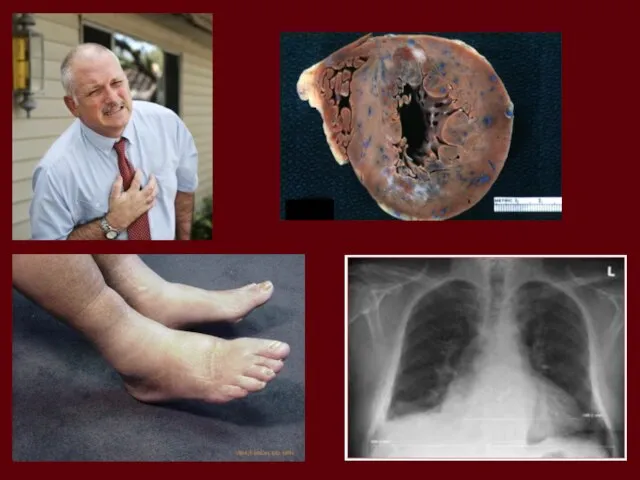
- 4. НЕДОСТАТНІСТЬ СЕРЦЯ – неспроможність органу забезпечувати нормальний хвилинний об`єм крові Недостатність серця від перевантаження 2. Недостатність
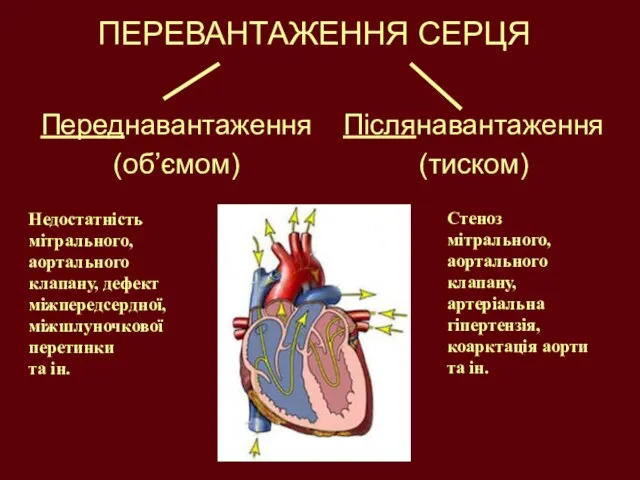
- 5. ПЕРЕВАНТАЖЕННЯ СЕРЦЯ Переднавантаження (об’ємом) Післянавантаження (тиском) Недостатність мітрального, аортального клапану, дефект міжпередсердної, міжшлуночкової перетинки та ін.
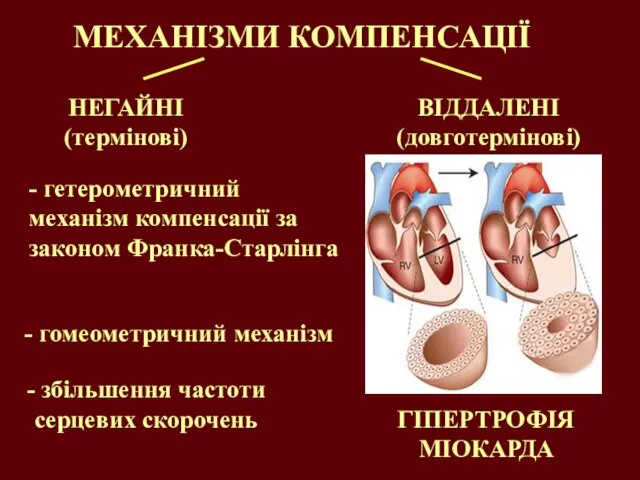
- 6. МЕХАНІЗМИ КОМПЕНСАЦІЇ НЕГАЙНІ (термінові) - гетерометричний механізм компенсації за законом Франка-Старлінга - гомеометричний механізм - збільшення
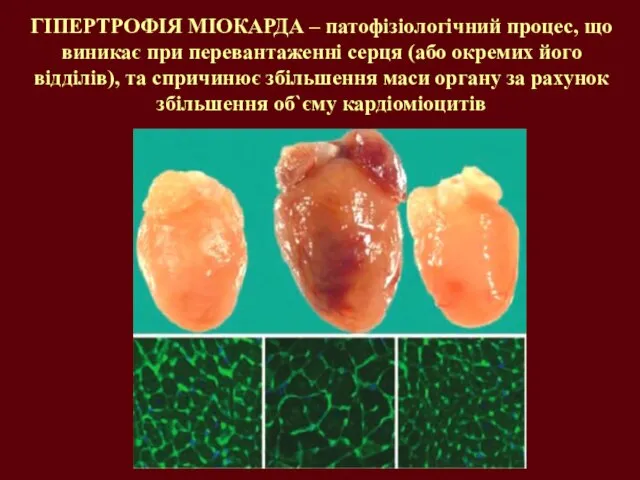
- 7. ГІПЕРТРОФІЯ МІОКАРДА – патофізіологічний процес, що виникає при перевантаженні серця (або окремих його відділів), та спричинює
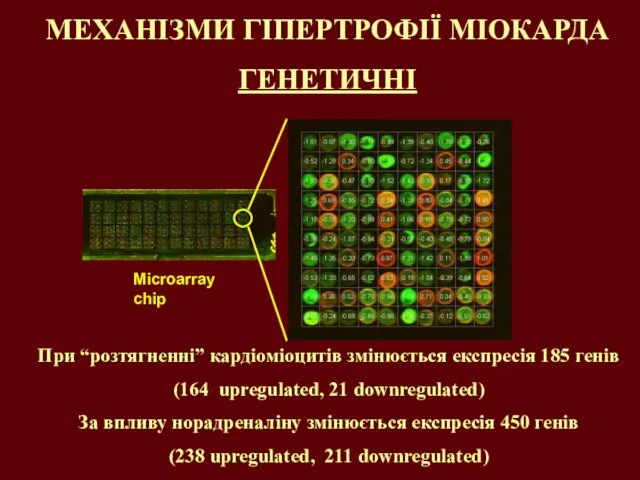
- 8. МЕХАНІЗМИ ГІПЕРТРОФІЇ МІОКАРДА ГЕНЕТИЧНІ При “розтягненні” кардіоміоцитів змінюється експресія 185 генів (164 upregulated, 21 downregulated) За
- 9. СТАДІЇ ГІПЕРТРОФІЇ МІОКАРДА (за Ф.З.Меєрсоном) 1. Аварійна 2. Завершеної гіпертрофії та відносно стійкої гіперфункції 3. Поступового
- 10. ФАТАЛЬНІ ПАРАДОКСИ ГІПЕРТРОФІЇ МІОКАРДА V3 → S2 При збільшенні об`єму в кубі – площа збільшується лише
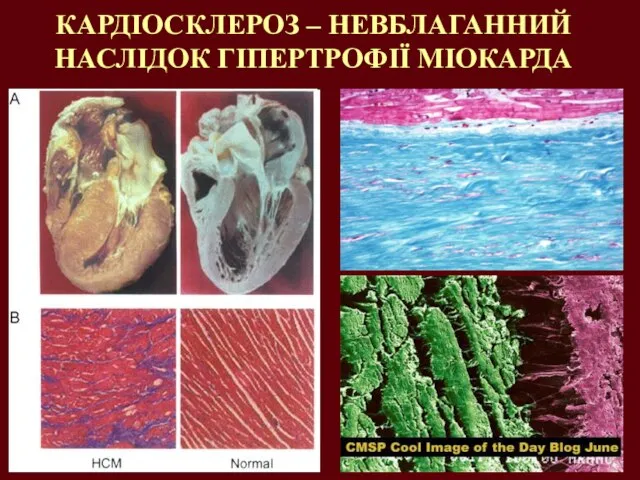
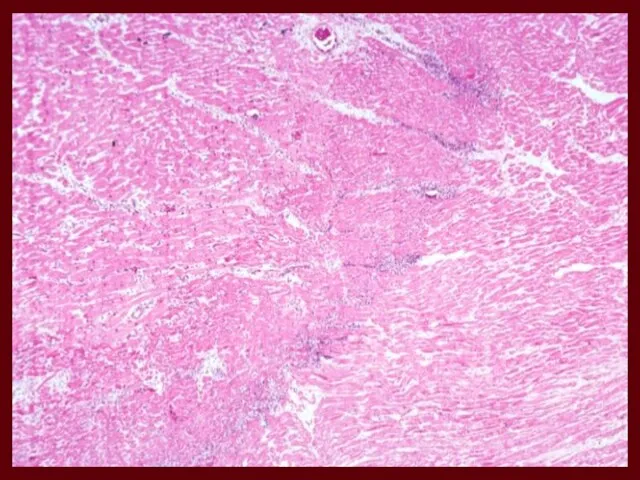
- 11. КАРДІОСКЛЕРОЗ – НЕВБЛАГАННИЙ НАСЛІДОК ГІПЕРТРОФІЇ МІОКАРДА
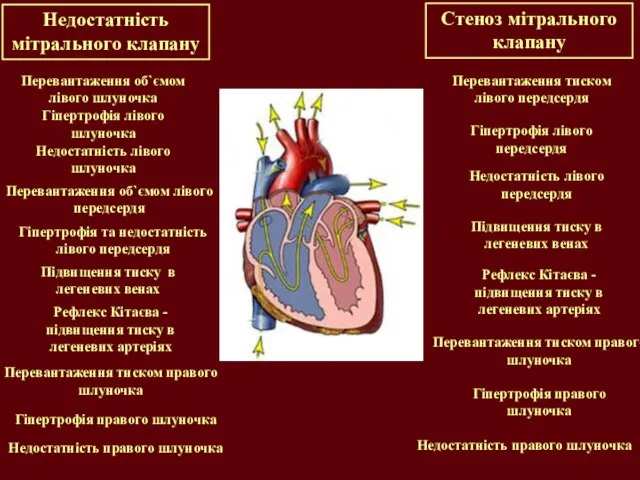
- 12. Недостатність мітрального клапану Перевантаження об`ємом лівого шлуночка Гіпертрофія лівого шлуночка Недостатність лівого шлуночка Підвищення тиску в
- 13. НЕДОСТАТНІСТЬ СЕРЦЯ – неспроможність органу забезпечувати нормальний хвилинний об`єм крові 1. Недостатність серця від перевантаження 2.
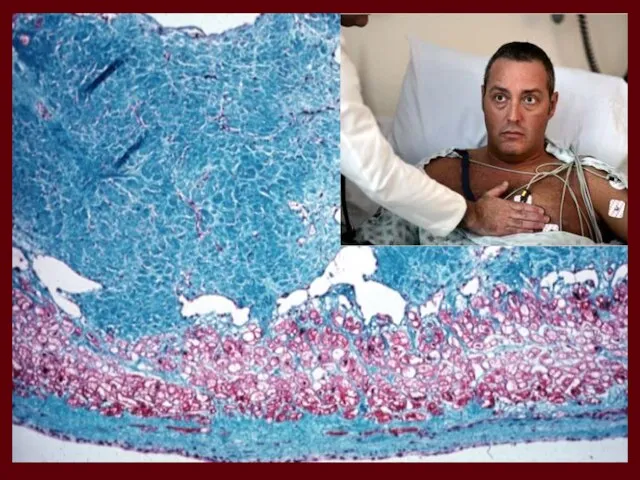
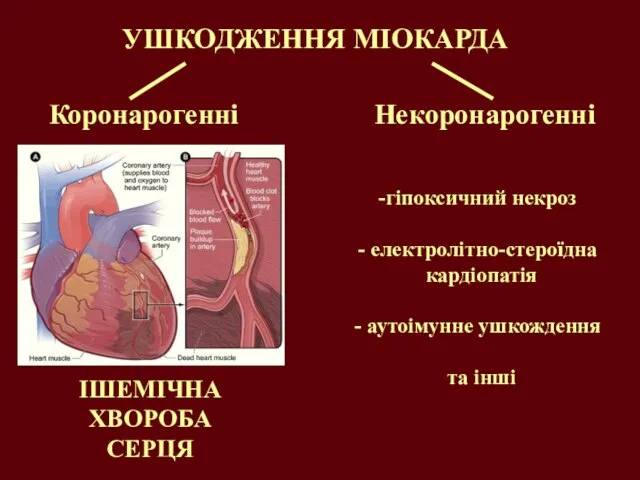
- 14. УШКОДЖЕННЯ МІОКАРДА Коронарогенні Некоронарогенні гіпоксичний некроз електролітно-стероїдна кардіопатія аутоімунне ушкождення та інші ІШЕМІЧНА ХВОРОБА СЕРЦЯ
- 15. ІШЕМІЧНА ХВОРОБА СЕРЦЯ – мультифакторне захворювання, що характеризується абсолютним або відносним порушенням кровопостачання міокарда внаслідок ураження
- 16. ФАКТОРИ РИЗИКУ ІШЕМІЧНОЇ ХВОРОБИ СЕРЦЯ ЕКЗОГЕННІ ЕНДОГЕННІ Алельний поліморфізм генів - SNP Переїдання (дисліпідемії, ожиріння, цукровий
- 17. Алельний поліморфізм – феномен, що визначає генетичну гетерогенність популяції та генетичну індивідуальність кожної людини ~ 30
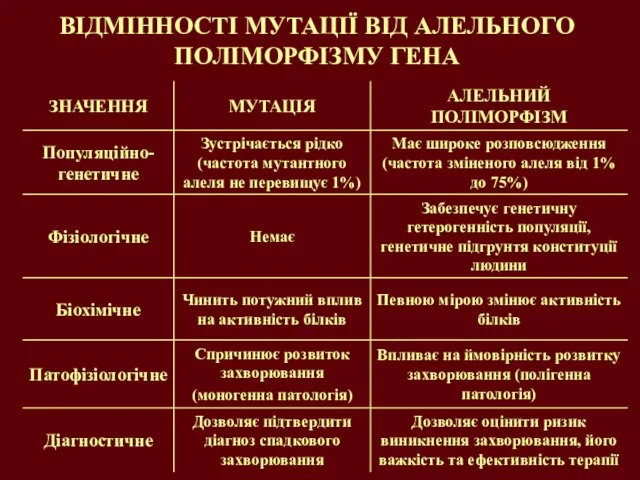
- 18. ВІДМІННОСТІ МУТАЦІЇ ВІД АЛЕЛЬНОГО ПОЛІМОРФІЗМУ ГЕНА
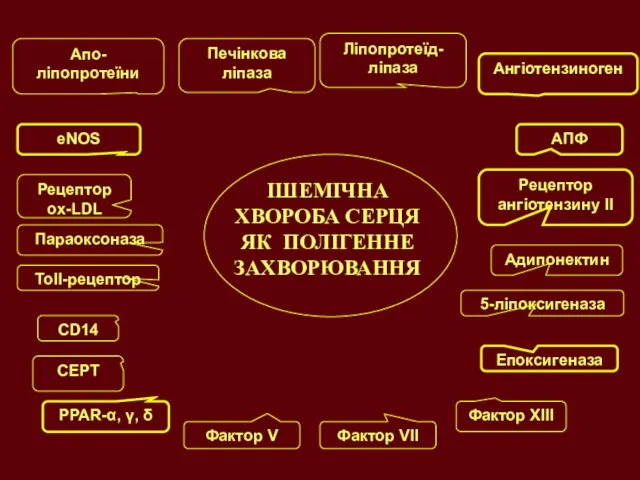
- 19. ІШЕМІЧНА ХВОРОБА СЕРЦЯ ЯК ПОЛІГЕННЕ ЗАХВОРЮВАННЯ PPAR-α, γ, δ CEPT Печінкова ліпаза Ліпопротеїд-ліпаза Ангіотензиноген AПФ Адипонектин
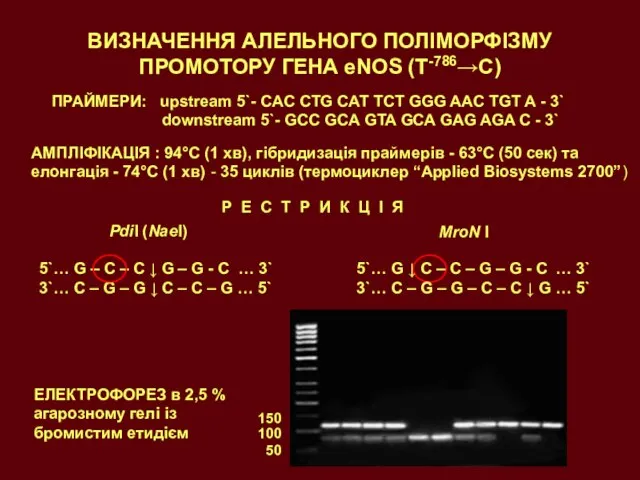
- 20. ВИЗНАЧЕННЯ АЛЕЛЬНОГО ПОЛІМОРФІЗМУ ПРОМОТОРУ ГЕНА eNOS (T-786→C) ПРАЙМЕРИ: upstream 5`- CAC CTG CAT TCT GGG AAC
- 21. ЗАСТОСУВАННЯ ПЛР В РЕАЛЬНОМУ ЧАСІ ДЛЯ ВИЗНАЧЕННЯ ПОЛІМОРФІЗМУ ПООДИНОКИХ НУКЛЕОТИДІВ
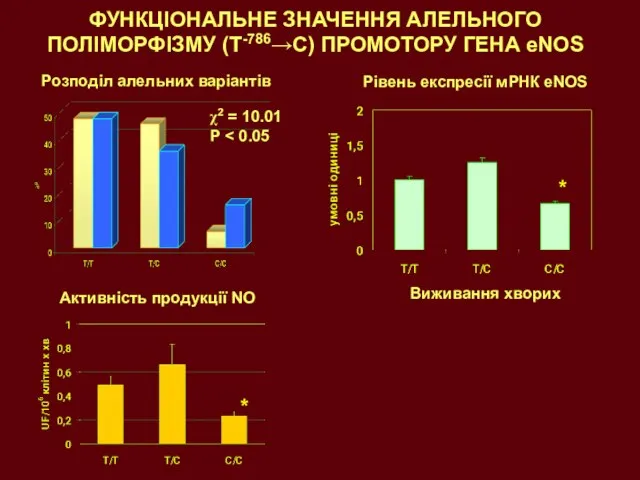
- 22. ФУНКЦІОНАЛЬНЕ ЗНАЧЕННЯ АЛЕЛЬНОГО ПОЛІМОРФІЗМУ (T-786→C) ПРОМОТОРУ ГЕНА еNOS χ2 = 10.01 P Розподіл алельних варіантів Рівень
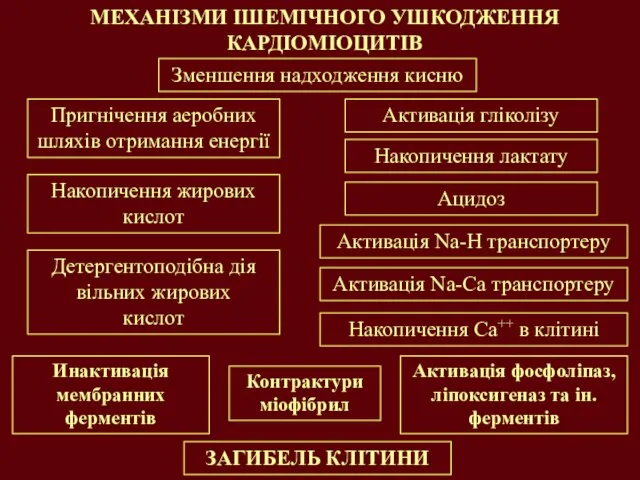
- 23. МЕХАНІЗМИ ІШЕМІЧНОГО УШКОДЖЕННЯ КАРДІОМІОЦИТІВ ЗАГИБЕЛЬ КЛІТИНИ Зменшення надходження кисню Пригнічення аеробних шляхів отримання енергії Активація гліколізу
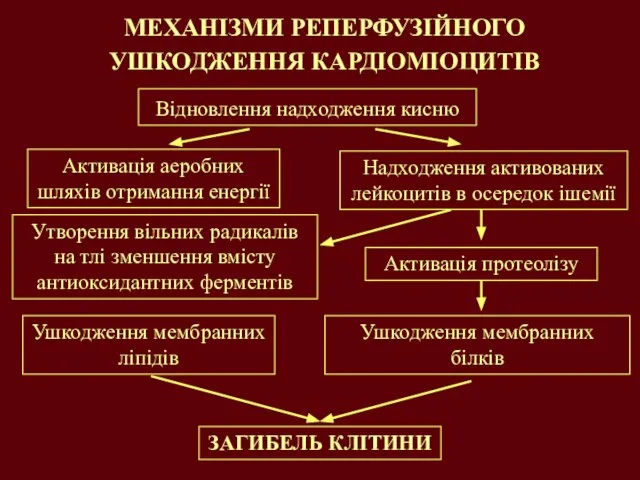
- 24. МЕХАНІЗМИ РЕПЕРФУЗІЙНОГО УШКОДЖЕННЯ КАРДІОМІОЦИТІВ ЗАГИБЕЛЬ КЛІТИНИ Відновлення надходження кисню Активація аеробних шляхів отримання енергії Надходження активованих
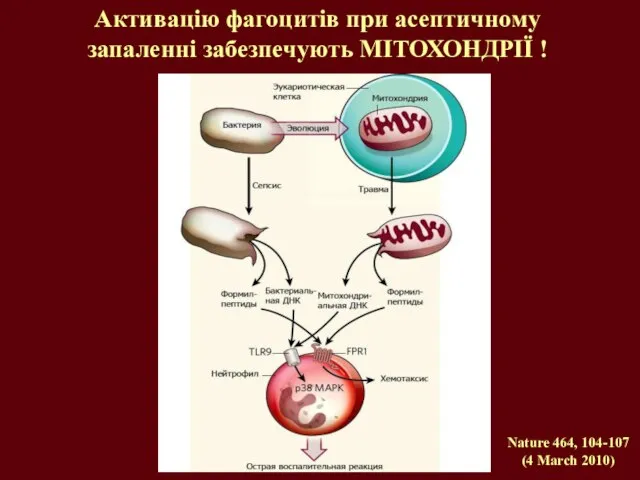
- 25. Активацію фагоцитів при асептичному запаленні забезпечують МІТОХОНДРІЇ ! Nature 464, 104-107 (4 March 2010)
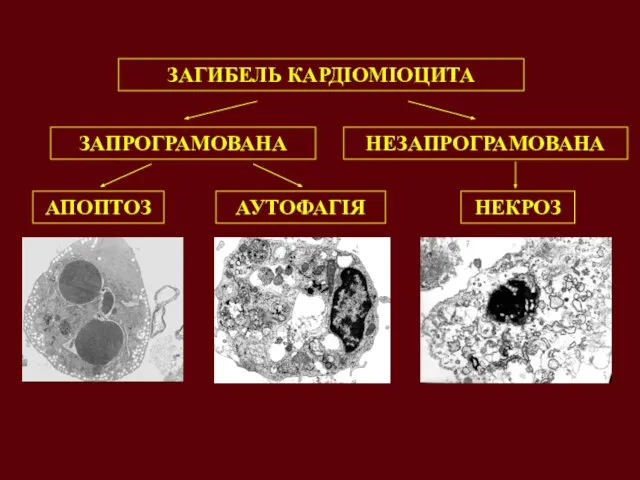
- 27. ЗАГИБЕЛЬ КАРДІОМІОЦИТА ЗАПРОГРАМОВАНА НЕЗАПРОГРАМОВАНА АПОПТОЗ АУТОФАГІЯ НЕКРОЗ
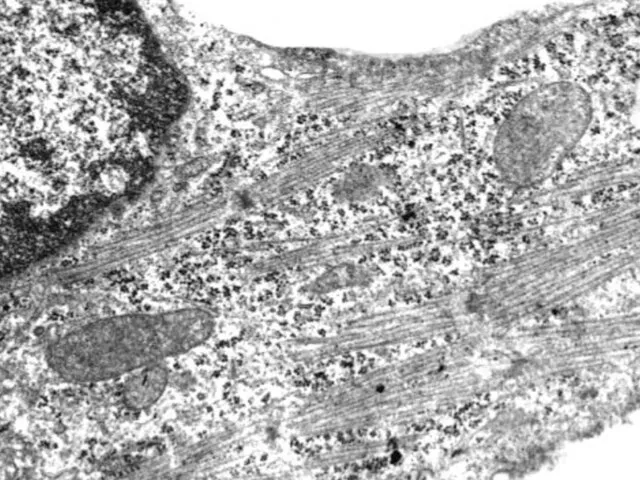
- 28. НЕОНАТАЛЬНИЙ КАРДІОМІОЦИТ ЩУРА ПІСЛЯ 24 ГОДИН КУЛЬТИВУВАННЯ
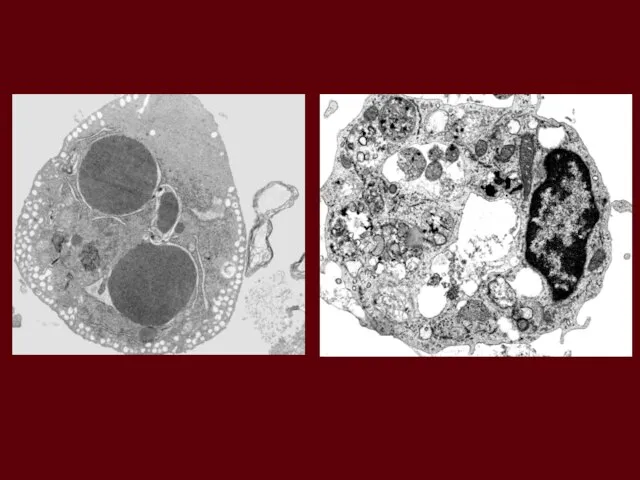
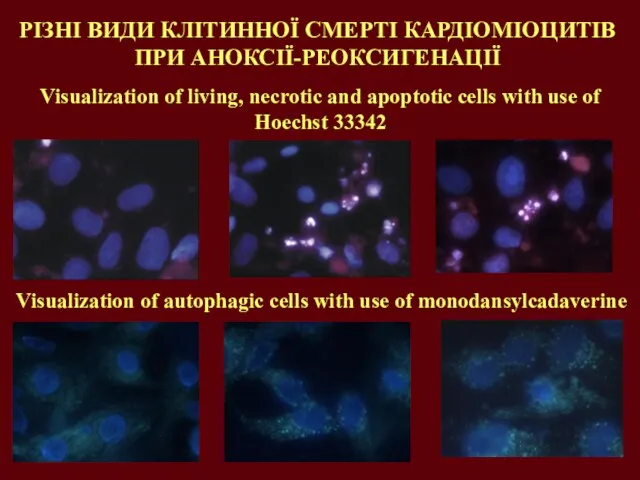
- 31. РІЗНІ ВИДИ КЛІТИННОЇ СМЕРТІ КАРДІОМІОЦИТІВ ПРИ АНОКСІЇ-РЕОКСИГЕНАЦІЇ Visualization of living, necrotic and apoptotic cells with use
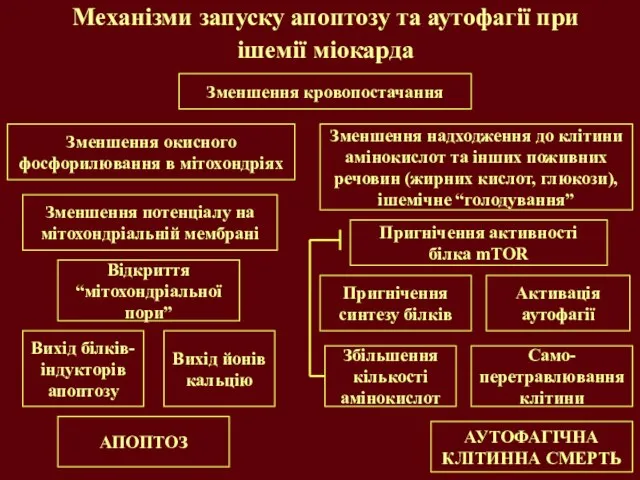
- 32. Механізми запуску апоптозу та аутофагії при ішемії міокарда Зменшення кровопостачання Зменшення надходження до клітини амінокислот та
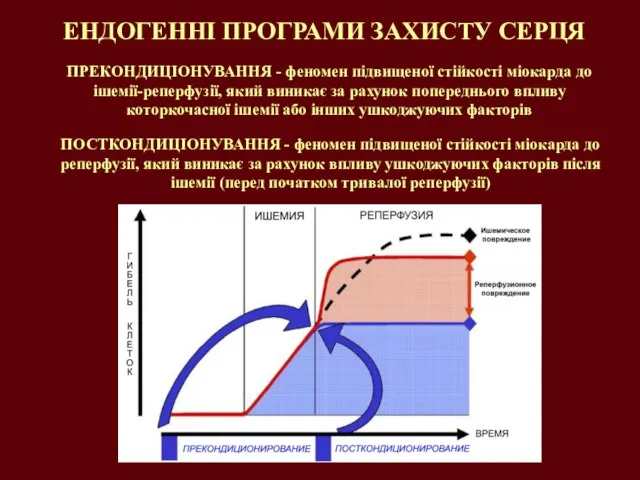
- 33. ЕНДОГЕННІ ПРОГРАМИ ЗАХИСТУ СЕРЦЯ ПРЕКОНДИЦІОНУВАННЯ - феномен підвищеної стійкості міокарда до ішемії-реперфузії, який виникає за рахунок
- 34. Хімічні – засоби для інгаляційного наркозу (десфлуран, ізофлуран, галотан), опіати, інгібітори протеасоми активатори АТФ-чутливих калієвих каналів
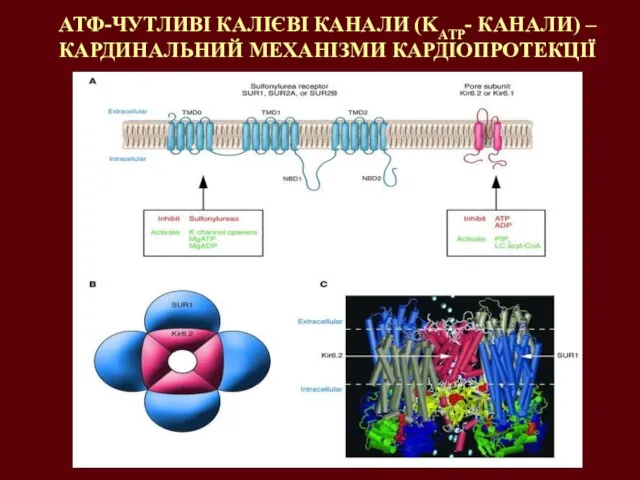
- 35. АТФ-ЧУТЛИВІ КАЛІЄВІ КАНАЛИ (KATP- КАНАЛИ) – КАРДИНАЛЬНИЙ МЕХАНІЗМИ КАРДІОПРОТЕКЦІЇ
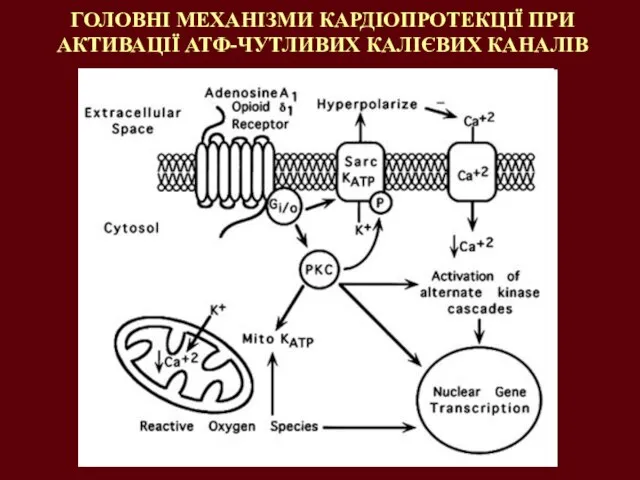
- 36. ГОЛОВНІ МЕХАНІЗМИ КАРДІОПРОТЕКЦІЇ ПРИ АКТИВАЦІЇ АТФ-ЧУТЛИВИХ КАЛІЄВИХ КАНАЛІВ
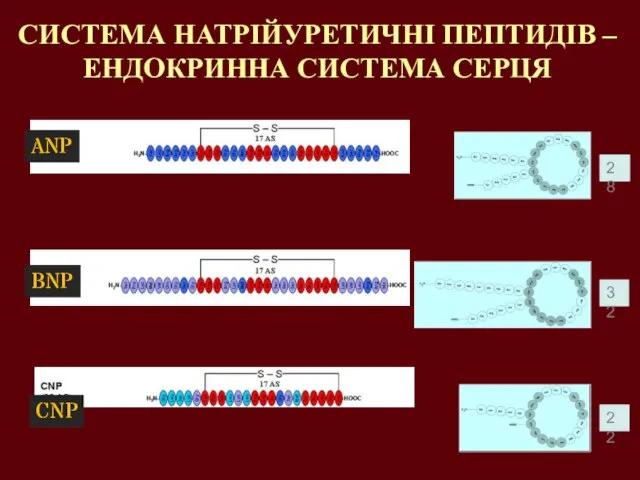
- 37. ANP BNP CNP 28 22 32 СИСТЕМА НАТРІЙУРЕТИЧНІ ПЕПТИДІВ – ЕНДОКРИННА СИСТЕМА СЕРЦЯ
- 38. ЕФЕКТИ NPS ВПЛИВ НА НИРКИ натрійурезу; діурезу; швидкості клубочкової фільтрації; кровообігу нирок. ВПЛИВ НА СЕРЦЕ Негативний
- 39. О.О.Мойбенко
- 41. Скачать презентацию












 Презентация "FERRY LINE IZMAYL - TULCEA" - скачать презентации по Экономике
Презентация "FERRY LINE IZMAYL - TULCEA" - скачать презентации по Экономике Проблемы правового регулирования рекламы в сети Интернет
Проблемы правового регулирования рекламы в сети Интернет Электронные платежные системы в Интернет и их особенности. Выполнил: Студент 3 курса (ШФ) ЮРГИ Факультет «Прикладная информатика
Электронные платежные системы в Интернет и их особенности. Выполнил: Студент 3 курса (ШФ) ЮРГИ Факультет «Прикладная информатика Муниципальное бюджетное дошкольное образовательное учреждение
Муниципальное бюджетное дошкольное образовательное учреждение  Складнопідрядні речення з кількома підрядними
Складнопідрядні речення з кількома підрядними Лекция 10. Международные и региональные валютно-кредитные
Лекция 10. Международные и региональные валютно-кредитные  АЛГЕБРА, 8 класс Тема урока: «Квадратные уравнения» Если ты услышишь, что кто-то не любит математику, не верь. Её нельзя н
АЛГЕБРА, 8 класс Тема урока: «Квадратные уравнения» Если ты услышишь, что кто-то не любит математику, не верь. Её нельзя н JavaScript安全 从浏览器到服务端 余弦
JavaScript安全 从浏览器到服务端 余弦 Языки программирования
Языки программирования Непрерывность функции в точке и на интервале
Непрерывность функции в точке и на интервале Казахстан в мировом сообществе. Внешняя политика Республики Казахстан
Казахстан в мировом сообществе. Внешняя политика Республики Казахстан ДИСКОНТИРОВАНИЕ мсфо
ДИСКОНТИРОВАНИЕ мсфо  Зима 2017. Издания книг
Зима 2017. Издания книг Система «человек - социальная среда
Система «человек - социальная среда Анкетирование. Опросный лист, его логика и структура
Анкетирование. Опросный лист, его логика и структура Понятие записи
Понятие записи Уголовно-правовые аспекты противодействия незаконному перемещению через границу объектов дикой флоры и фауны Курамшина Ольга
Уголовно-правовые аспекты противодействия незаконному перемещению через границу объектов дикой флоры и фауны Курамшина Ольга  Аттестационная работа. Совершенствование и проектирование ранее изученных элементов техники акробатических упражнений
Аттестационная работа. Совершенствование и проектирование ранее изученных элементов техники акробатических упражнений Гражданские правоотношения. (Лекция 6)
Гражданские правоотношения. (Лекция 6) Уильям Риверс
Уильям Риверс Why are family holidays important
Why are family holidays important Урок математики 1 класс
Урок математики 1 класс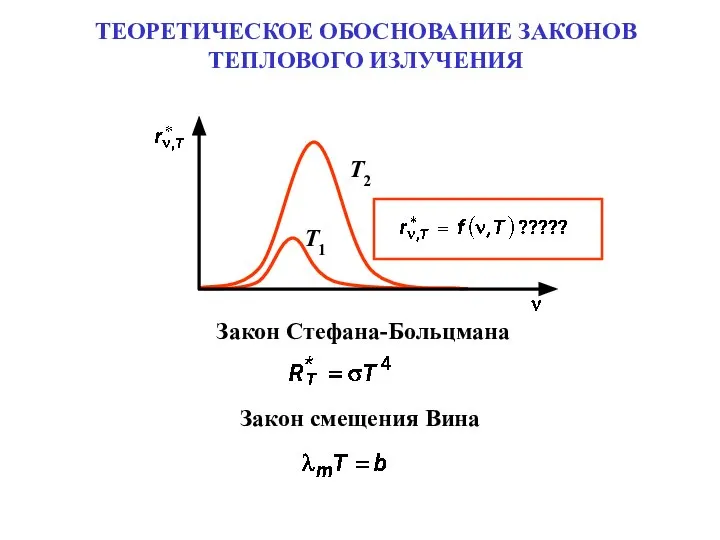 ТЕОРЕТИЧЕСКОЕ ОБОСНОВАНИЕ ЗАКОНОВ ТЕПЛОВОГО ИЗЛУЧЕНИЯ
ТЕОРЕТИЧЕСКОЕ ОБОСНОВАНИЕ ЗАКОНОВ ТЕПЛОВОГО ИЗЛУЧЕНИЯ Точность деталей сборочных единиц изделий
Точность деталей сборочных единиц изделий Інженерна підготовка і благоустрій територій населених пунктів із несприятливими природніми умовами
Інженерна підготовка і благоустрій територій населених пунктів із несприятливими природніми умовами Прогнозирование прибыли и рентабельности. УЭФ-Л 12-13
Прогнозирование прибыли и рентабельности. УЭФ-Л 12-13 Якими якостями повинна володти людина
Якими якостями повинна володти людина Спортивная медицина
Спортивная медицина