Содержание
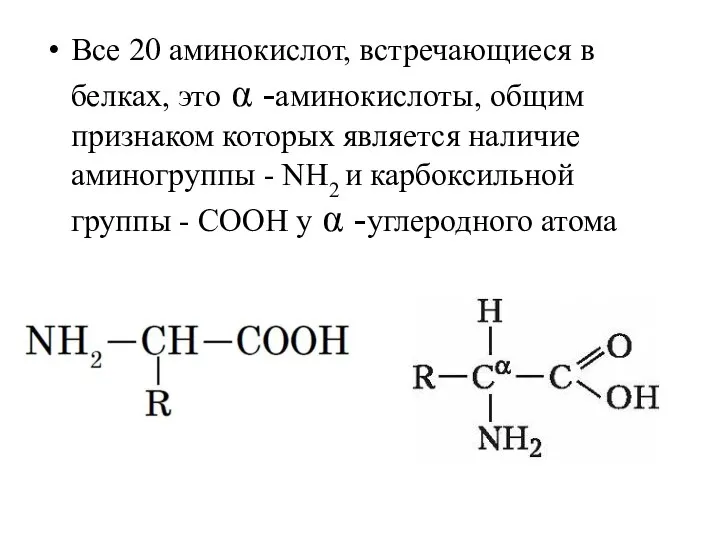
- 2. Все 20 аминокислот, встречающиеся в белках, это α -аминокислоты, общим признаком которых является наличие аминогруппы -
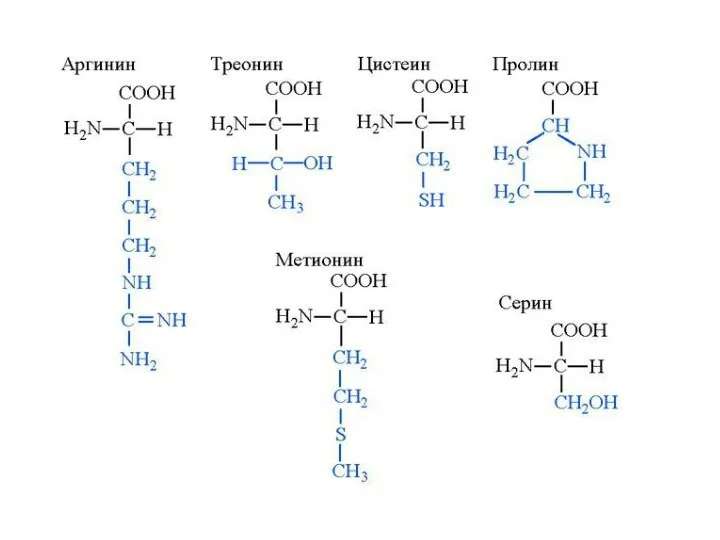
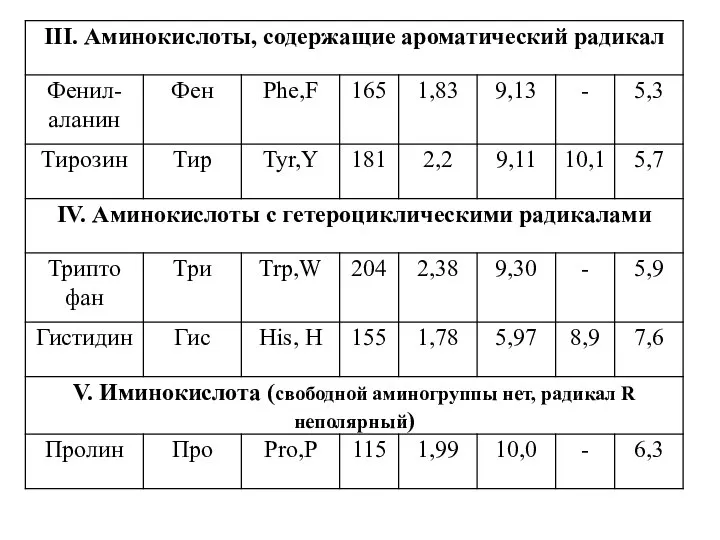
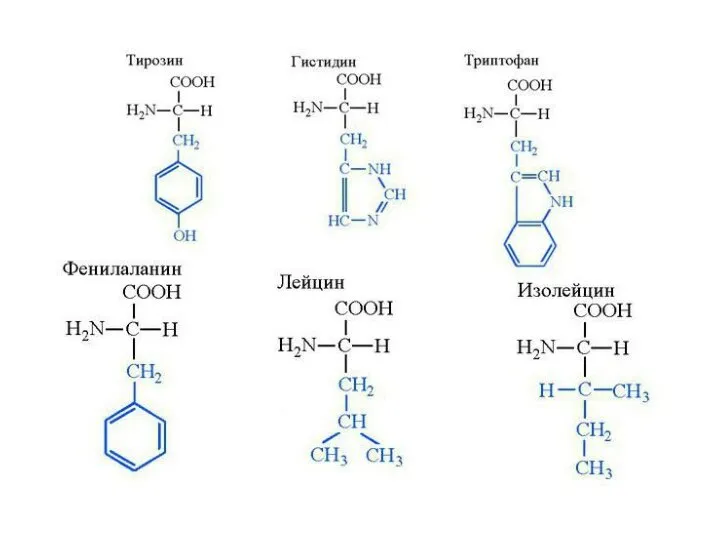
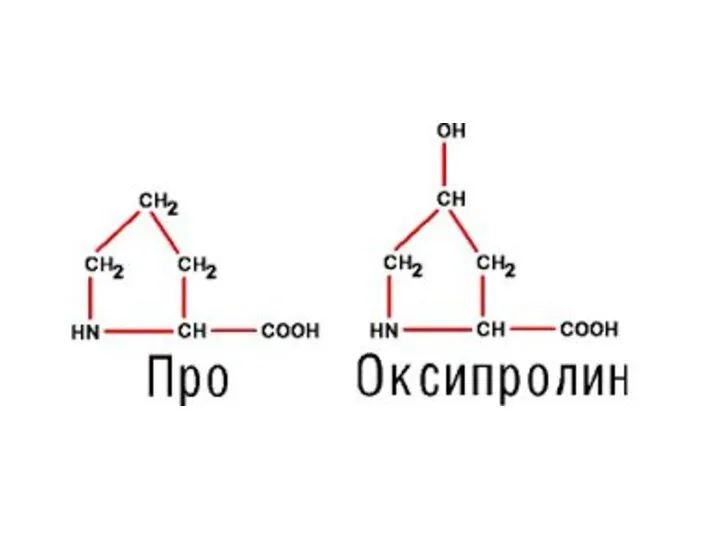
- 3. КЛАССИФИКАЦИЯ АМИНОКИСЛОТ ПО ХИМИЧЕСКОМУ СТРОЕНИЮ По химическому строению аминокислоты можно разделить на алифатические, ароматические и гетероциклические.
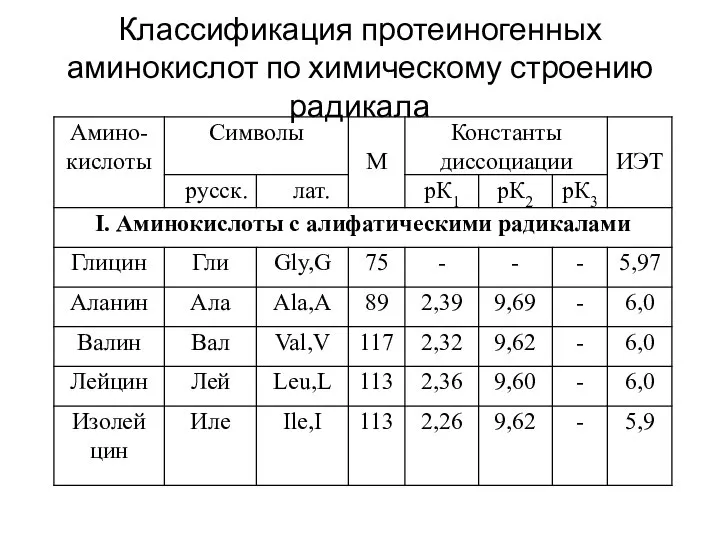
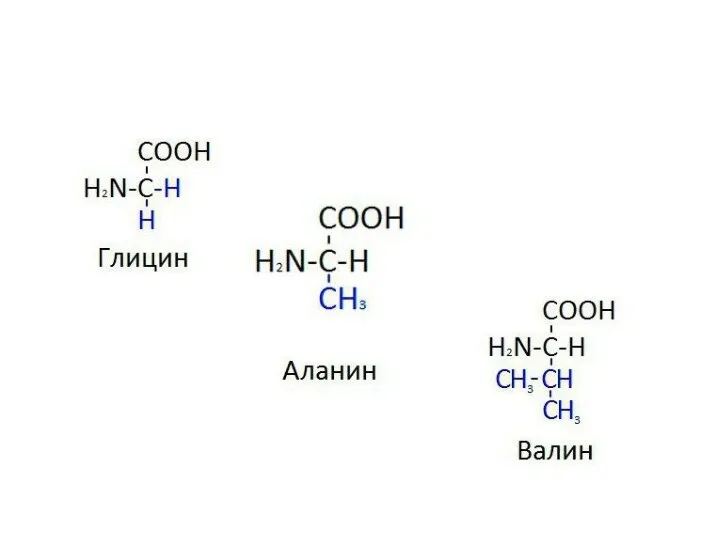
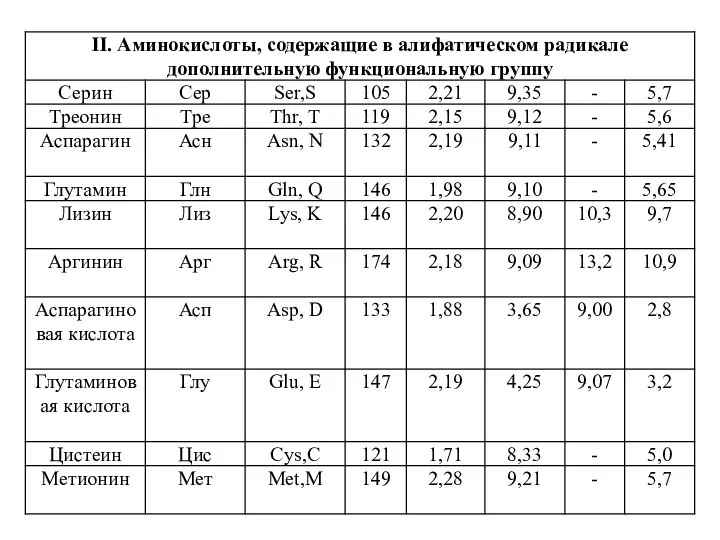
- 4. Классификация протеиногенных аминокислот по химическому строению радикала
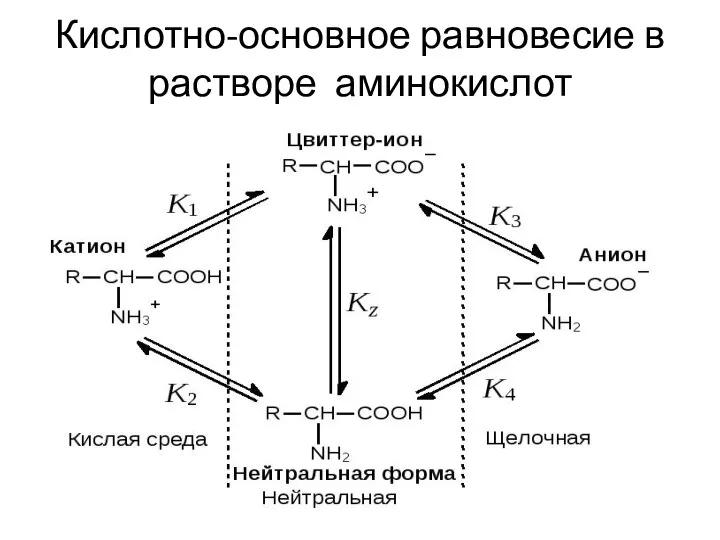
- 11. Кислотно-основное равновесие в растворе аминокислот
- 12. В природе известно более 100 аминокислот, из них 20 являются жизненно необходимыми. По способности синтезироваться в
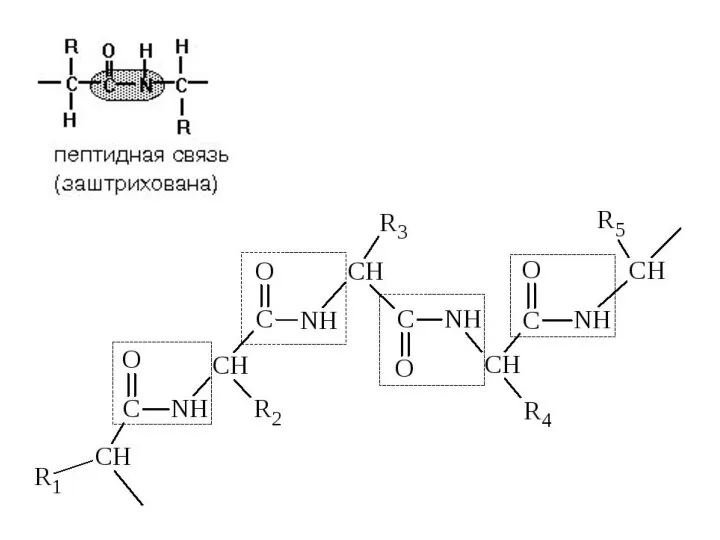
- 13. ПЕПТИДНАЯ СВЯЗЬ. СТРОЕНИЕ ПЕПТИДОВ α-Аминокислоты могут ковалентно связываться друг с другом с помощью пептидных связей. Пептидная
- 14. СТРОЕНИЕ ПЕПТИДА Количество аминокислот в составе пептидов может сильно варьировать. Пептиды, содержащие до 10 аминокислот, называют
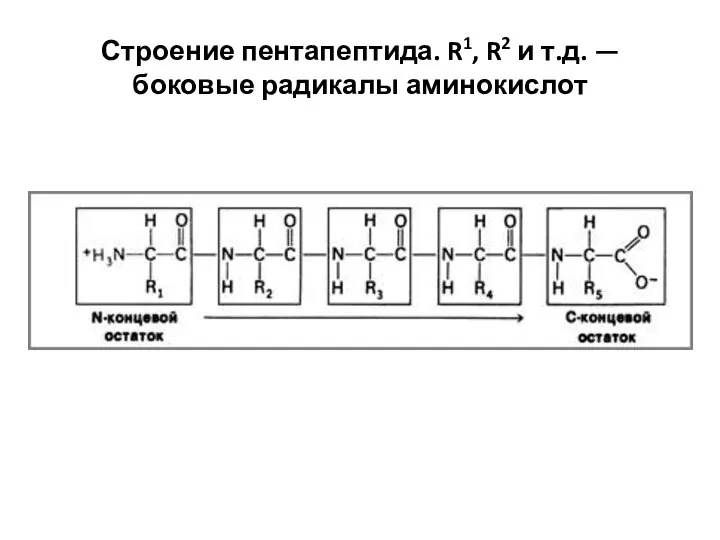
- 16. Строение пентапептида. R1, R2 и т.д. — боковые радикалы аминокислот
- 17. Белки - высокомолекулярные биополимеры, построенные из остатков аминокислот. Они составляют структурную и функциональную основу любого организма.
- 18. 5. Сократительная – белки мышц (актин, миозин, актомиозин) обеспечивают сокращение и расслабление мышц 6. Энергетическая –
- 19. Физико-химические и функциональные особенности белков Белки в среднем составляют 18-24% общей сырой массы организма и до
- 20. Сходство: медленность диффузии, неспособность к диализу, размер частиц. Различия: растворы ВМС – гомогенны, не имеют поверхности
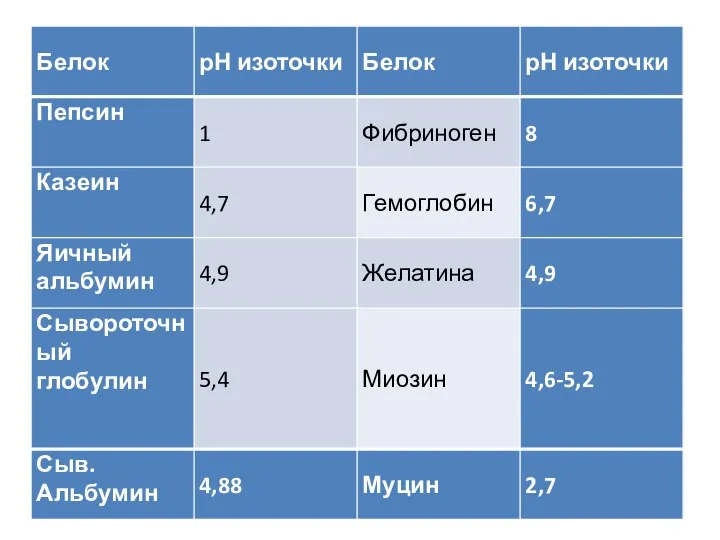
- 21. При определенной для каждого белка концентрации водородных ионов в молекуле белка устанавливается равенство положительных и отрицательных
- 23. В изоточке белок менее гидратирован, уменьшается его растворимость, он легче выпадает в осадок. Растворы ВМС устойчивы
- 24. Кроме явления коагуляции в растворах ВМС наблюдается при определенных условиях явление расслоения, при котором раствор ВМС
- 25. Одним из важнейших свойств белков, как лиофильных коллоидов, является их способность задерживать большое количество воды –
- 26. Все белки по форме молекул делят на фибриллярные и глобулярные. Фибриллярные (фибриллиа – волокно, лат.). Длина
- 27. Свойства глобулярных фибриллярных различны. Глобулярные растворимы в воде и в разбавленных солевых растворах. Фибриллярные в воде
- 28. Белки - это высокомолекулярные соединения (полимеры), состоящие из α -аминокислот - мономерных звеньев, соединенных между собой
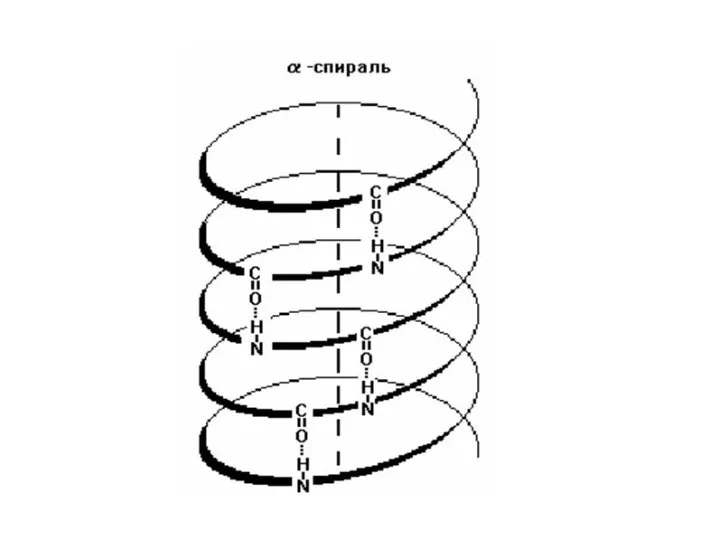
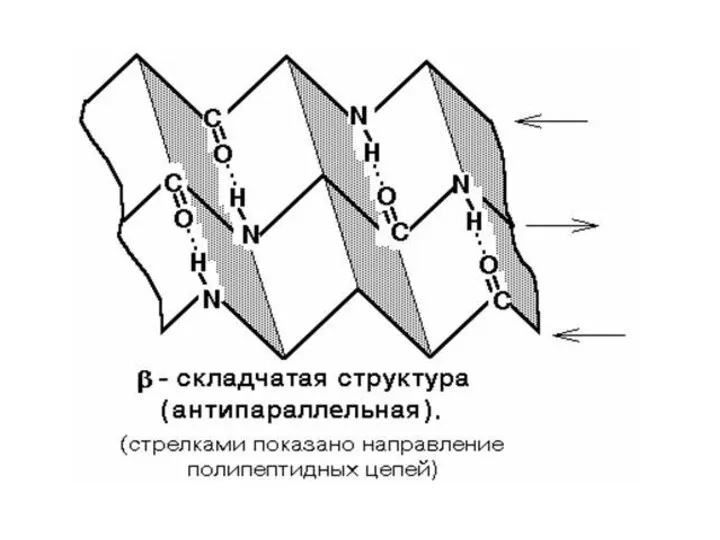
- 29. Первичная структура – это линейная последовательность аминокислотных остатков в полипептидной цепи. Вторичная структура белков – это
- 32. Третичная структура белка – это трехмерная пространственная структура, образующаяся за счет взаимодействий между радикалами аминокислот, которые
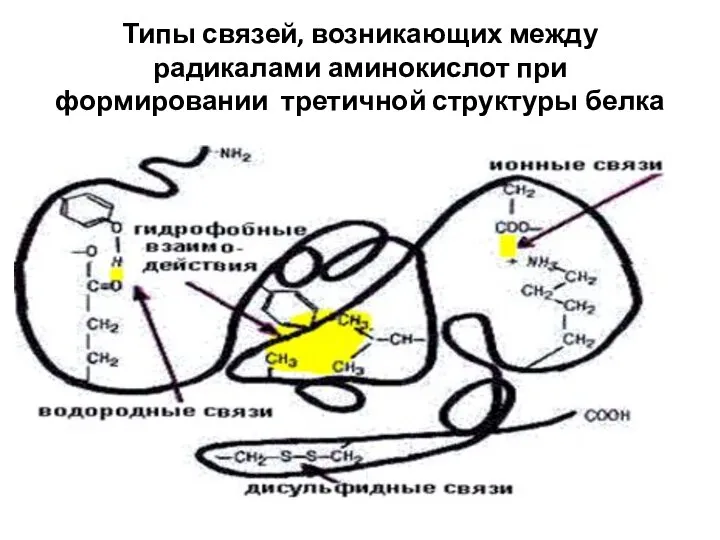
- 33. СВЯЗИ, СТАБИЛИЗИРУЮЩИЕ ТРЕТИЧНУЮ СТРУКТУРУ ГЛОБУЛЯРНОГО БЕЛКА Электростатические силы притяжения между R-группами, несущими противоположно заряженные ионогенные группы
- 34. Типы связей, возникающих между радикалами аминокислот при формировании третичной структуры белка
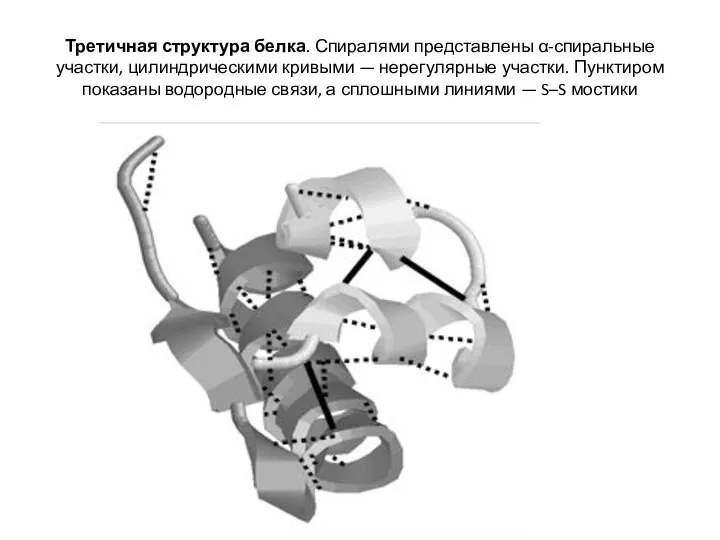
- 35. Третичная структура белка. Спиралями представлены α-спиральные участки, цилиндрическими кривыми — нерегулярные участки. Пунктиром показаны водородные связи,
- 36. ПРОСТРАНСТВЕННАЯ ЧЕТВЕРТИЧНАЯ СТРУКТУРА Ассоциация и взаиморасположение полипептидных цепей в пространстве называют «четвертичная структура белков». Отдельные полипептидные
- 37. Четвертичная структура гемоглобина
- 38. ДЕНАТУРАЦИЯ БЕЛКОВ И ПОДДЕРЖАНИЕ ИХ НАТИВНОЙ КОНФОРМАЦИИ В УСЛОВИЯХ КЛЕТКИ Денатурация белков – это разрушение их
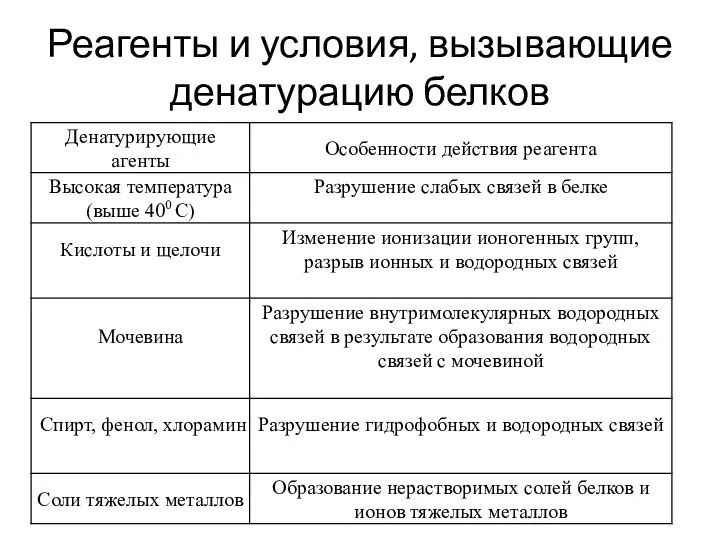
- 39. Реагенты и условия, вызывающие денатурацию белков
- 40. Денатурирующие агенты не разрушают первичную структуру белка. Сохранность первичной структуры белка - необходимое условие для восстановления
- 42. Скачать презентацию






















 Виртуальный режим
Виртуальный режим Нормы литературного языка
Нормы литературного языка Преступность и ее основные характеристики
Преступность и ее основные характеристики Аттестационная работа. Творческий проект: Кукла-столбушка в русском народном костюме
Аттестационная работа. Творческий проект: Кукла-столбушка в русском народном костюме ПРОФИЛЬНОЕ ОБУЧЕНИЕ – ВОПРОСЫ И ОТВЕТЫ
ПРОФИЛЬНОЕ ОБУЧЕНИЕ – ВОПРОСЫ И ОТВЕТЫ Презентация Соглашение СМГС
Презентация Соглашение СМГС Волинські Вконтакте
Волинські Вконтакте Благовещение Пресвятой Богородицы
Благовещение Пресвятой Богородицы Хронический холецистит, дисфункция желчного пузыря, Спазм сфинктера одди, хронческий панкреатит
Хронический холецистит, дисфункция желчного пузыря, Спазм сфинктера одди, хронческий панкреатит  Восточно-Азиатские системы государства и права
Восточно-Азиатские системы государства и права Борьба судьи Самсона с филистимлянами. Книга Руфь. Общее введение в книги Царств
Борьба судьи Самсона с филистимлянами. Книга Руфь. Общее введение в книги Царств Денсаулық сақтау саласындағы. Қауіп менеджменті
Денсаулық сақтау саласындағы. Қауіп менеджменті Настольный теннис. Основные правила игры
Настольный теннис. Основные правила игры Конструкции одноэтажных промышленных зданий
Конструкции одноэтажных промышленных зданий Круговорот веществ и превращение энергии в экосистеме
Круговорот веществ и превращение энергии в экосистеме Спрос, предложение и рыночное равновесие
Спрос, предложение и рыночное равновесие Футбольные фанаты
Футбольные фанаты Тема 8 Национальная экономика: результаты и измерения Вопросы: Мера экономического успеха в современных обществах Система
Тема 8 Национальная экономика: результаты и измерения Вопросы: Мера экономического успеха в современных обществах Система  Політичний устрій та соціально-економічний розвиток Руської держави
Політичний устрій та соціально-економічний розвиток Руської держави Дискуссия о роли «итальянской» и «французской» школ в становлении современной дипломатии 1
Дискуссия о роли «итальянской» и «французской» школ в становлении современной дипломатии 1 Воспитание общей выносливости у пловцов 12-14 лет С ДЦП
Воспитание общей выносливости у пловцов 12-14 лет С ДЦП Тормозная система КамАЗ
Тормозная система КамАЗ Презентация на тему "Гражданское право и гражданские правоотношения" - скачать презентации по Педагогике
Презентация на тему "Гражданское право и гражданские правоотношения" - скачать презентации по Педагогике Искусство 20 века
Искусство 20 века Регулируемый электропривод подачи токарного станка
Регулируемый электропривод подачи токарного станка 3.3. Инструменты управления конкурентоспособностью
3.3. Инструменты управления конкурентоспособностью Программирование на языке Паскаль
Программирование на языке Паскаль Патология эндокринной системы
Патология эндокринной системы