Содержание
- 2. Окисление – это химическая реакция, включающая потерю атомом или молекулой одного или более электронов. Всегда является
- 3. Биологическое окисление – это совокупность реакций окисления, направленных на обеспечение организма энергией в доступной для использования
- 4. Все три типа реакций имеют место в живой клетке. Если акцептором водорода в реакциях дегидрирования служит
- 5. История развития учения о биоокислении 1) Антуан Лоран Лавуазье (1743—1794), французский химик. указал на то, что
- 6. 2) Теория А.Н.Баха – «теория активации кислорода» или «перекисная теория» Алексей Николаевич Бах (1857-1946) Согласно теории
- 7. По Баху, окислительные ферменты оксидазы состоят из самоокисляющихся веществ, которые, присоединяя кислород воздуха, образуют перекисеобразные соединения.
- 8. В дальнейшем оказалось, что действительно в клетках существует ферменты, способные активировать молекулярный кислород и использовать его
- 9. 3) Теория В.И. Палладина – «теория активации водорода» Владимир Иванович Палладин (1859-1922) По теории В.И. Палладина,
- 10. Основные положения теории Палладина: 1. Непременным участником дыхания является вода. 2. Вода наряду с окисляемым субстратом
- 11. Впоследствии теория В.И. Палладина подтвердилась для процессов митохондриального окисления, а ферменты, принимающие непосредственное участие в отнятии
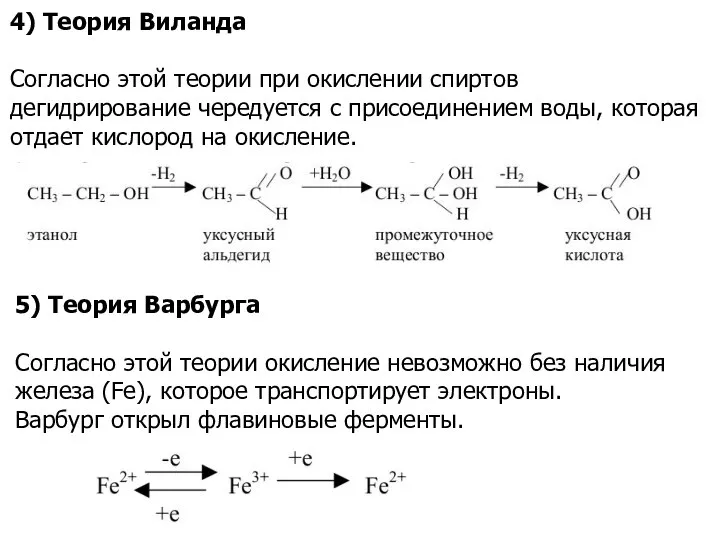
- 13. 4) Теория Виланда Согласно этой теории при окислении спиртов дегидрирование чередуется с присоединением воды, которая отдает
- 14. 6) В 30-х годах Энгельгардт наблюдал, что при тканевом дыхании накапливаются молекулы АТФ, т.е. показал связь
- 15. Ферменты и коферменты, участвующие в биологическом окислении Перенос электронов от окисляемых субстратов к кислороду происходит в
- 16. Первичные акцепторы водорода Первичные акцепторы водорода окислительно-восстановительных реакций относят к 2 типам дегидрогеназ: никотинамидзависимым, содержащим в
- 17. Никотинамидзависимые дегидрогеназы содержат в качестве коферментов NAD+ или NADP+. NAD+ и NADP+ - производные витамина PP.
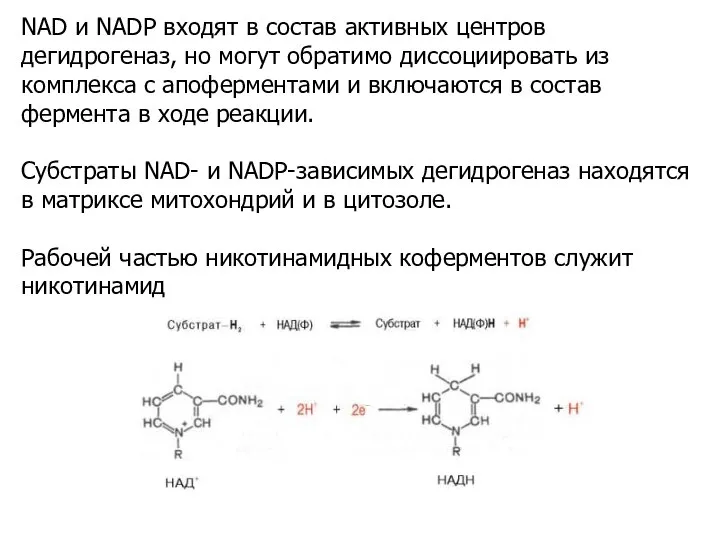
- 18. NAD и NADP входят в состав активных центров дегидрогеназ, но могут обратимо диссоциировать из комплекса с
- 19. Большинство дегидрогеназ, поставляющих электроны в ЭТЦ, содержат NAD+. Они катализируют реакции типа: R-CHOH-R1 + NAD+↔ R-CO-R1
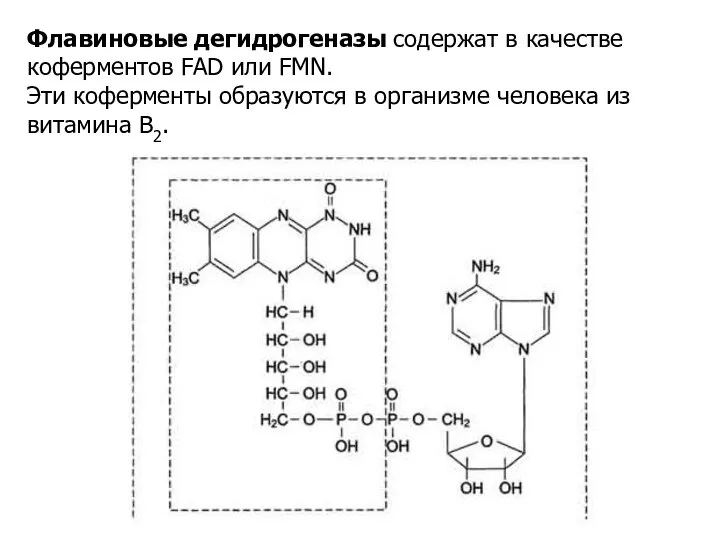
- 20. Флавиновые дегидрогеназы содержат в качестве коферментов FAD или FMN. Эти коферменты образуются в организме человека из
- 21. Флавиновые коферменты прочно связаны с апоферментами. Рабочей частью FAD и FMN служит изоаллоксазиновая сопряжённая циклическая система:
- 22. FAD служит акцептором электронов от многих субстратов в реакциях типа: R-CH2-CH2-R1 + Е (FAD) ↔ R-CH=CH-R1
- 24. Скачать презентацию


















 Презентация на тему "Традиционная медицина Руси" - скачать презентации по Медицине
Презентация на тему "Традиционная медицина Руси" - скачать презентации по Медицине Модель безопасности рабочего места
Модель безопасности рабочего места Интерфейс RS-232
Интерфейс RS-232 ТИПОЛОГИЯ ПОЛИТИЧЕСКИХ СИСТЕМ. Выполнили: студенты 3-го курса Группы Ю-101 Меженько Юлия Шевцова Екатерина
ТИПОЛОГИЯ ПОЛИТИЧЕСКИХ СИСТЕМ. Выполнили: студенты 3-го курса Группы Ю-101 Меженько Юлия Шевцова Екатерина Индивидуальные занятия по развитию слухового восприятия и обучения
Индивидуальные занятия по развитию слухового восприятия и обучения  Эмпедокл (490-430 до н.э.)
Эмпедокл (490-430 до н.э.) Урок развития речи. Сочинение-рассказ о произведениях народного промысла
Урок развития речи. Сочинение-рассказ о произведениях народного промысла Дресс-Код
Дресс-Код ПЕРВЫЕ ШАГИ ПРИ УСТРОЙСТВЕ НА РАБОТУ Информационно-правовой практикум 11 класс Земель Л.С. Мананникова Н.Н.
ПЕРВЫЕ ШАГИ ПРИ УСТРОЙСТВЕ НА РАБОТУ Информационно-правовой практикум 11 класс Земель Л.С. Мананникова Н.Н.  Керамика Латинской Америки
Керамика Латинской Америки Управление программами и портфелями проектов
Управление программами и портфелями проектов Волейбол
Волейбол  Выпиливание лобзиком
Выпиливание лобзиком AUATSS labojums
AUATSS labojums Съезд Родной партии РФ
Съезд Родной партии РФ Покупайте и коллекционируйте картины студентов лучших художественных ВУЗов по фиксированной цене
Покупайте и коллекционируйте картины студентов лучших художественных ВУЗов по фиксированной цене Психологические школы .
Психологические школы .  Операционная система предприятия
Операционная система предприятия Дисперсии «Лакротэн» в водоосновных ЛКМ для печати по ДВП Оргхимпром Производство акриловых дисперсий
Дисперсии «Лакротэн» в водоосновных ЛКМ для печати по ДВП Оргхимпром Производство акриловых дисперсий  Презентация «РЕНТА И ПОЖИЗНЕННОЕ СОДЕРЖАНИЕ С ИЖДИВЕНИЕМ»
Презентация «РЕНТА И ПОЖИЗНЕННОЕ СОДЕРЖАНИЕ С ИЖДИВЕНИЕМ» Два лица Кореи
Два лица Кореи Проект реконструкции и озеленения территории МКОУ Бутурлиновская ООШ № 9 г. Бутурлиновка Воронежской области
Проект реконструкции и озеленения территории МКОУ Бутурлиновская ООШ № 9 г. Бутурлиновка Воронежской области Работа или удовольствие – зачем выбирать
Работа или удовольствие – зачем выбирать Чемпионат мира по футболу 2006 и его эффект на имидж и экономику Германии
Чемпионат мира по футболу 2006 и его эффект на имидж и экономику Германии Лексер. Парсер. (Часть 2)
Лексер. Парсер. (Часть 2) Пейзаж. Часть 1
Пейзаж. Часть 1 Этические принципы и юридическая ответственность психолога
Этические принципы и юридическая ответственность психолога Переговоры и этикет
Переговоры и этикет