Содержание
- 2. 09/02/2023 Коваль А. Н., 2006 (C) Общие свойства Аминокислоты (АК) обычно содержат карбоксильную группу (COOH), аминогруппу
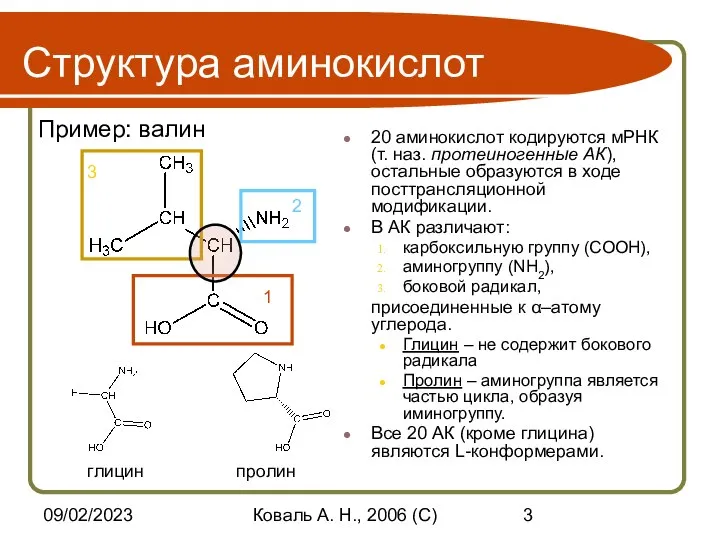
- 3. 09/02/2023 Коваль А. Н., 2006 (C) Структура аминокислот 20 аминокислот кодируются мРНК (т. наз. протеиногенные АК),
- 4. 09/02/2023 Коваль А. Н., 2006 (C) Классификация аминокислот По боковому радикалу: Гидрофобные АК – способны к
- 5. 09/02/2023 Коваль А. Н., 2006 (C) Заряды аминокислот Заряды α–аминогрупп и α–карбоксильных групп Заряды боковых радикалов
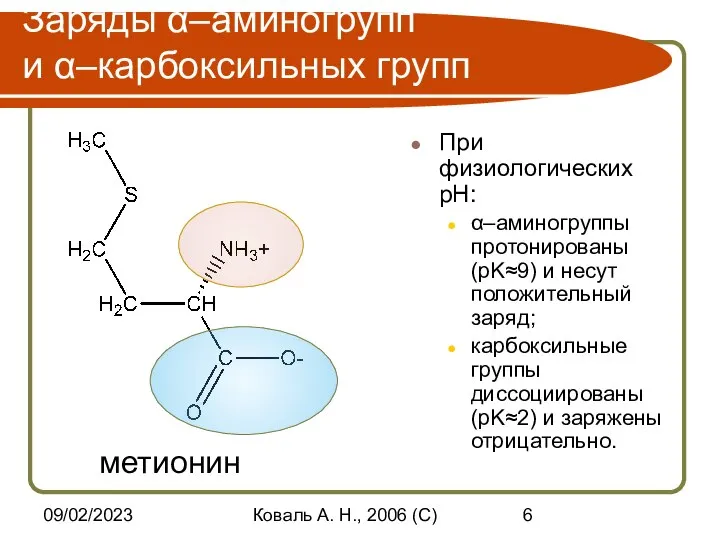
- 6. 09/02/2023 Коваль А. Н., 2006 (C) Заряды α–аминогрупп и α–карбоксильных групп При физиологических pH: α–аминогруппы протонированы
- 7. 09/02/2023 Коваль А. Н., 2006 (C) Заряды боковых радикалов Положительные заряды Боковые радикалы основных аминокислот –
- 8. 09/02/2023 Коваль А. Н., 2006 (C) Заряды боковых радикалов Отрицательные заряды Боковые радикалы кислых АК -
- 9. 09/02/2023 Коваль А. Н., 2006 (C) Изоэлектрическая точка (pI) Изоэлектрическая точка (pI) – это значение pH,
- 10. 09/02/2023 Коваль А. Н., 2006 (C) Определение заряда пептидов при различных pH Особенности пептидов: В них
- 11. Пример расчета зарядов пептида при различных pH
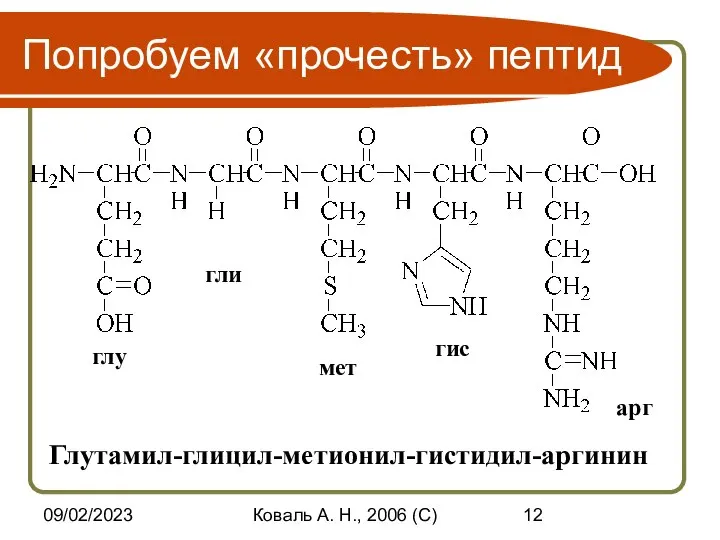
- 12. 09/02/2023 Коваль А. Н., 2006 (C) Попробуем «прочесть» пептид глу гли мет гис арг Глутамил-глицил-метионил-гистидил-аргинин
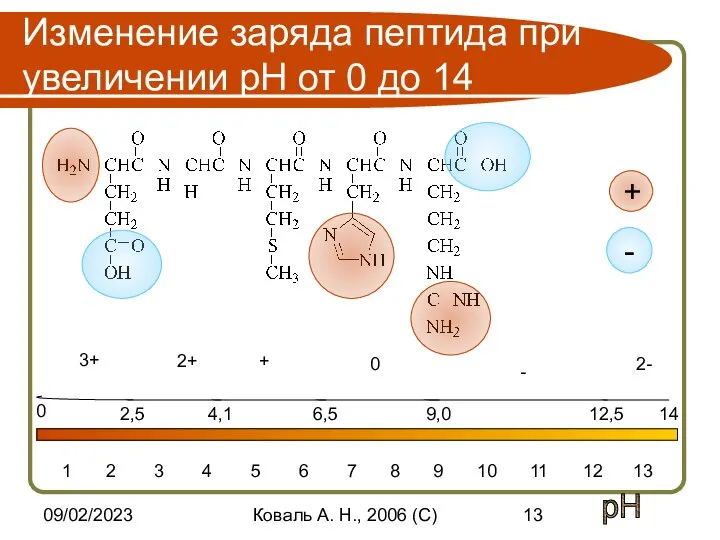
- 13. 09/02/2023 Коваль А. Н., 2006 (C) Изменение заряда пептида при увеличении pH от 0 до 14
- 14. 09/02/2023 Коваль А. Н., 2006 (C)
- 15. 09/02/2023 Коваль А. Н., 2006 (C)
- 16. 09/02/2023 Коваль А. Н., 2006 (C)
- 17. 09/02/2023 Коваль А. Н., 2006 (C)
- 18. 09/02/2023 Коваль А. Н., 2006 (C)
- 19. 09/02/2023 Коваль А. Н., 2006 (C)
- 20. 09/02/2023 Коваль А. Н., 2006 (C)
- 22. Скачать презентацию








 Поведінка будівельних конструкцій під час пожежі
Поведінка будівельних конструкцій під час пожежі Двумерные массивы. Задачи
Двумерные массивы. Задачи Национальные костюмы народов России
Национальные костюмы народов России School Uniforms in different countries
School Uniforms in different countries Амнистия. Помилование.Судимость.
Амнистия. Помилование.Судимость. Параметры конструкции, Х-величины. Лекция 10
Параметры конструкции, Х-величины. Лекция 10 Использование видео и аудио в HTML
Использование видео и аудио в HTML Презентация по алгебре Тригонометрические уравнения и методы их решения
Презентация по алгебре Тригонометрические уравнения и методы их решения  Тире между подлежащим и сказуемым 5 класс - презентация_
Тире между подлежащим и сказуемым 5 класс - презентация_ Tajemnice Światła
Tajemnice Światła Базовые алгоритмы обработки одномерных массивов
Базовые алгоритмы обработки одномерных массивов ПРЕЗЕНТАЦИЯ НА ТЕМУ: «Витамины, гормоны, лекарства.»
ПРЕЗЕНТАЦИЯ НА ТЕМУ: «Витамины, гормоны, лекарства.» Основные принципы проектирования энергоэффективных зданий
Основные принципы проектирования энергоэффективных зданий Instructed second language vocabulary learning
Instructed second language vocabulary learning Кислородцентрированные соединения
Кислородцентрированные соединения  Водный и Огненный лабиринты
Водный и Огненный лабиринты Технология приготовления блюд обеда для туристов из Белоруссии
Технология приготовления блюд обеда для туристов из Белоруссии Контроллинг в системе управления
Контроллинг в системе управления Культура Японии
Культура Японии Благоустройство зоны отдыха для проведения массовых мероприятий с. Уточка» в Утянском сельском поселении
Благоустройство зоны отдыха для проведения массовых мероприятий с. Уточка» в Утянском сельском поселении Физическая форма
Физическая форма Нормативно-правовые основы формирования системы дополнительного образования в ДОО
Нормативно-правовые основы формирования системы дополнительного образования в ДОО Symbol of Mongolia
Symbol of Mongolia Государственные закупки. Строительство зданий
Государственные закупки. Строительство зданий Методические рекомендации по использованию технологии Эдварда де Боно «Шесть шляп мышления».
Методические рекомендации по использованию технологии Эдварда де Боно «Шесть шляп мышления». Пейзажи Беларуси
Пейзажи Беларуси Динамические структуры данных (язык Си)
Динамические структуры данных (язык Си) Многоэтажный жилой дом (КП)
Многоэтажный жилой дом (КП)