Содержание
- 2. Зависимость константы скорости реакции от ионной силы раствора определяется соотношением Бренстеда — Бьеррума: , где k
- 3. Зависимость lg(kr/k0) от I1/2 для ионных реакций: [Со(NH3)5Br]2+ + Hg2+; СН2ВгСОО- + S2032-; СН2СlСОО- + ОН-;
- 4. Вторичный солевой эффект заключается в том, что внесенный электролит приводит к уменьшению коэффициентов активности слабых электролитов.
- 5. ХАРАКТЕРИСТИКИ ХИМИЧЕСКОГО ПРОЦЕССА: СТЕПЕНЬ ПРЕВРАЩЕНИЯ, СЕЛЕКТИВНОСТЬ, ВЫХОД ПРОДУКТА Первичной основой учения о химических превращениях является стехиометрия,
- 6. Мольные количества веществ ni удобны для характеристики периодических процессов. Для характеристики непрерывных процессов, когда вещества подают
- 7. СТЕХИОМЕТРИЯ РЕАКЦИЙ. МАТЕРИАЛЬНЫЕ РАСЧЕТЫ С точки зрения стехиометрии все химические реакции подразделяются на простые и сложные.
- 8. При этом стехиометрические коэффициенты расходуемых веществ берутся со знаком минус, а образующихся – со знаком плюс;
- 9. Пример. Пусть реакция диспропорционирования циклогексена с образованием бензола и циклогексана является простой, вычислить ni, если известно,
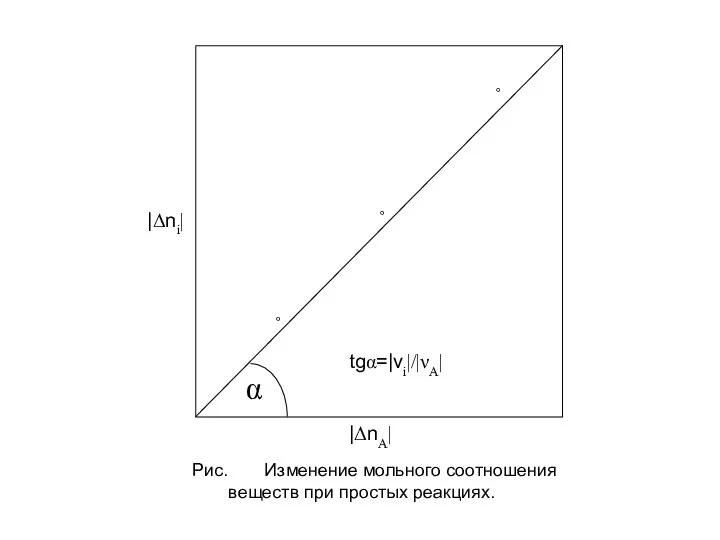
- 10. Из равенств К3 следует, что при простых реакциях мольное соотношение образующихся или расходуемых веществ постоянно и
- 11. Рис. Изменение мольного соотношения веществ при простых реакциях.
- 12. Сложные реакции состоят из ряда простых реакций. К ним принадлежат: обратимые реакции νAA + ... νBB
- 13. При анализе известной системы сложных реакций прежде всего необходимо определить число стехиометрически независимых превращений, уравнения которых
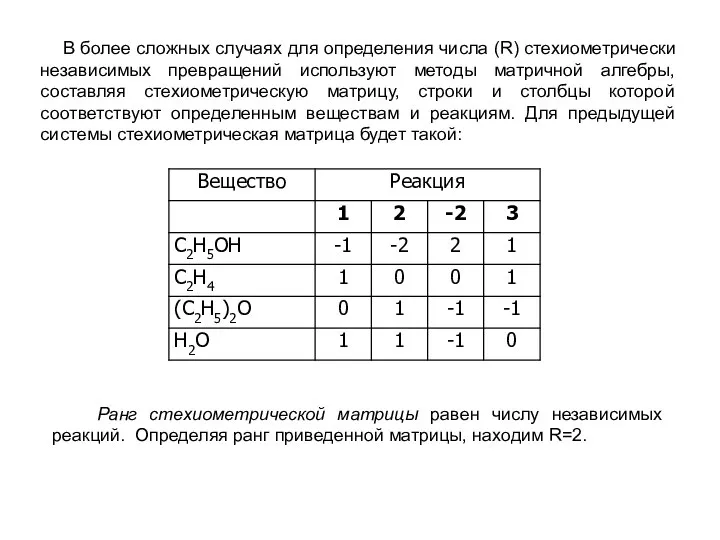
- 14. В более сложных случаях для определения числа (R) стехиометрически независимых превращений используют методы матричной алгебры, составляя
- 15. Одновременно с числом независимых реакций определяют равное ему число так называемых ключевых веществ, по которым можно
- 16. Тогда, имея в виду, что каждое из веществ может участвовать в нескольких реакциях (Δni=ΣΔnij), получим: ni
- 17. БЕЗРАЗМЕРНЫЕ ХАРАКТЕРИСТИКИ МАТЕРИАЛЬНОГО БАЛАНСА РЕАКЦИЙ В химии и технологии большое значение имеют безразмерные характеристики материального баланса:
- 18. В разных процессах химической технологии степень конверсии изменяется от 4 – 5 до почти 100 %.
- 19. где - абсолютное значение стехио-метрического коэффициента при А.
- 20. Для сложных реакций, имеющих более одного ключевого вещества, степень конверсии показывает лишь долю превращенного реагента, но
- 21. Тогда получим выражение для селективности: К9 в котором двойной индекс при Ф означает, что селективность определена
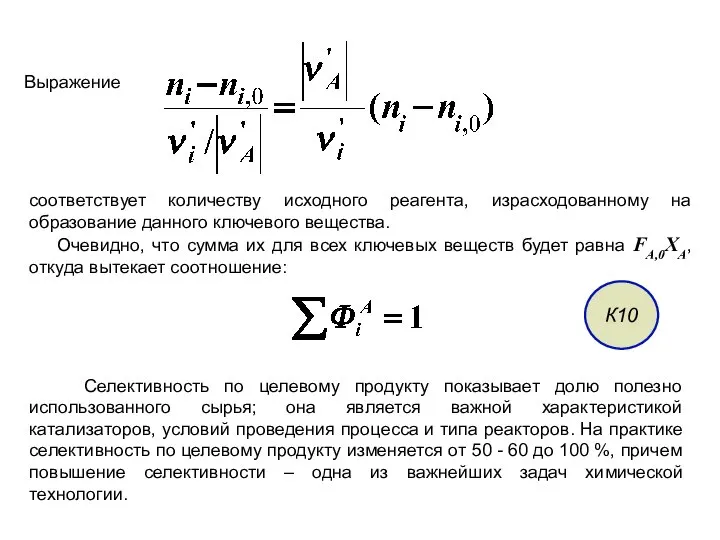
- 22. Выражение соответствует количеству исходного реагента, израсходованному на образование данного ключевого вещества. Очевидно, что сумма их для
- 23. Выход – это не однозначное понятие. Иногда под ним понимают абсолютное количество полученного продукта (в г,
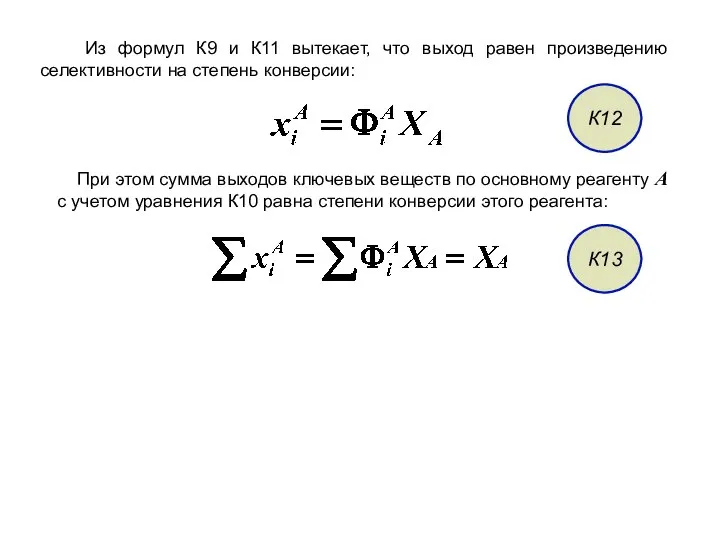
- 24. Из формул К9 и К11 вытекает, что выход равен произведению селективности на степень конверсии: При этом
- 25. Из уравнения К11 мольные количества или потоки продуктов можно выразить через их выходы: К14 К15 Последние
- 26. Парциальные молярные балансы. На безразмерных характеристиках реакций основаны расчеты так называемых парциальных молярных балансов, составляемых на
- 27. Величина (ΔFAj / FA,0) есть степень полноты или частная степень конверсии основного реагента по данной суммарной
- 28. КОНЦЕНТРАЦИИ, ПАРЦИАЛЬНЫЕ ДАВЛЕНИЯ И МОЛЬНЫЕ ДОЛИ Кроме мольных количеств или потоков веществ и безразмерных характеристик баланса
- 29. Нередко объем или объемный поток остаются постоянными во время реакции. Это типично для жидкофазных процессов, а
- 30. Более сложные соотношения существуют для реакций, протекающих с изменением объема. При жидкофазных процессах это бывает при
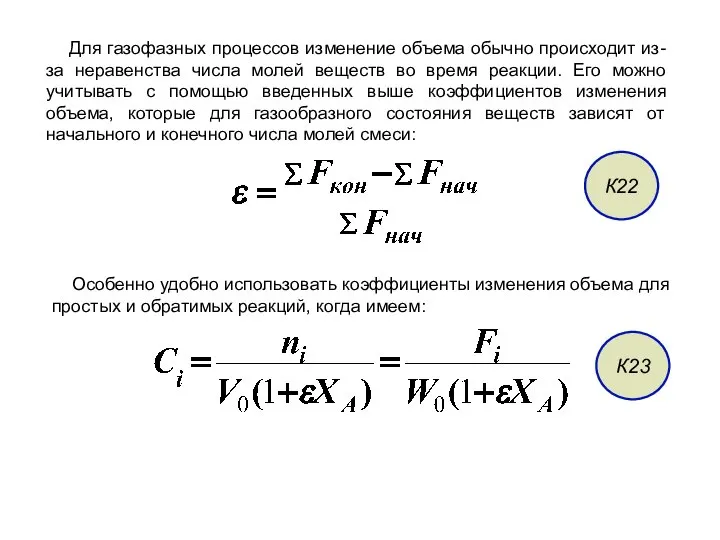
- 31. Для газофазных процессов изменение объема обычно происходит из-за неравенства числа молей веществ во время реакции. Его
- 32. При подстановке Fi как функции FA,0 и XA оказывается, что Ci выражается через начальную концентрацию (CA,0=FA,0/W0).
- 34. Скачать презентацию

![Зависимость lg(kr/k0) от I1/2 для ионных реакций: [Со(NH3)5Br]2+ + Hg2+; СН2ВгСОО-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1305160/slide-2.jpg)
























 Разминка по дисциплине : «Ценообразование» Галибина Л. Т-114
Разминка по дисциплине : «Ценообразование» Галибина Л. Т-114  Права и обязанности медицинских работников, граждан, отдельных групп населения при оказании им медицинской помощи. Семейное право
Права и обязанности медицинских работников, граждан, отдельных групп населения при оказании им медицинской помощи. Семейное право Э п о х а г е н и е в Титаны Ренессанса
Э п о х а г е н и е в Титаны Ренессанса Виктор Николаевич Сорока-Россинский
Виктор Николаевич Сорока-Россинский Жанры изобразительного искусства
Жанры изобразительного искусства Путешествие в Государственную Третьяковскую галерею. «Жизнь коротка, а искусство долго». Гиппократ.
Путешествие в Государственную Третьяковскую галерею. «Жизнь коротка, а искусство долго». Гиппократ.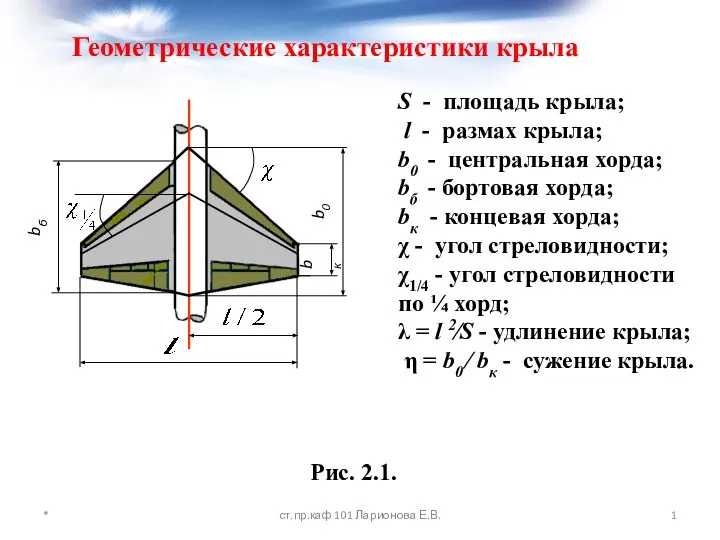 Геометрические характеристики крыла
Геометрические характеристики крыла Проект администрируемой сети на базе сервера
Проект администрируемой сети на базе сервера Valves mechanism
Valves mechanism Хозяйственные договора
Хозяйственные договора Культурно- національне відродження в кінці 18-початку 20 ст
Культурно- національне відродження в кінці 18-початку 20 ст Запись линейных алгоритмов в словесно-формульном представлении. (урок 2)
Запись линейных алгоритмов в словесно-формульном представлении. (урок 2) Практикум по теме: «Гражданское право»
Практикум по теме: «Гражданское право» Computational and Problem Solving(SDP1)
Computational and Problem Solving(SDP1) Что продавать в кризис. Как выбрать нишу для бизнеса?
Что продавать в кризис. Как выбрать нишу для бизнеса? Основы теории четырёхполюсников
Основы теории четырёхполюсников Оптимизация размера заказа при наличии скидок, зависящих от объема заказа
Оптимизация размера заказа при наличии скидок, зависящих от объема заказа Маркетинговая среда предприятия Подготовили Кондратенко Эльвира Арсёнова Виктория
Маркетинговая среда предприятия Подготовили Кондратенко Эльвира Арсёнова Виктория Лк 2 Хирургическая инфекция
Лк 2 Хирургическая инфекция Презентация____
Презентация____ Презентация "1С Предприятие" - скачать презентации по Экономике
Презентация "1С Предприятие" - скачать презентации по Экономике Презентация "Библия - книга книг" - скачать презентации по МХК
Презентация "Библия - книга книг" - скачать презентации по МХК В час нічний. А. С. Х
В час нічний. А. С. Х Взаимодействие с государственными институтами и технология лоббирования
Взаимодействие с государственными институтами и технология лоббирования Системи вищої освіти у країнах Європи та Америки
Системи вищої освіти у країнах Європи та Америки Основы теплового расчета энерготехнологического агрегата (камера радиационного охлаждения)
Основы теплового расчета энерготехнологического агрегата (камера радиационного охлаждения) Язык и государственная языковая политика
Язык и государственная языковая политика Таможенное регулирование как средство обеспечения экономической безопасности государства. Выполнила: студентка 3-го курса ФТ
Таможенное регулирование как средство обеспечения экономической безопасности государства. Выполнила: студентка 3-го курса ФТ