Содержание
- 2. Цель занятия: Сформировать знания студентов об окислительно-восстановительных методах количественного анализа. Задачи: Сформировать знания об основных методах
- 3. Студент должен знать: теоретические основы аналитической химии; методы качественного и количественного анализа неорганических и органических веществ,
- 4. В результате освоения темы «Окислительно-восстановительное титрование» обучающийся должен овладеть ОК: ОК 2. Организовывать собственную деятельность, определять
- 5. План. Общая характеристика методов редоксиметрии. Пермангонатометрия . Йодометрия. Нитритометрия. Броматометрия. Дихроматометрия.
- 6. 1. Общая характеристика методов редоксиметрии. ОВ-реакции лежат в основе ряда методов титриметрического анализа, которые объединяются под
- 7. Все методы оксидиметрии классифицируют в зависимости от окислителя или восстановителя, црименяемого в рабочем растворе, на следующие
- 8. Методы оксидиметрии позволяют с помощью рабочих растворов окислителей количественно определять в растворах или смесях разнообразные восстановители:
- 9. К реакциям, используемым в оксидиметрии, предъявляются требования: реакция при титровании должна протекать быстро и необратимо с
- 10. В оксидиметрии применяются различные методы определения точки эквивалентности. Например, в перманганатометрии она фиксируется по изменению окраски
- 11. 2. Пермангонатометрия Перманганатометрией называется метод объёмного анализа, в котором в качестве рабочего раствора применяют перманганат кали
- 12. Образование темного осадка затрудняет определение конца реакции, поэтому титрование проводят в кислой среде, прибавляя большой избыток
- 13. В некоторых случаях реакция окисления с помощью перманганата калия проходит с небольшой скоростью. Поэтому титрование проводят
- 14. Перманганатометрию чаще всего применяют для анализа солей железа (II), кальция (в виде оксалата), щавелевой кислоты, меди
- 15. 3. Йодометрия. Йодометрией называют метод объёмного анализа, в основе которого лежат реакции: I2+2e-→ 2I-, 2I--2e-→I2. Методом
- 16. 1. Определение окислителей. Методом йодометрии можно определять те окислители, которые количественно окисляют I- в свободный I2.
- 17. Большинство окислителей нельзя непосредственно титровать тиосульфатом натрия, так как невозможно фиксировать точку эквивалентности. Поэтому для определения
- 18. Индикатором в методе йодометрии служит раствор крахмала. Это чувствительный и специфический индикатор, образующий с йодом адсорбционное
- 19. 2. Определение восстановителей. Из числа восстановителей этим методом чаще всего определяют сульфиты, сульфиды, тиосульфаты, хлорид олова
- 20. Все йодометрические определения проводят при следующих условиях: Реакция должна протекать практически до конца; многие йодометрические реакции
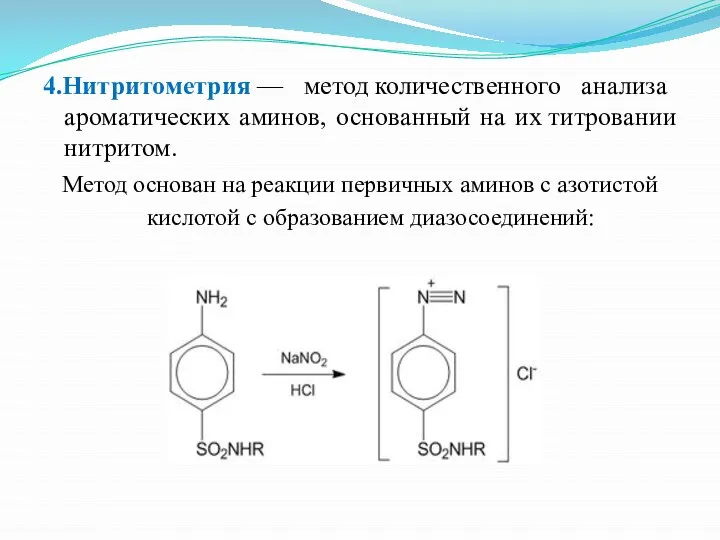
- 21. 4.Нитритометрия — метод количественного анализа ароматических аминов, основанный на их титровании нитритом. Метод основан на реакции
- 22. Титрантом является раствор нитрита натрия, готовят с титром установленным, исходное вещество – сульфаниловая кислота, предварительно высушенная
- 23. Точка эквивалентности определяется при помощи индикаторов — тропеолина 00 (переход от красного цвета раствора к жёлтому),
- 24. Для титрования обычно используют 0,1М раствор нитрита натрия. Навеску препарата (например, лекарственного средства класса сульфаниламидов) растворяют
- 25. Применение Нитритометрия используется для количественного анализа соединений с первичной или вторичной ароматической аминогруппой, гидразидов и ароматических
- 26. 5. Броматометрия — метод окислительно-восстановительного титрования, основанный на реакции восстановления бромат-иона. Методы бромирования применяются для количественного
- 27. При использовании метода бромирования в качестве титрованного раствора применяется раствор бромата калия. Этот раствор можно готовить
- 28. Свободный бром в момент выделения бромирует органические соединения, находящиеся в определяемом растворе. В методах бромирования используют
- 29. Наряду с реакциями окисления — восстановления в присутствии бромидов наблюдаются также реакции присоединения брома и замещение
- 30. В методе прямого титрования определение точки эквивалентности осуществляют визуально по изменению окраски титруемого раствора, индикаторным методом
- 31. Для повышения четкости и точности определения конца титрования применяют специальные необратимые индикаторы (азокрасители) метиловый оранжевый и
- 32. Техника титрования. Титрование проводят в кислой среде в присутствии хлористоводородной или серной кислоты, способствующих мгновенному выделению
- 33. В методах обратного титрования очень часто прибегают к постановке холостого опыта для того, чтобы уточнить, какое
- 34. Кроме того, броматометрию применяют для определения многих других неорганических и органических соединений: фенолов и их производных,
- 35. Броматометрический метод отличается рядом достоинств по сравнению с другими методами. 1. Бромат-бромидные растворы можно применять не
- 36. Броматометрический метод имеет также ряд недостатков. 1. Вода, присутствующая в растворе или образующаяся в процессе титрования
- 37. 6. Дихроматометрия Хроматометрия (дихроматометрия) — метод окислительно-восстановительного титрования, основанный на реакциях окисления раствором дихромата калия в
- 38. Титрант метода Титрантом метода является водный раствор дихромата калия К2Cr2О7, чаще всего с молярной концентрацией эквивалента
- 39. Определение конечной точки титрования Водные растворы дихромата калия имеют оранжевую окраску, однако ее интенсивность недостаточна для
- 40. Применение Прямым дихроматометрическим титрованием можно определять ряд восстановителей, таких, как железо(II) (включая определение ферроцианидов, содержащих ферроцианид-ион
- 41. Общая оценка метода Дихроматометрия в сравнении с перманганатометрией обладает как некоторыми преимуществами, так и недостатками. К
- 42. IV. Закрепление. Составить таблицу по графам Метод редоксиметрии Область применения Способы титрования Рабочие растворы в соответствии
- 43. V.Задание на дом. Тема: Редоксиметрия. Вопросы для самоподготовки: Пермангонатометрия . Йодометрия. Нитритометрия. Броматометрия. Дихроматометрия.
- 45. Скачать презентацию









































 Анализ и диагностика финансового состояния предприятия
Анализ и диагностика финансового состояния предприятия  Собеседование по найму: понятие, виды, типичные вопросы
Собеседование по найму: понятие, виды, типичные вопросы Презентация Документы, регламентирующие перевозку железнодорожным транспортом
Презентация Документы, регламентирующие перевозку железнодорожным транспортом  Антибиотики
Антибиотики Определение инновационной деятельности
Определение инновационной деятельности Набойка Костромы. Кустарное производство Костромы
Набойка Костромы. Кустарное производство Костромы МОДУЛЬНЫЙ ПРИНЦИП ПРЕДМЕТА «ОРКСЭ» – СИТУАЦИЯ РОДИТЕЛЬСКОГО ВЫБОРА Методист Регионального центра духовно-нравственного ра
МОДУЛЬНЫЙ ПРИНЦИП ПРЕДМЕТА «ОРКСЭ» – СИТУАЦИЯ РОДИТЕЛЬСКОГО ВЫБОРА Методист Регионального центра духовно-нравственного ра Онлайн курсы по спортивному ориентированию. Зимний курс теоретических тренировок для летнего спортивного ориентирования
Онлайн курсы по спортивному ориентированию. Зимний курс теоретических тренировок для летнего спортивного ориентирования Қазақстан Республикасының азаматтық құқығы
Қазақстан Республикасының азаматтық құқығы Hard disk
Hard disk 3
3 Порядок создания предприятия
Порядок создания предприятия  Дневник – помощник в саморазвитии школьника Дневники 1 – 4-го кл. Образовательной системы «Школа 2100»
Дневник – помощник в саморазвитии школьника Дневники 1 – 4-го кл. Образовательной системы «Школа 2100» Разработка системных приложений. Основные понятия. Процессы
Разработка системных приложений. Основные понятия. Процессы Bobby
Bobby Тема 2. Общие проблемы экономического развития.
Тема 2. Общие проблемы экономического развития.  Изобразительное искусство Древней Руси на примере иконописи конца XIV - начало XVI в
Изобразительное искусство Древней Руси на примере иконописи конца XIV - начало XVI в Вещество, энергия, информация
Вещество, энергия, информация Кейс на основе судебного решения по возмещению вреда, причиненного жизни и здоровью гражданина
Кейс на основе судебного решения по возмещению вреда, причиненного жизни и здоровью гражданина Идеал человека в христианстве
Идеал человека в христианстве Повірка імпульсних та універсальних вольтметрів (тема № 2, заняття № 3)
Повірка імпульсних та універсальних вольтметрів (тема № 2, заняття № 3) Три котенка - презентация для начальной школы
Три котенка - презентация для начальной школы Администрирование
Администрирование Работа с базой PHP MYSQL
Работа с базой PHP MYSQL Halloween. Origins and Traditions
Halloween. Origins and Traditions Мин татарча сөйләшәм
Мин татарча сөйләшәм Презентация на тему "Методические подходы к подготовке учащихся 5–8 классов к участию в математических конкурсах и олимпиадах&qu
Презентация на тему "Методические подходы к подготовке учащихся 5–8 классов к участию в математических конкурсах и олимпиадах&qu Хронические неспецифические заболевания лёгких у детей Хронические неспецифические заболевания лёгких у детей
Хронические неспецифические заболевания лёгких у детей Хронические неспецифические заболевания лёгких у детей