Содержание
- 2. Н.Н.Семенов - цепные реакции перекисного окисления жирных кислот 1957 - свободных радикалов в организме нет 2.
- 3. Перекисное окисление липидов ПОЛ представляет цепной свободнорадикальный процесс окисления ненасыщенных жирных кислот, протекающий по типу аутоокисления
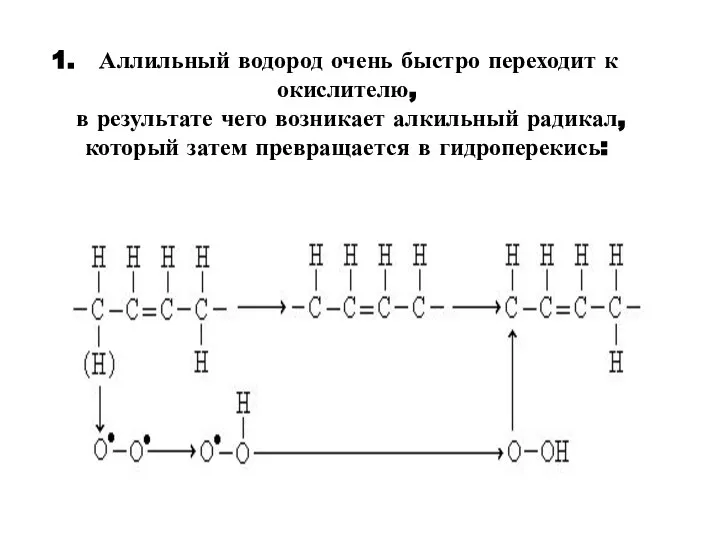
- 4. Аллильный водород очень быстро переходит к окислителю, в результате чего возникает алкильный радикал, который затем превращается
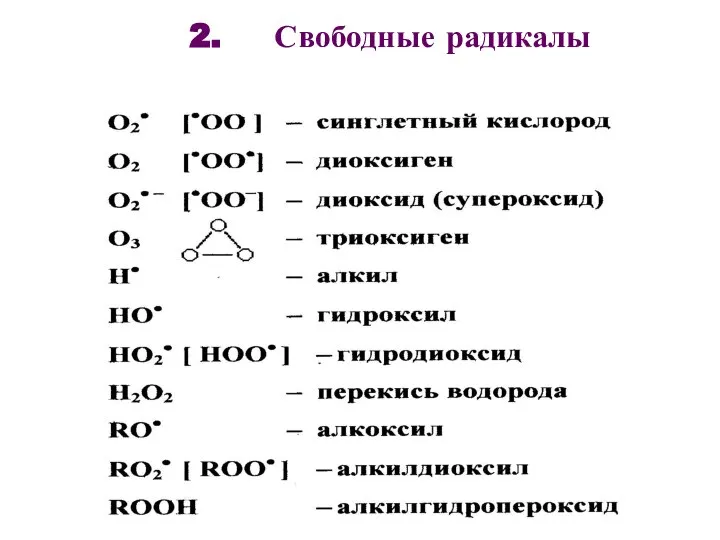
- 5. 2. Свободные радикалы
- 6. Молекулярный кислород находится в триплетном состоянии, его обозначают О=О Молекула О2 содержит 2 неспаренных электрона, одновременно
- 7. O2· [·OO ] – синглетный кислород Синглетный кислород образуется при переходе электрона внутри молекулы между внешними
- 8. O2·– [·OO–] - супероксидный радикал Супероксидный анион - отрицательно заряженный свободный радикал O2·– дает ограниченный токсический
- 9. HO· – гидроксилный радикал образуется при взаимодействии с водородом, очень реакционноспособен и может представлять угрозу для
- 10. Активные формы кислорода Термин "АФК" шире, чем "свободные радикалы кислорода" (О2∙-, НО∙) включает также молекулы: Н2О2
- 11. Значение свободнорадикального окисления Бактерицидное и цитотоксическое действие Регуляция артериального давления Развитие радиационных повреждений Развитие УФ -
- 12. 3. Образование свободных радикалов
- 13. Продолжение 4.
- 14. 5. Продукты перекисного окисления липидов 6. гидроксиноненали: С5Н9 –СНОН – СН = СН – СНО (4
- 15. АФК вызывают в липидах (L) (остатках полиненасыщенных жирных кислот) цепные реакции с накоплением липидных радикалов L·,
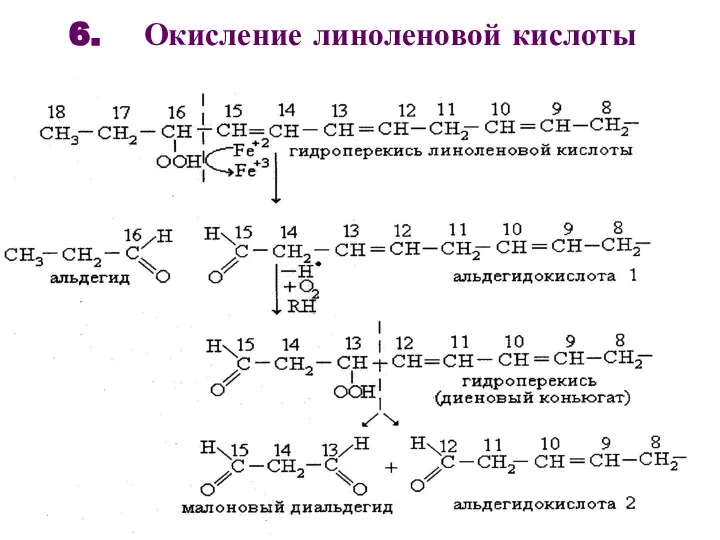
- 16. 6. Окисление линоленовой кислоты
- 17. Классификация радикалов Первичные - образуются за счет реакций одноэлектронного восстановления с участием металлов с переменной валентностью
- 18. Первичные радикалы специально вырабатываются в организме Вторичные – оказывают цитотоксическое действие Многие заболевания развиваются вследствие образования
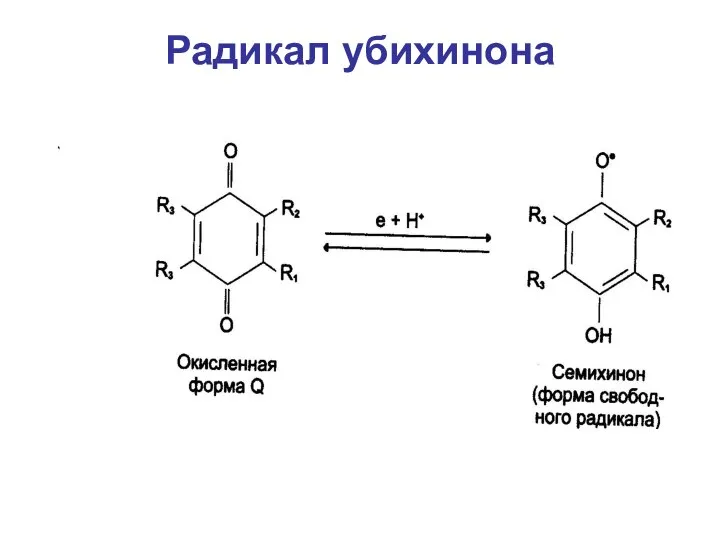
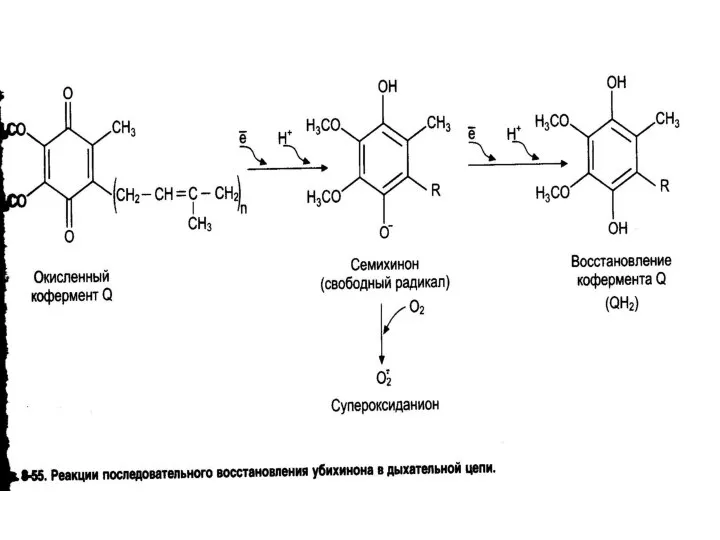
- 19. Радикал убихинона
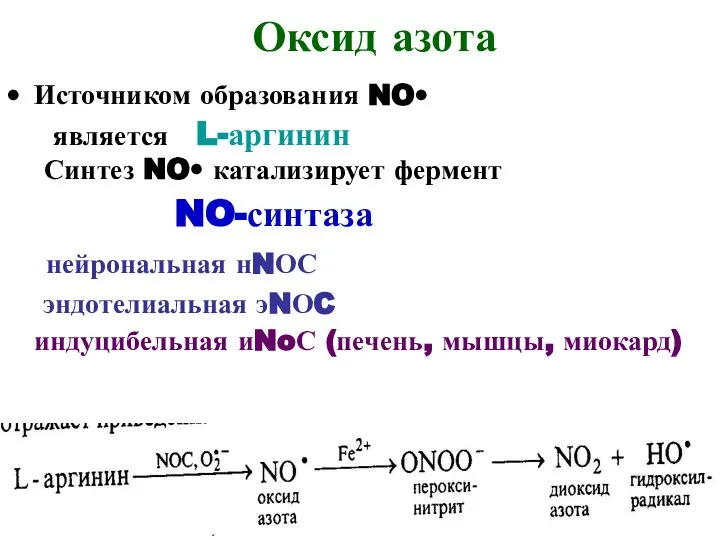
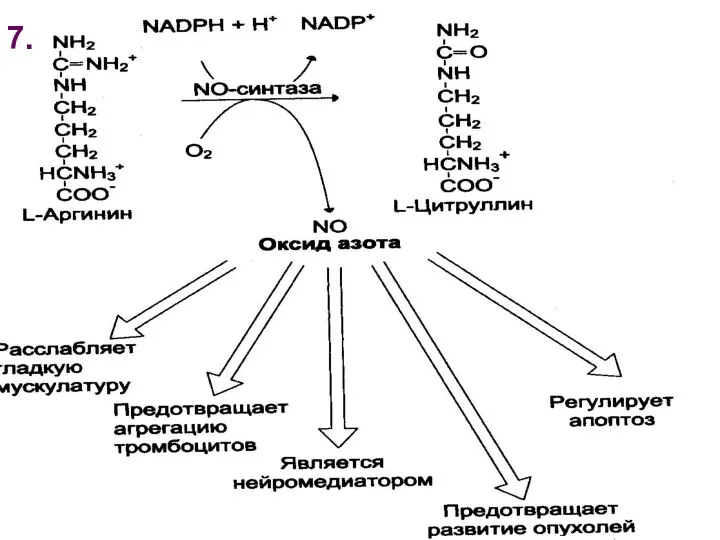
- 20. Оксид азота Источником образования NO• является L-аргинин Синтез NO• катализирует фермент NO-синтаза нейрональная нNОС эндотелиальная эNОC
- 21. iNOS Синтезируется в макрофагах, фибробластах, гепатоцитах Идукторы: ИЛ-1, АФК, эндотоксины, бактериальные компоненты NO· повреждает микрорганизмы, чужеродные
- 22. 7.
- 23. Методы изучения процессов ПОЛ Продукты ПОЛ Хемилюминесценция – реакция рекомбинации супероксида, гидроксила, липидных радикалов (10-9М) Электронный
- 24. Значение ПОЛ 5% кислорода восстанавливается в супероксид-ион, 10% О2 превращается в Н2О2 Ненасыщенные соединения, входящие в
- 25. ОБРАЗОВАНИЕ ПЕРЕКИСИ ВОДОРОДА В КЛЕТКЕ Утилизация кислорода в клетке осуществляется в следующих процессах: биологического окисления в
- 26. Образование перекиси водорода в клетке
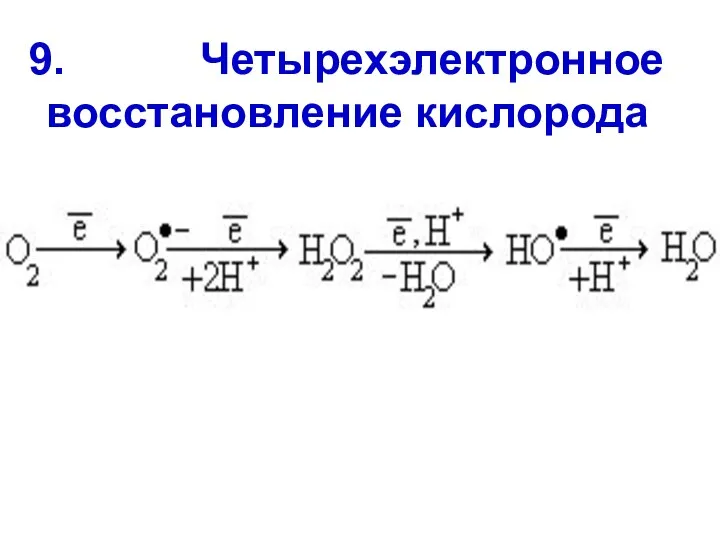
- 27. 9. Четырехэлектронное восстановление кислорода
- 28. Скорость образования Н2О2 в органеллах Микросомы - 1,5 – 3 нмоль/мин∙г белка Митохондрии - 0,5 нмоль/мин∙г
- 30. Каталаза Гемопротеид, содержит 4 гемовые группы Обладает пероксидазной активностью, утилизирует Н2О2 для окисления фенолов, формальдегида, этанола,
- 31. Супероксиддисмутаза СОД в цитоплазме состоит из 2 субъединиц, содержит ионы Zn2+ и Cu2+ СОД в митохондриях
- 32. Окислительная модификация (ОМ) Окислительная модификация нуклеиновых кислот При ОМ ДНК происходит образование гидропероксидов ROOH (из тимина
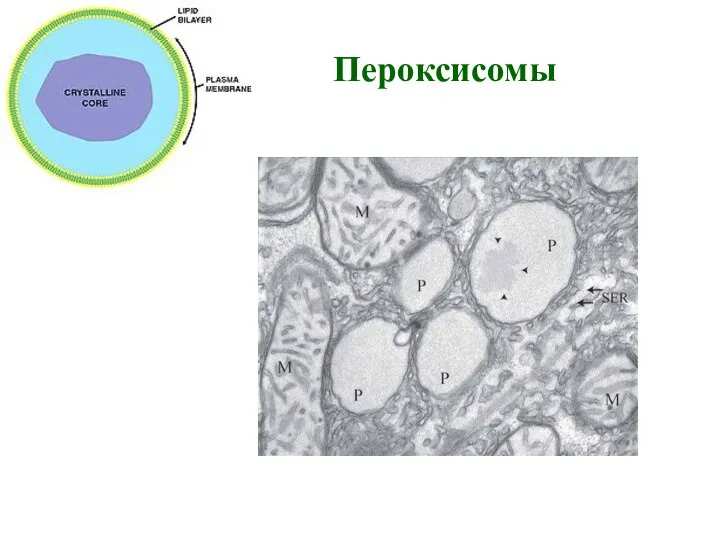
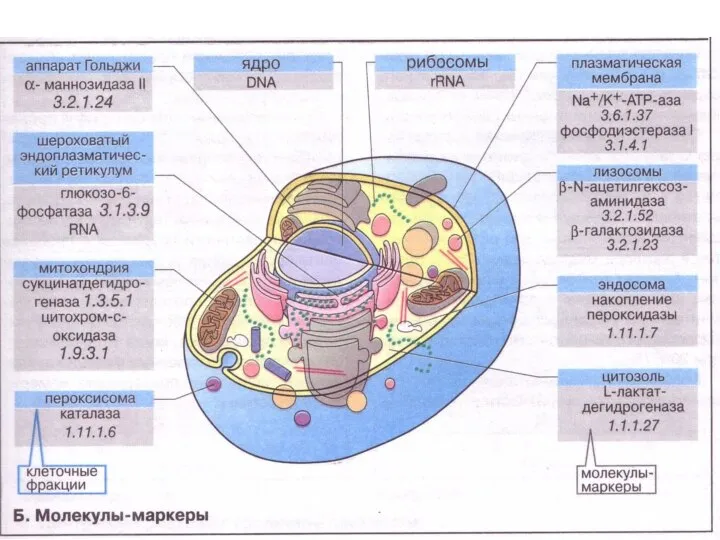
- 33. Пероксисомы – специфические органеллы, в которых происходит образование и разрушение перекиси водорода Пероксисомы(или микротельца) — 0,3-1,5
- 34. Пероксисомы
- 35. Пероксисомы Пероксисома (лат. peroxysoma) — обязательная органелла клетки) — обязательная органелла клетки, содержит оксидазы D-аминокислот, уратоксидазу
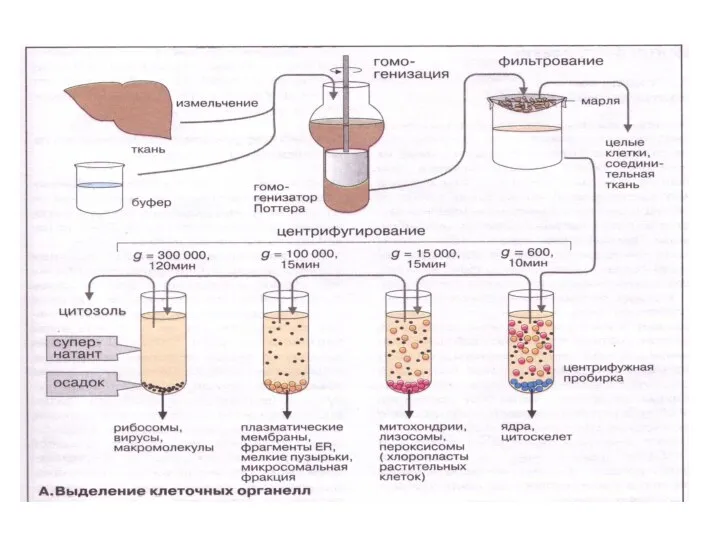
- 36. Пероксисомы выделяют из клетки методом дифференциального центрифугирования Удельная плотность пероксисом 1,25, митохондрий (1,19) лизосом (1,23) Выделяются
- 39. Ферменты пероксисом Моноаминоксидаза превращает амины в альдегиды Ксантиноксидаза превращает гипоксантин в ксантин Уратоксидаза окисляет ураты: Мочевая
- 40. Функции пероксисом Метаболическая функция Образование Н2О2 с участием оксидаз Липидный обмен: локализация вблизи капель нейтрального жира,
- 41. Роль пероксисом Количество пероксисом увеличивается при авитаминозе Е, голодании, недостатке неэтерифицированных жирных кислот, при изменении гомеостаза
- 42. Наследственные дефекты пероксисом При акаталазии наблюдается угнетение липидного обмена. Болезнь Цельвегера характеризуется отсутствием пероксисом, сопровождается резкой
- 43. РЕГУЛЯЦИЯ ПЕРЕКИСНОГО ОКИСЛЕНИЯ В КЛЕТКЕ Состояние ПОЛ в клетке определяется следующими факторами: Качественным составом ненасыщенных жирных
- 44. Не все фосфолипиды одинаково чувствительны к перекисному окислению При усилении ПОЛ мембраны обогащаются более устойчивыми к
- 45. ПРООКСИДАНТЫ Прооксиданты (или катализаторы) – это вещества, стимулирующие процессы ПОЛ К ним относятся: активные формы кислорода
- 46. Роль ионов железа
- 47. Метаболизм железа в организме Содержание железа в белках: Гемоглобин 3,0 г Миоглобин 0,15 г Ферритин 0,7
- 48. Усвоению железа в полости кишечника способствует аскорбиновая кислота, восстанавливающая железо. В клетках слизистой кишечника железо соединяется
- 49. Антиоксиданты содержат подвижный атом водорода с ослабленной связью с углеродом, препятствуют образованию свободных радикалов Ловушки радикалов
- 50. Ловушки радикалов Ингибиторы свободнорадикальных реакций, липидные антиоксиданты Резко тормозят свободнорадикальные реакции в низких концентрациях Витамин Е,
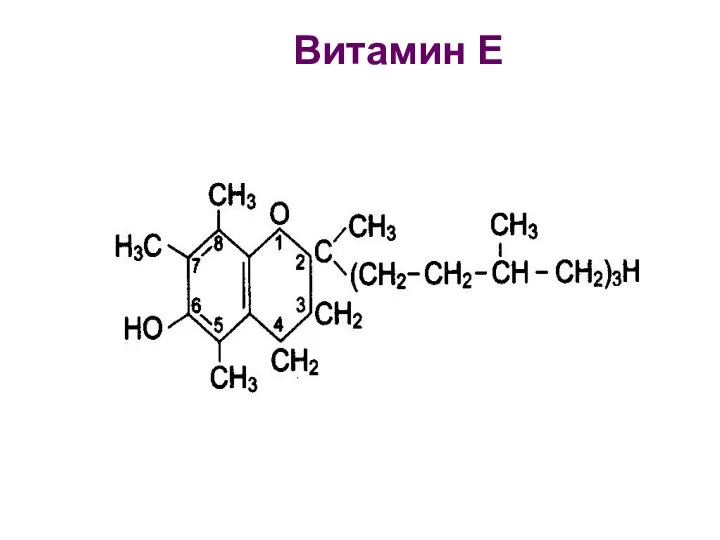
- 51. Витамин Е
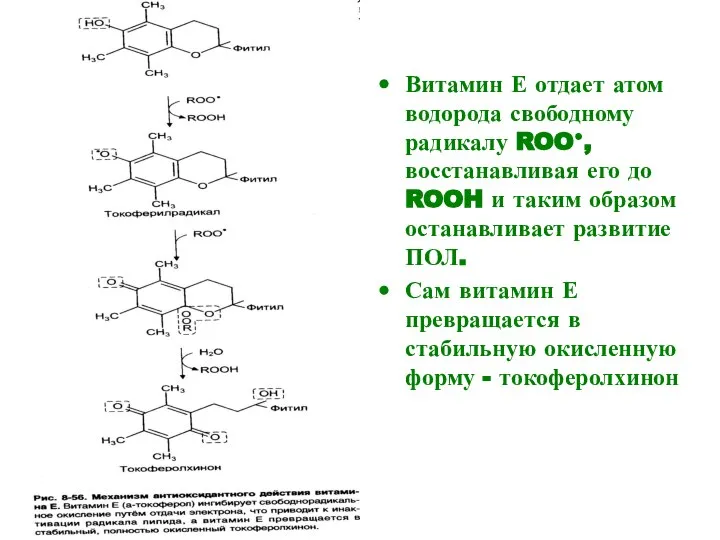
- 52. Витамин Е отдает атом водорода свободному радикалу ROO●, восстанавливая его до ROOH и таким образом останавливает
- 53. Витамин Е Фактор резистентности эритроцитов к гемолизу, повышает перекисную резистентность эритроцитов Снижает агрегацию тромбоцитов Повышает уровень
- 54. Вещества-синергисты Способны восстанавливать Fe3+ до Fe2+ Являясь донорами водорода, способны восстанавливать окисленную форму антиоксиданта и замедляют
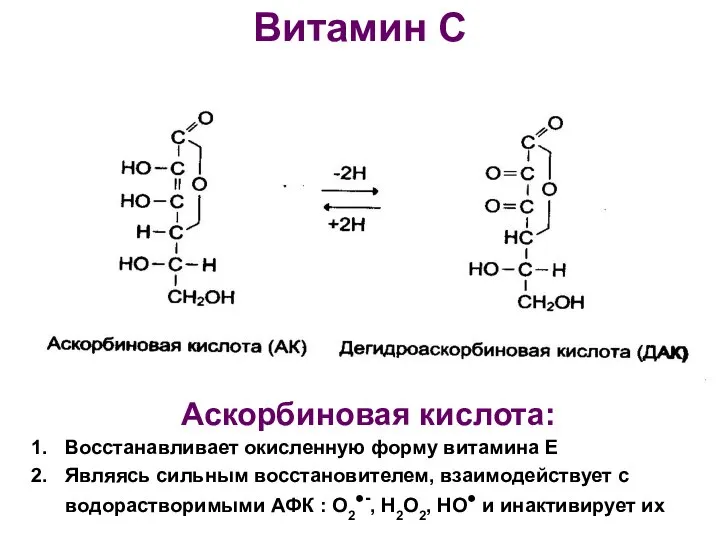
- 55. Витамин С Аскорбиновая кислота: Восстанавливает окисленную форму витамина Е Являясь сильным восстановителем, взаимодействует с водорастворимыми АФК
- 56. 12. Суточная потребность в витаминах Е 100 - 600 мг С 100 - 700 мг В2
- 57. Витамин С Связывает токсические вещества: свинец, мышьяк, бензол, бактерии, вирусы Предотвращает ломкость сосудов, Поддерживает целостность сосудистой
- 58. Комплексоны Снижают образование вторичных радикалов, связывая ионы железа ЭДТА, ортофосфаты, пирофосфаты, десфероксамин (десферал), тетрациклин К природным
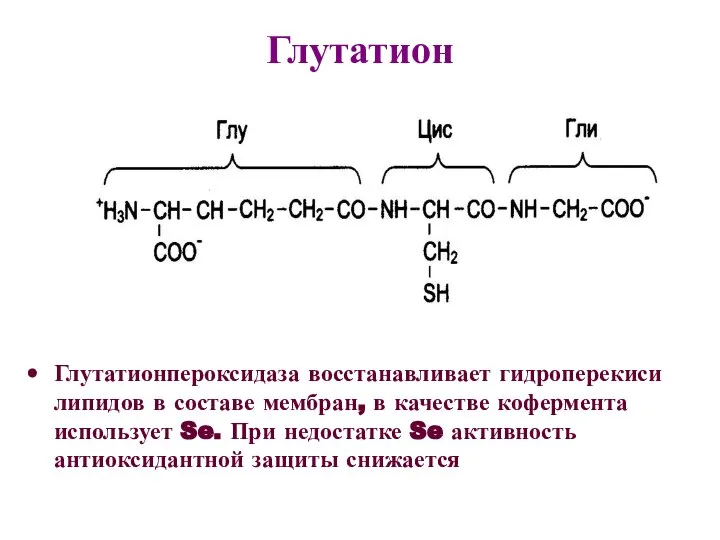
- 59. Глутатион Глутатионпероксидаза восстанавливает гидроперекиси липидов в составе мембран, в качестве кофермента использует Se. При недостатке Se
- 60. 13. Система глутатион-глутатионпероксидаза обладает антирадикальным и антиперекисным действием Глутатионпероксидаза 2G–SH + 2RO2∙ → G–SS–G + 2ROOH
- 62. Кудесан
- 63. КЛАССИФИКАЦИЯ ПЕРЕКИСНЫХ СИСТЕМ В образовании липидных перекисей в клетках животных принимают участие 2 системы: 1. Аскорбатзависимая
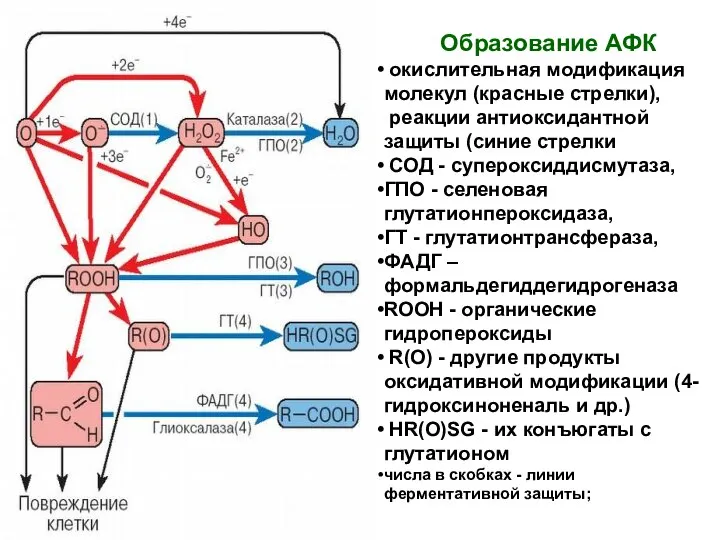
- 64. Образование АФК окислительная модификация молекул (красные стрелки), реакции антиоксидантной защиты (синие стрелки СОД - супероксиддисмутаза, ГПО
- 65. Значение АФК Человек в покое вдыхает около 280 мл О2 /мин, или не менее 400 л/сут,
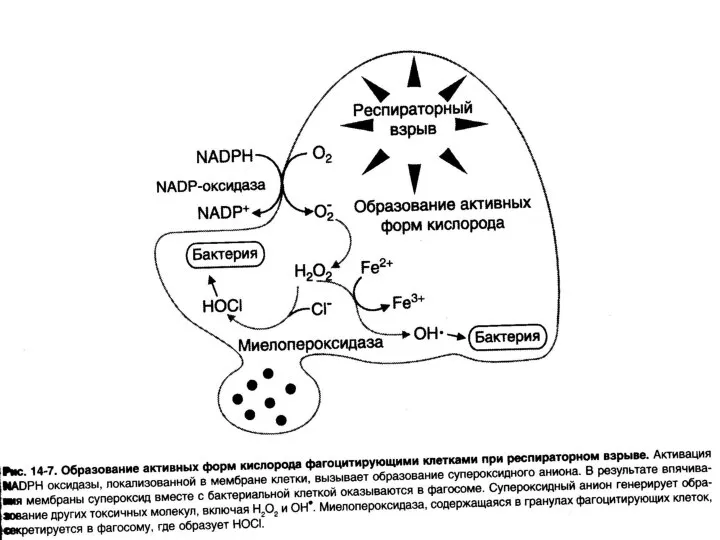
- 66. Биологическая роль ПОЛ Синтез эйкозаноидов Образование перекисей липидов в микросомах Образование желчных кислот из холестерола Респираторный
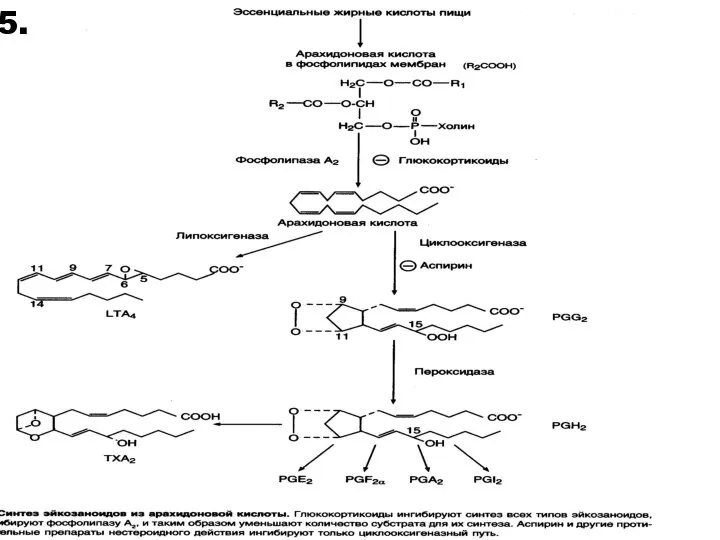
- 67. Эйкозаноиды-производные полиненасыщенных жирных кислот Простаноиды – циклические, лейкотриены - линейные. Промежуточными метаболитами являются пероксиды Простагландины образуются
- 68. 15.
- 69. Производные арахидоновой кислоты Каннабиноиды – продукты взаимодействия арахидоновой кислоты с аминами (анандамин) Изопростаны – продукты взаимодействия
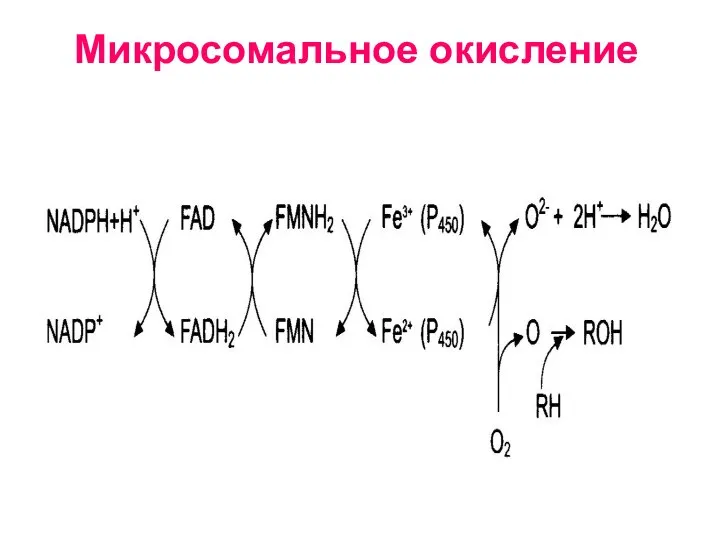
- 70. Микросомальное окисление
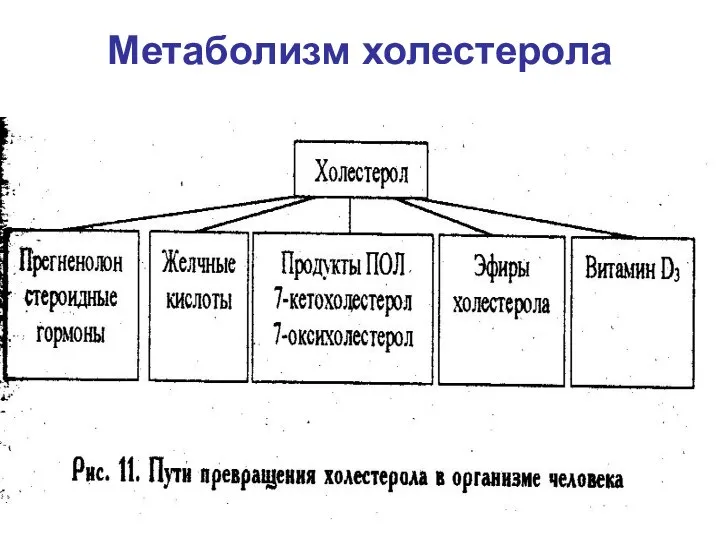
- 71. Метаболизм холестерола
- 73. ПОЛ при патологии Ионизирующие излучения Злокачественный рост Атеросклероз Катаракта
- 74. Ионизирующие излучения Радиолиз воды Радиотоксины семихиноны, альдегиды, кетоны, перекиси Кислородный эффект Скрытые повреждения Окисление SH-групп, однонитевые
- 75. Злокачественный рост Факторы: канцерогены, ионизирующие излучения, вирусы На начальных этапах количество радикалов – увеличивается В сформировавшейся
- 76. Атеросклероз Атеросклероз – хроническое поражение артерий, вызванное разрастанием множественных плотных утолщений артерий (бляшек), суживающих их просвет
- 77. Липопротеины При атеросклерозе изменяется состав ЛП крови: повышается содержание ЛПНП и снижается содержание ЛПВП ЛПНП являются
- 78. Перекисно-модифицированные липопротеины Окисленные липопротеины имеют большую плотность, больше содержат сфингомиелина, лизофосфатидилхолина, чем нативные ЛПНП Окисленные ЛПНП
- 79. ПОЛ при атеросклерозе Активация аутоокисления ХС Антиоксидантная недостаточность Нарушение превращения ХС в желчные кислоты Свободно-радикальное окисление
- 80. Тромбоз Предрасположенность к тромбозу: Повреждение эндотелия Изменение скорости кровотока Склонность к повышенной свертываемости крови Дефицит витамина
- 81. Факторы риска при атеросклерозе Гиподинамия Снижение поступления антиоксидантов с рафинированной пищей Снижение количества антиоксидантов в пище
- 82. Катаракта Катаракта – помутнение хрусталика Факторы: действие ионизирующих излучений, ультрафиолет, травмы хрусталика, диабет, воспалительные заболевания глаз,
- 83. Гипероксия, гипоксия Гипероксия – кислородное отравление При гипероксии – избыток акцептора электронов - О2 Гипоксия –
- 84. Окислительный стресс Повреждение мембран Снижение активности антиоксидантных ферментов Накопление первичных и вторичных продуктов ПОЛ Распад липопротеинов
- 85. Активные формы кислорода Образование свободных радикалов ингибирует ферменты Инициирует образование поперечных сшивок в молекулах коллагена АФК,
- 86. Три линии защиты от цитотоксического действия АФК Супероксиддисмутаза – защищает от O2· – Каталаза - защищает
- 87. Перекисная гипотеза гибели клетки В биологических мембранах клетки содержатся ненасыщенные жирные кислоты, фосфолипиды, холестерол, ионы Fe2+.
- 89. Скачать презентацию



![O2· [·OO ] – синглетный кислород Синглетный кислород образуется при переходе](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1302987/slide-6.jpg)
![O2·– [·OO–] - супероксидный радикал Супероксидный анион - отрицательно заряженный свободный](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1302987/slide-7.jpg)





























































 Общеразвивающие упражнения
Общеразвивающие упражнения places-in-the-school-ppt-flashcards-fun-activities-games-picture-descriptio_53340
places-in-the-school-ppt-flashcards-fun-activities-games-picture-descriptio_53340 Модели деловой карьеры менеджера
Модели деловой карьеры менеджера Тема проповеди: Секрет 10 конвертов, или Как правильно планировать семейный бюджет
Тема проповеди: Секрет 10 конвертов, или Как правильно планировать семейный бюджет Строковые потоки и буферы
Строковые потоки и буферы Уран - самая голубая планета
Уран - самая голубая планета  Тренажёр по русскому языку 2 класс Учитель начальных классов МАОУ «СОШ №26 г. Сыктывкара» Республики Коми Иконникова Зоя Никол
Тренажёр по русскому языку 2 класс Учитель начальных классов МАОУ «СОШ №26 г. Сыктывкара» Республики Коми Иконникова Зоя Никол Конституционные правовые отношения
Конституционные правовые отношения Специальное снаряжение для водного туризма
Специальное снаряжение для водного туризма Проектирование электрооборудования станка токарно-винторезного МК6046М. Схемы
Проектирование электрооборудования станка токарно-винторезного МК6046М. Схемы Program M2 Internship at SPIN Center-PMMG
Program M2 Internship at SPIN Center-PMMG Курсовая работа по дисциплине «Основы управления персоналом» тема: «Совершенствование условий труда персонала»
Курсовая работа по дисциплине «Основы управления персоналом» тема: «Совершенствование условий труда персонала» Приключения в парке В. Маяковского. Одним субботним днем
Приключения в парке В. Маяковского. Одним субботним днем Политическая культура
Политическая культура Презентация на тему "Проект - это" - скачать презентации по Педагогике
Презентация на тему "Проект - это" - скачать презентации по Педагогике Выполнили: студенты ФФМО специальности «лечебное дело» группы 222 Буданова Анна Милинтеева Ксения.
Выполнили: студенты ФФМО специальности «лечебное дело» группы 222 Буданова Анна Милинтеева Ксения.  Геополитические отношения между Россией и Японией
Геополитические отношения между Россией и Японией Презентация "Дело в шляпе" - скачать презентации по МХК
Презентация "Дело в шляпе" - скачать презентации по МХК Noveyshaya_istoria_2
Noveyshaya_istoria_2 Основы религиозной культуры и светской этики
Основы религиозной культуры и светской этики Urok_trezvosti
Urok_trezvosti Механический мерительный инструмент с преобразователями
Механический мерительный инструмент с преобразователями Лабораторія промислових контролерів Unitronics VISION
Лабораторія промислових контролерів Unitronics VISION Парфенон
Парфенон Предел последовательности - презентация по Алгебре
Предел последовательности - презентация по Алгебре Политический процесс и политическое изменение
Политический процесс и политическое изменение Halloween. Корни этого праздника
Halloween. Корни этого праздника Презентация "Стратегический менеджмент" - скачать презентации по Экономике
Презентация "Стратегический менеджмент" - скачать презентации по Экономике