Содержание
- 2. Теория гибридизации Лайнус Полинг Лаунус Полинг – американский химик, физик (1901-94 гг) Первые исследования по применению
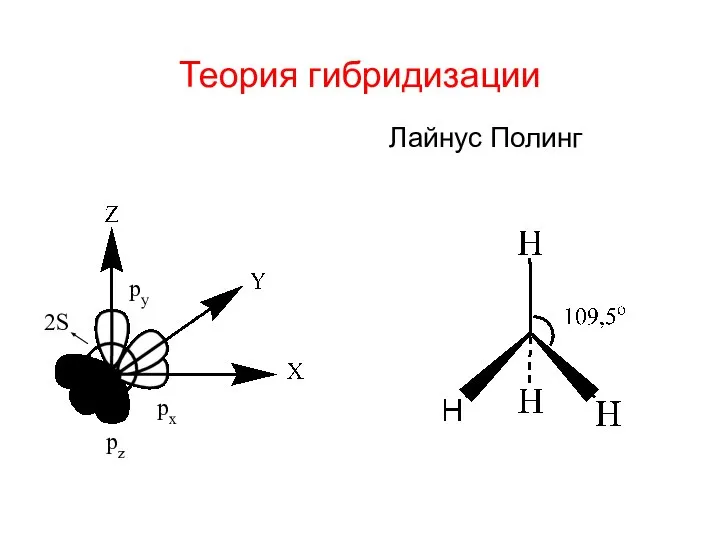
- 3. Теория гибридизации Лайнус Полинг 2S pz px py
- 4. Графан
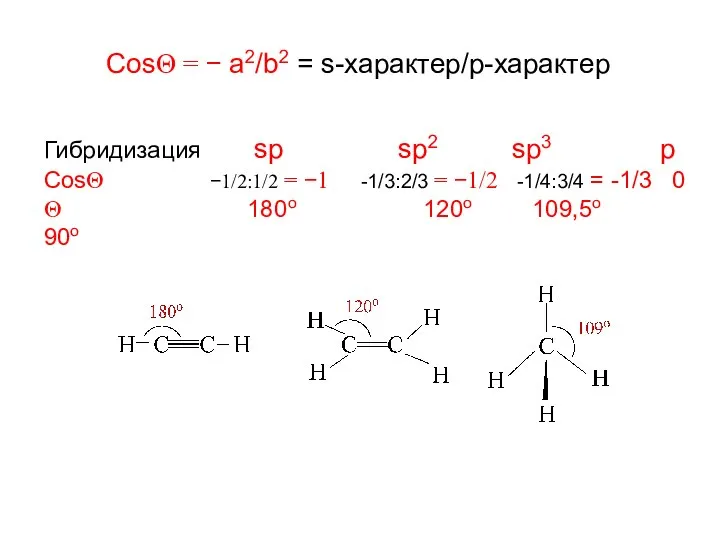
- 6. CosΘ = − a2/b2 = s-характер/p-характер Гибридизация sp sp2 sp3 p CosΘ −1/2:1/2 = −1 -1/3:2/3
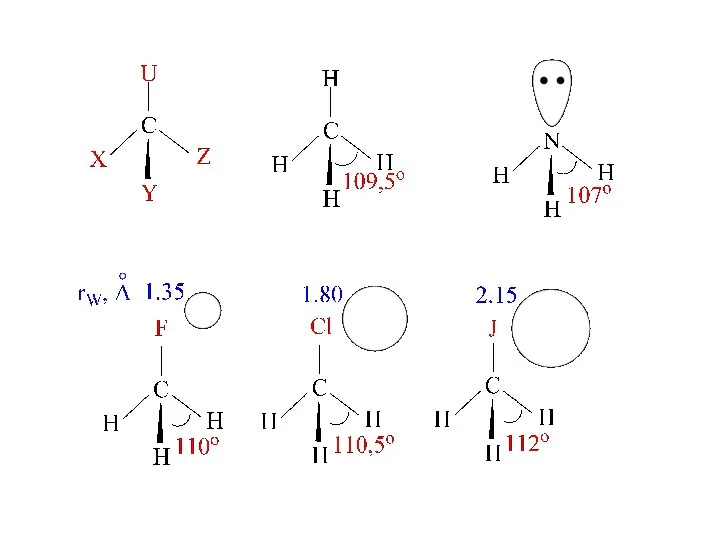
- 8. Правило Бента: В соединениях углерода и некоторых других элементов 2-ого периода s-характер концентрируется преимущественно в направлении
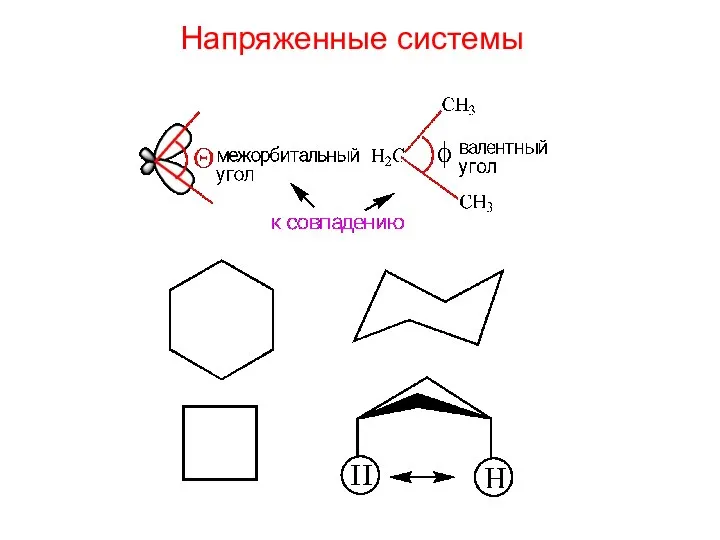
- 9. Напряженные системы
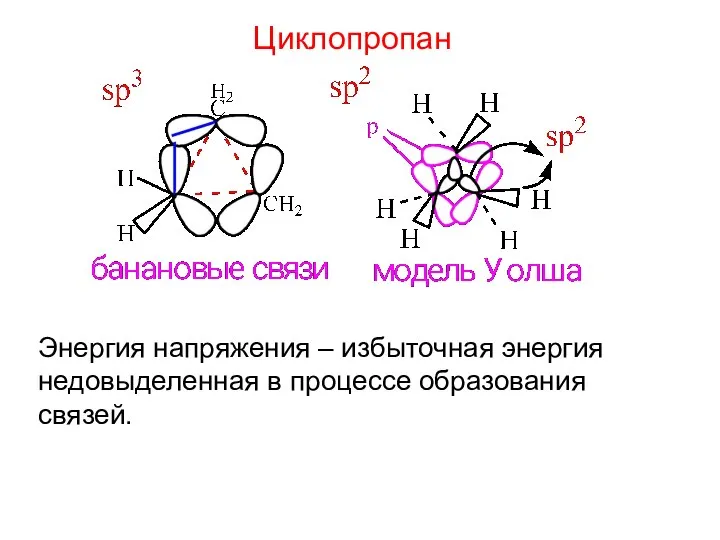
- 10. Циклопропан Энергия напряжения – избыточная энергия недовыделенная в процессе образования связей.
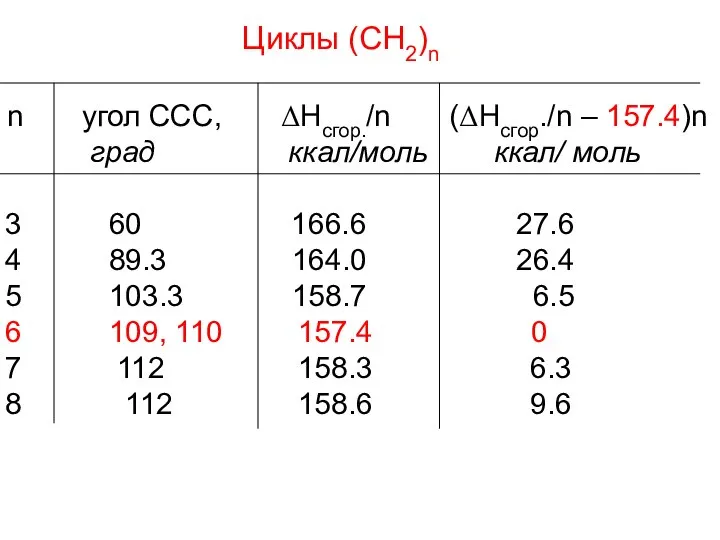
- 11. Циклы (СН2)n n угол ССС, ΔHсгор./n (ΔHсгор./n – 157.4)n град ккал/моль ккал/ моль 60 166.6 27.6
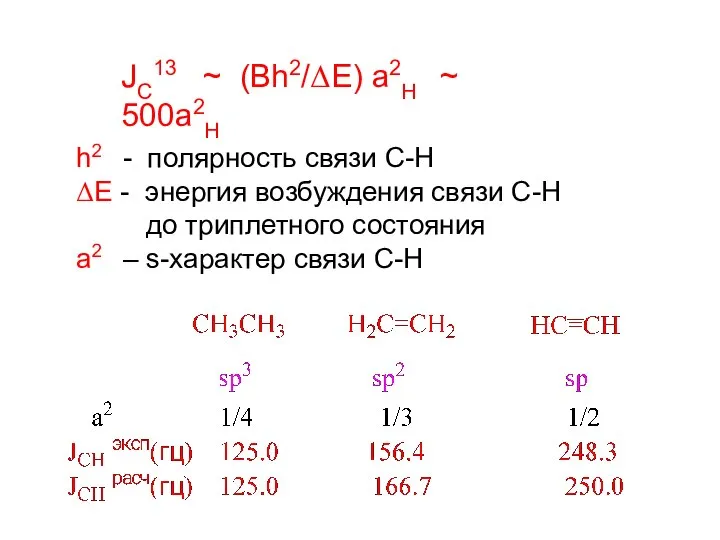
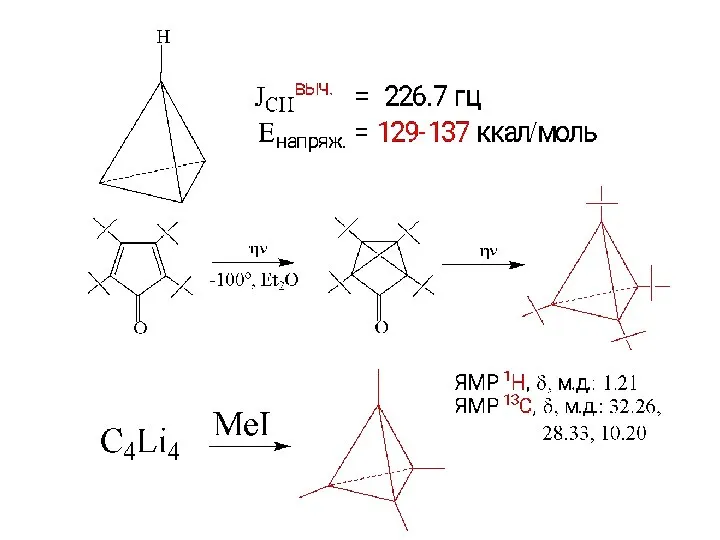
- 12. JC13 ~ (Bh2/ΔE) a2H ~ 500a2H h2 - полярность связи С-Н ΔE - энергия возбуждения связи
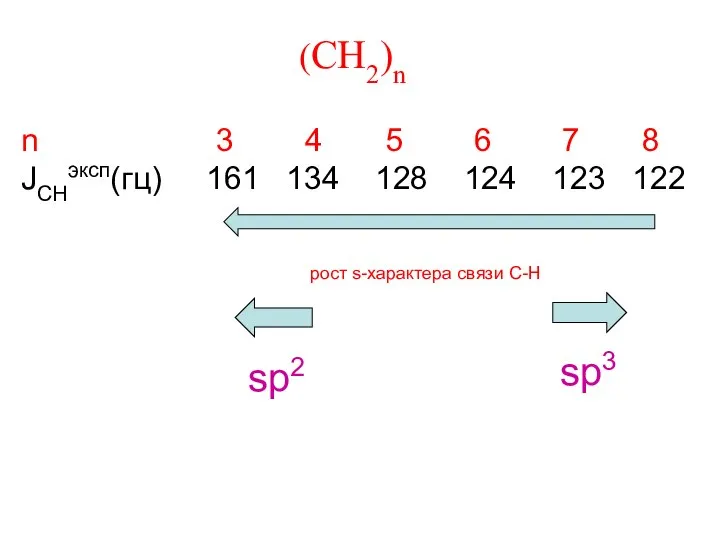
- 13. (CH2)n n 3 4 5 6 7 8 JCHэксп(гц) 161 134 128 124 123 122 рост
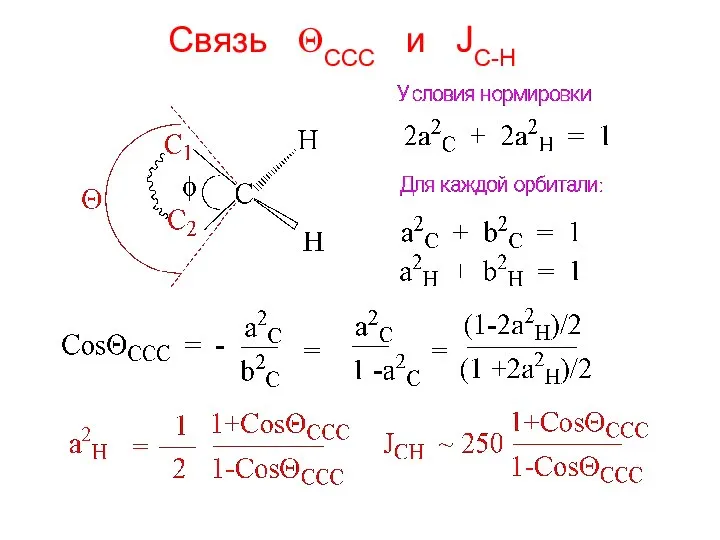
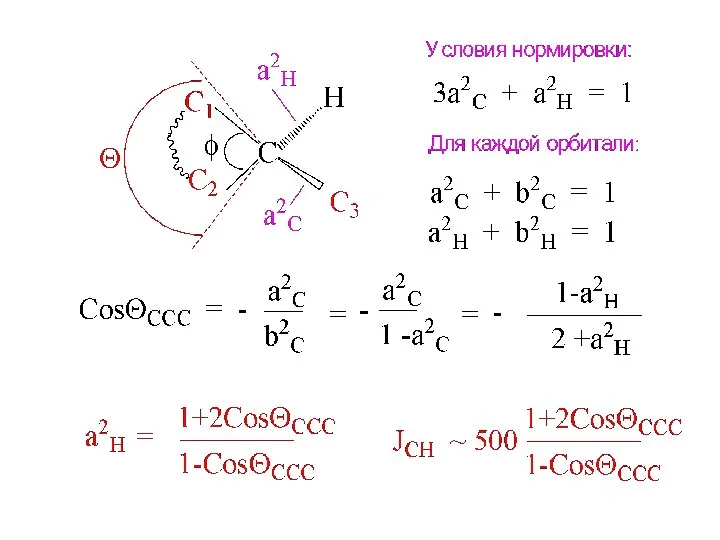
- 14. Связь ΘCCC и JC-H
- 15. Принимаем: Θ = Aφ + B Найдем A и B 1-ая точка Θ = φ =
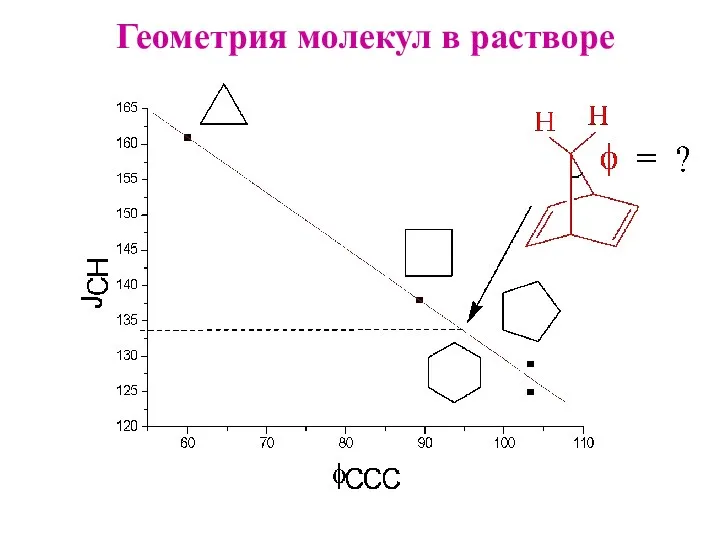
- 16. Геометрия молекул в растворе
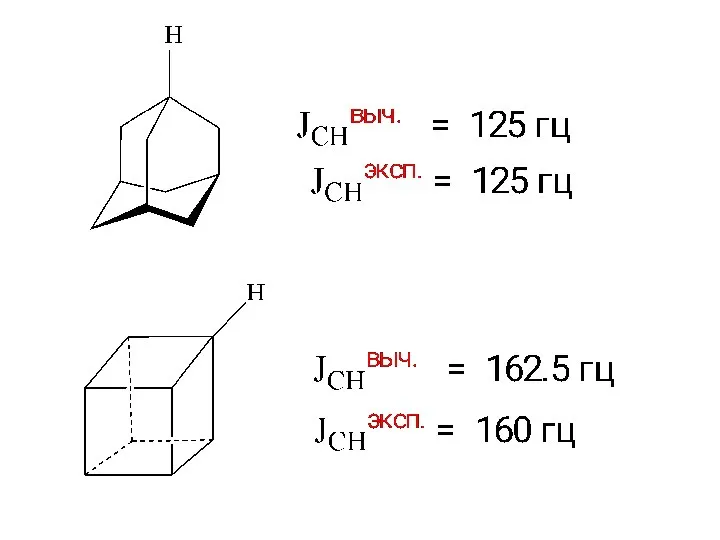
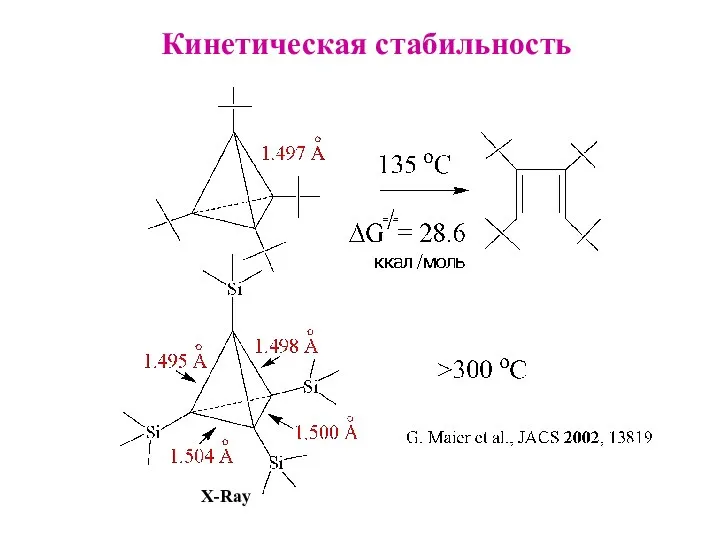
- 20. Кинетическая стабильность X-Ray
- 22. Скачать презентацию





 Әлемдегі ең ерекше 10 қонақүй
Әлемдегі ең ерекше 10 қонақүй Физиология органа зрения и основные зрительные функции
Физиология органа зрения и основные зрительные функции Почему украинский кризис - ошибка Запада
Почему украинский кризис - ошибка Запада Всероссийский интернет-урок антинаркотической направленности Имею право знать
Всероссийский интернет-урок антинаркотической направленности Имею право знать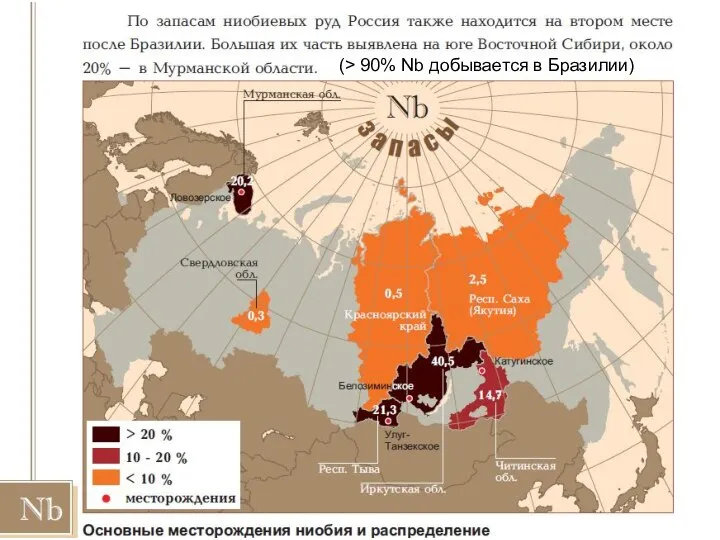 Запасы тантала Nb,Ta,TR RF
Запасы тантала Nb,Ta,TR RF Военно-полевые сборы
Военно-полевые сборы Системы менеджмента качества
Системы менеджмента качества Аттестационная работа. Проект по созданию мобильных экскурсионных групп
Аттестационная работа. Проект по созданию мобильных экскурсионных групп Служебно-деловой этикет
Служебно-деловой этикет Язык программирования Java
Язык программирования Java Навстречу комплексу ГТО
Навстречу комплексу ГТО Анекдоты и карикатуры. Работа системы здравоохранения
Анекдоты и карикатуры. Работа системы здравоохранения Стерилизация Презентация по дисциплине: «Основы Сестринского Дела» Автор: Филатова А.С.
Стерилизация Презентация по дисциплине: «Основы Сестринского Дела» Автор: Филатова А.С. Сварные соединения
Сварные соединения «Забери -Товар». РФ
«Забери -Товар». РФ Засiб вимiрювання. Iндикатори годинникового типу електроннi. (Завдання 3)
Засiб вимiрювання. Iндикатори годинникового типу електроннi. (Завдання 3) Структура научно-исследовательской работы учащихся
Структура научно-исследовательской работы учащихся Технология монтажа модульных потолков
Технология монтажа модульных потолков Введение в психологию. Предмет, объект и методы психологии Вопросы: 1. Психология как наука и учебная дисциплина 2. Основные з
Введение в психологию. Предмет, объект и методы психологии Вопросы: 1. Психология как наука и учебная дисциплина 2. Основные з Как создать сайт на Google
Как создать сайт на Google Презентация урока по алгебре: Функция у=ах² +вх+с Учитель математики МОУ СОШ №32 Г. Хабаровска Тараскина С.В.
Презентация урока по алгебре: Функция у=ах² +вх+с Учитель математики МОУ СОШ №32 Г. Хабаровска Тараскина С.В. Немецкая кухня
Немецкая кухня Рай. Вселенная 25
Рай. Вселенная 25 Внешняя политика государства. Теории и реалии
Внешняя политика государства. Теории и реалии Сдержанность в речи
Сдержанность в речи Презентация Изучение проблемных областей государственного регулирования.
Презентация Изучение проблемных областей государственного регулирования. Специальные упражнения на развитие общей,мелкой, артикуляционной моторики. Дыхательная гимнастика - презентация для начальной шк
Специальные упражнения на развитие общей,мелкой, артикуляционной моторики. Дыхательная гимнастика - презентация для начальной шк Классный час. Готов к труду и обороне (ГТО)
Классный час. Готов к труду и обороне (ГТО)