Содержание
- 2. Электроны атома в ядерной модели не могут быть неподвижны. Если бы они не двигались, то в
- 3. подробно обсуждался. В квантовой механике классическое представление об орбите заменяется представлением о геометрическом месте точек, в
- 4. Видно, что скорость электрона в атоме водорода весьма велика, а ускорение таково, что электрон в атоме
- 5. Применение к ядерной модели атома Резерфорда классических законов механики, электричества и оптики привело к полному противоречию
- 6. Линейчатый спектр атома водорода Светящиеся газы дают линейчатые спектры испускания, состоящие из отдельных спектральных линий. Когда
- 7. Здесь R = 10 973 731 м-1 называется постоянной Ридберга. Величина, обратная длине волны, v* =
- 8. Кроме линий серии Бальмера, расположенных.в видимой части спектра, у водорода были обнаружены другие серии спектральных линий,
- 9. серия Пфунда: и серия Хэмфри: С другой стороны от видимой области, в далекой ультрафиолетовой области спектра,
- 10. Рис. 28.3 На шкале справа указаны волновые числа в см-1. Смысл шкалы слева выяснится дальше. Все
- 11. Для данной серии n = m + 1, m + 2 и т. д. Для серии
- 12. определяющими энергетические уровни атома водорода. Однако от открытия сериальных формул для атома водорода до строгого решения
- 14. Скачать презентацию
Электроны атома в ядерной модели не могут быть неподвижны. Если бы
Электроны атома в ядерной модели не могут быть неподвижны. Если бы
Рассмотрим, например, ядерную модель простейшего атома — атома водорода, который состоит из одного электрона и ядра — протон). Для простоты будем считать, что электрон движется вокруг ядра по круговой орбите. Заметим, прежде всего, что, употребляя слово «орбита», следует помнить, что волновые свойства электрона и соотношения неопределенностей приводят к тому, что для электрона в атоме представление об орбите как о траектории движения не выдерживает критики. Этот вопрос
подробно обсуждался. В квантовой механике классическое представление об орбите заменяется представлением
подробно обсуждался. В квантовой механике классическое представление об орбите заменяется представлением
Скорость электрона в атоме водорода на круговой орбите
с радиусом r ≈ 10-10 м можно подсчитать, приняв во внимание,
что центростремительной силой, удерживающей электрон на ор-
бите, является кулоновская сила его притяжения к ядру:
Из этого уравнения, подставив численные значения массы т элект-рона, его заряда е и электрической постоянной ε0, получим, что: υ ≈«106 м/с. При этом центростремительное ускорение электрона a= υ2/r по порядку величины составляет 1022 м/с2.
Видно, что скорость электрона в атоме водорода весьма
велика, а ускорение таково,
Видно, что скорость электрона в атоме водорода весьма велика, а ускорение таково,
Этот вывод с неизбежностью следует из применения к электрону в ядерной модели классических законов. Но отсюда, далее, следует, что атом не может быть устойчив: электрон, непрерывно теряющий энергию на излучение, не может удержаться на круговой траектории. Он должен по спирали приближаться к ядру и через время τ ≈ 10-10 с упасть на него. С другой стороны, частота, с ко-; торой электрон движется вокруг ядра, должна непрерывно изменяться. А из этого следует, что непрерывно должна изменяться частота электромагнитных волн, излучаемых электроном. Другими словами, атом водорода должен давать излучение с непрерывным спектром частот. Линейчатого спектра у атома быть не должно.
Применение к ядерной модели атома Резерфорда классических законов механики, электричества и
Применение к ядерной модели атома Резерфорда классических законов механики, электричества и
В действительности оказывается, что:
а) атом является исключительно устойчивой системой;
б) атом излучает электромагнитные волны лишь при определенных условиях;
в) атом испускает свет, обладающий линейчатым спектром, связанным со строением и свойствами его электронной оболочки.
Полное несоответствие выводов, основанных на классическом истолковании ядерной модели атома, и опытных фактов вызвало сомнения в возможности применять к электронам в атомах законы классической физики и привело к созданию современной квантовой механики.
Линейчатый спектр атома водорода
Светящиеся газы дают линейчатые спектры испускания, состоящие
Линейчатый спектр атома водорода
Светящиеся газы дают линейчатые спектры испускания, состоящие
линий спектра водорода могут быть вычислены по формуле 28.3
(28.3)
Формулу (28.3) Ридберг предложил записывать в виде
(28.4)
Здесь R = 10 973 731 м-1 называется постоянной Ридберга. Величина,
Здесь R = 10 973 731 м-1 называется постоянной Ридберга. Величина,
В настоящее время известно большое число спектральных
линий водорода, длины волн которых с большой степенью точности
удовлетворяют формуле Бальмера - Ридберга. Из (27.4) видно,
что спектральные линии, отличающиеся различными значениями п,
образуют группу, или серию, линий, называемую серией Бальмера.
С увеличением п спектральные линии серии сближаются друг с другом. Граница серии Бальмера определяется длиной волны λгран,
при которой п →∞: λгран = 4/R = 364,5068 нм.
Кроме линий серии Бальмера, расположенных.в видимой части спектра, у водорода были
Кроме линий серии Бальмера, расположенных.в видимой части спектра, у водорода были
В далекой инфракрасной области были обнаружены еще три серии спектральных линий водорода: серия Брэкета:
серия Пфунда:
и серия Хэмфри:
С другой стороны от видимой области, в далекой
серия Пфунда:
и серия Хэмфри:
С другой стороны от видимой области, в далекой
Каждая из этих серий характеризуется сгущением спектральных линии при возрастании чисел п и своей граничной частотой или длиной волны. На рис. 28.3 изображены серии спектра водорода.
Рис. 28.3
На шкале справа указаны волновые числа в см-1. Смысл шкалы
Рис. 28.3
На шкале справа указаны волновые числа в см-1. Смысл шкалы
Все частоты (или волновые числа) всех спектральных линий водорода можно выразить единой формулой:
Для данной серии n = m + 1, m + 2
Для данной серии n = m + 1, m + 2
ν*rpaн = R/m2 .
Формула (28.5) подтвердилась на опыте с большой, спектроскопической точностью. В ней ярко выступила особая роль целых чисел в спектроскопических закономерностях, осмысленная до конца лишь в квантовой механике. Ранее мы видели, что в квантовой механике вскрывается особая роль целых чисел — квантовых чисел п, определяющих дискретные значения энергии электронов в потенциальном «ящике» и осцилляторе. Забегая вперед, укажем, что числа т и п в формуле (28.5) также являются квантовыми числами,
(28.5)
определяющими энергетические уровни атома водорода. Однако от открытия сериальных формул для
определяющими энергетические уровни атома водорода. Однако от открытия сериальных формул для
Постулаты Бора
В 1913 г. Бор создал первую неклассическую теорию атома. В основе этой теории лежала идея связать в единое целое три результата, полученные в физике к тому времени:
а) эмпирические закономерности линейчатого спектра атома
водорода, выраженные в формуле Бальмера - Ридберга;
б) ядерную модель атома Резерфорда, не допускающую классического истолкования;
в) квантовый характер излучения и поглощения света.











 Текст Государственного гимна Российской Федерации. Конституция Российской Федерации,
Текст Государственного гимна Российской Федерации. Конституция Российской Федерации, Организация работы на уроках русского языка с использованием ТУДО
Организация работы на уроках русского языка с использованием ТУДО Запорожские казаки сегодня
Запорожские казаки сегодня Социолингвистика в США
Социолингвистика в США Некоторые приемы работы со сборками. Анализ собираемости
Некоторые приемы работы со сборками. Анализ собираемости Тема: «Возрастная периодизация психического развития человека»
Тема: «Возрастная периодизация психического развития человека»  Подшипники скольжения
Подшипники скольжения Тема урока: Жизнь египетского вельможи План урока: В усадьбе вельможи Служба вельмож Вельможа при дворе фараона
Тема урока: Жизнь египетского вельможи План урока: В усадьбе вельможи Служба вельмож Вельможа при дворе фараона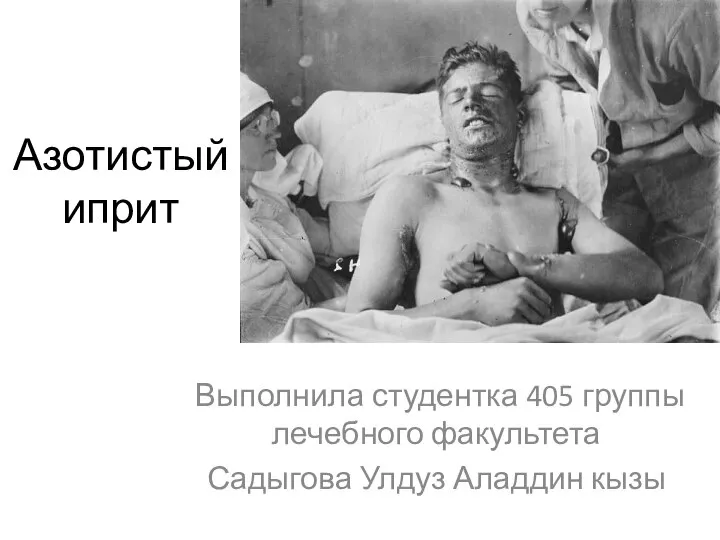 Азотистый иприт
Азотистый иприт  Закономерности распределения напряжений в грунте фазы деформаций грунта под фундаментом
Закономерности распределения напряжений в грунте фазы деформаций грунта под фундаментом Федеральный закон-52 О санитарно-эпидемиологическом благополучии населения
Федеральный закон-52 О санитарно-эпидемиологическом благополучии населения Презентация Рынок недвижимости и особенности его функционирования
Презентация Рынок недвижимости и особенности его функционирования  Приборы радиационного контроля
Приборы радиационного контроля  Разработка мехатронного модуля выдвижного устройства гидрологического прибора
Разработка мехатронного модуля выдвижного устройства гидрологического прибора МУЛЬТИПЛИКАТОР ЦЕНА/ВЫРУЧКА ОТ РЕАЛИЗАЦИИ В ОЦЕНКЕ СТОИМОСТИ ПРЕДПРИЯТИЯ (БИЗНЕСА)
МУЛЬТИПЛИКАТОР ЦЕНА/ВЫРУЧКА ОТ РЕАЛИЗАЦИИ В ОЦЕНКЕ СТОИМОСТИ ПРЕДПРИЯТИЯ (БИЗНЕСА)  Презентация Управление развитием таможенной деятельности в Стратегии развития таможенной службы
Презентация Управление развитием таможенной деятельности в Стратегии развития таможенной службы  Ферми-системы. Модель Хаббарда
Ферми-системы. Модель Хаббарда открывая двери_финал
открывая двери_финал Финансовое планирование и прогнозирование
Финансовое планирование и прогнозирование  Механический мерительный инструмент с преобразователями
Механический мерительный инструмент с преобразователями ВНЕШНЯЯ И ВНУТРЕННЯЯ СРЕДА ОРГАЗИЗАЦИИ
ВНЕШНЯЯ И ВНУТРЕННЯЯ СРЕДА ОРГАЗИЗАЦИИ Закон о кассовых аппаратах
Закон о кассовых аппаратах Назначение таможенной операции «временное хранение товаров» Презентацию подготовил студент 1 курса Фомин Максим
Назначение таможенной операции «временное хранение товаров» Презентацию подготовил студент 1 курса Фомин Максим  Презентация по экономике на тему: «История возникновения денег»
Презентация по экономике на тему: «История возникновения денег» Конденсаторы: виды, характеристики
Конденсаторы: виды, характеристики Специалист в автоматизации
Специалист в автоматизации Общие сведения о сборно-разборных и цельноперевозимых пролетных строениях
Общие сведения о сборно-разборных и цельноперевозимых пролетных строениях АНО ДОД ДЮСШ «REAL-M»
АНО ДОД ДЮСШ «REAL-M»