Содержание
- 2. ВАКЦИНЫ это препараты, содержащие антигены (АГ) возбудителей инфекционных заболеваний, и предназначенные для создания искусственного активного иммунитета
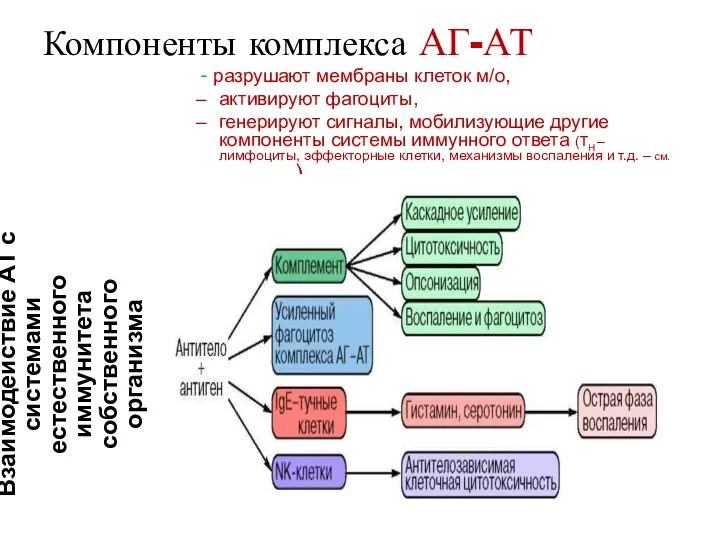
- 4. Компоненты комплекса АГ-АТ - разрушают мембраны клеток м/о, активируют фагоциты, генерируют сигналы, мобилизующие другие компоненты системы
- 5. Костюм для работы с ООИ
- 6. Вакцины нового поколения Лишены недостатков традиционных вакцин. Для их разработки применяют методы генной инженерии.
- 7. Если антитела, вырабатываемые в ответ на введение традиционных вакцин, связываются с поверхностными белками патогенного м/о и
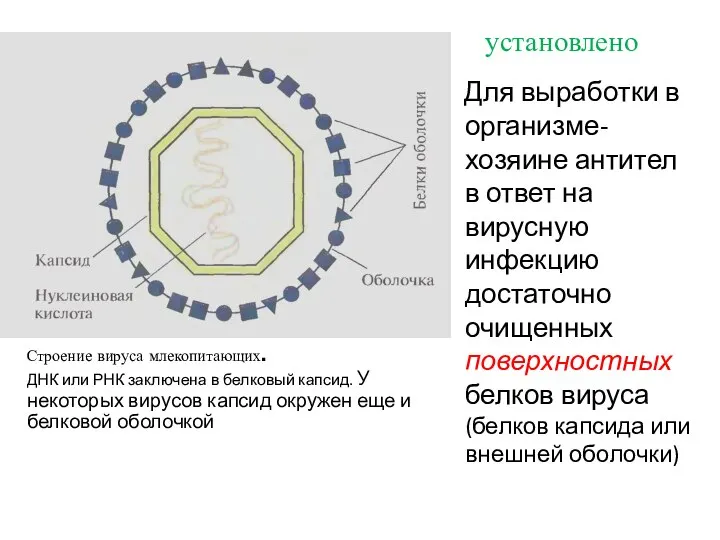
- 8. установлено Строение вируса млекопитающих. ДНК или РНК заключена в белковый капсид. У некоторых вирусов капсид окружен
- 9. 1. Субъединичные вакцины Вакцины, содержащие лишь отдельные компоненты патогенного м/о
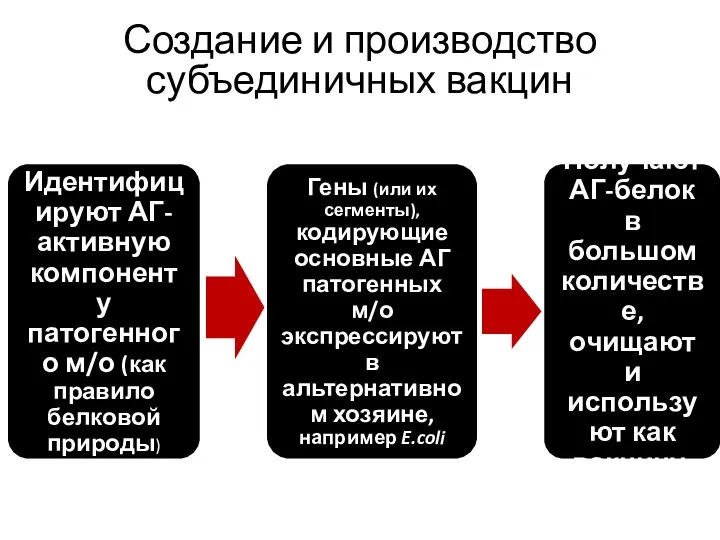
- 10. Создание и производство субъединичных вакцин
- 11. Преимущества и недостатки субъединичных вакцин Преимущества: очищенный иммуногенный белок стабилен Безопасен (в сравнении с патогенным м/о
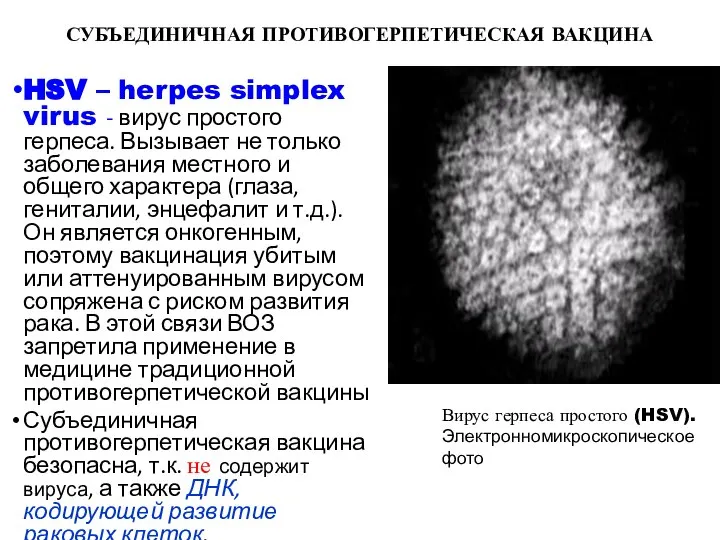
- 12. СУБЪЕДИНИЧНАЯ ПРОТИВОГЕРПЕТИЧЕСКАЯ ВАКЦИНА HSV – herpes simplex virus - вирус простого герпеса. Вызывает не только заболевания
- 13. СОЗДАНИЕ И ПРОИЗВОДСТВО ВАКЦИНЫ ПРОТИВ ГЕРПЕСА ПРОСТОГО
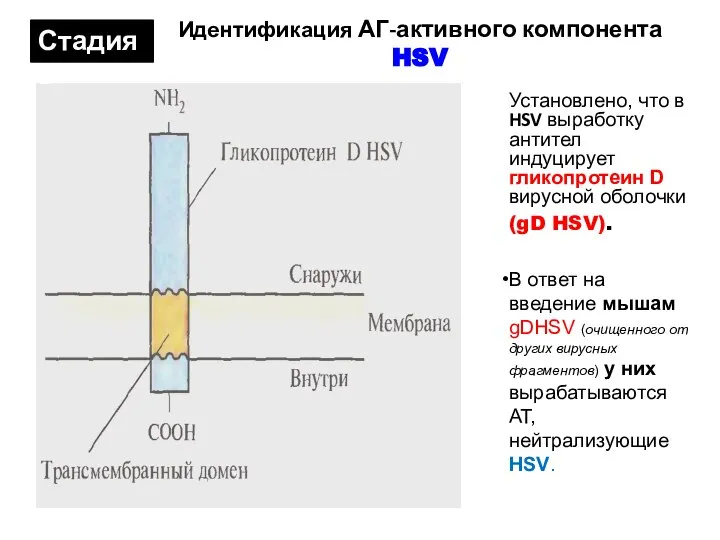
- 14. Идентификация АГ-активного компонента HSV Установлено, что в HSV выработку антител индуцирует гликопротеин D вирусной оболочки (gD
- 15. Идентификация генов, кодирующих АГ-активный компонент HSV Ген, кодирующий gD HSV, был изолирован и клонирован в клетках
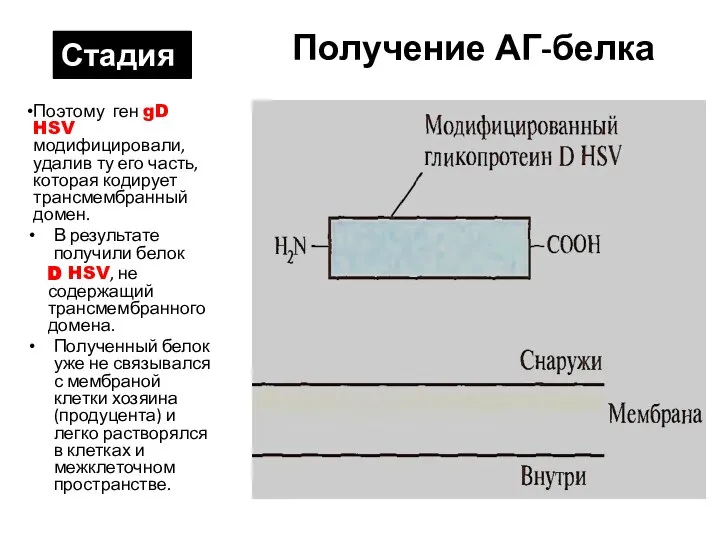
- 16. Получение АГ-белка Поэтому ген gD HSV модифицировали, удалив ту его часть, которая кодирует трансмембранный домен. В
- 17. Получаение АГ-белка Однако для выработки точно специфичных АТ важно было получить не просто протеин, а гликопротеин.
- 18. Субъединичная противотуберкулезная вакцина В стадии разработки. Возбудитель туберкулеза – Mycobacterium tuberculosis. 2 млрд людей инфицировано. Актуальность
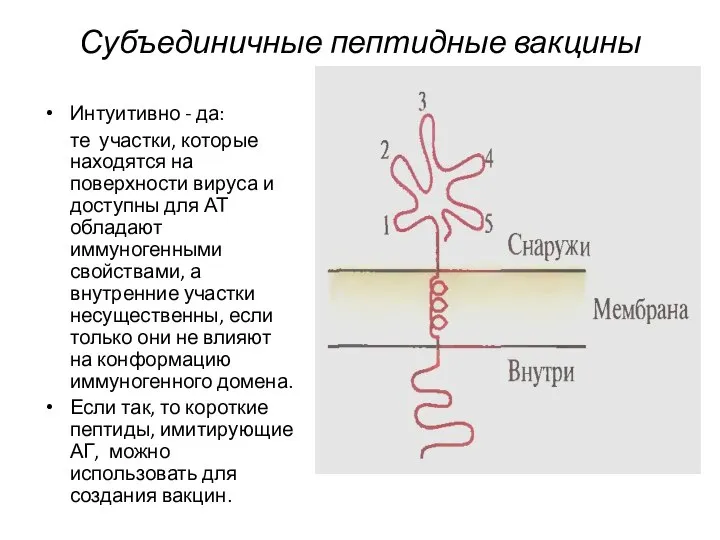
- 19. Субъединичные пептидные вакцины А может ли небольшой участок белковой молекулы (домен) служить субъединичной вакциной и индуцировать
- 20. Субъединичные пептидные вакцины Интуитивно - да: те участки, которые находятся на поверхности вируса и доступны для
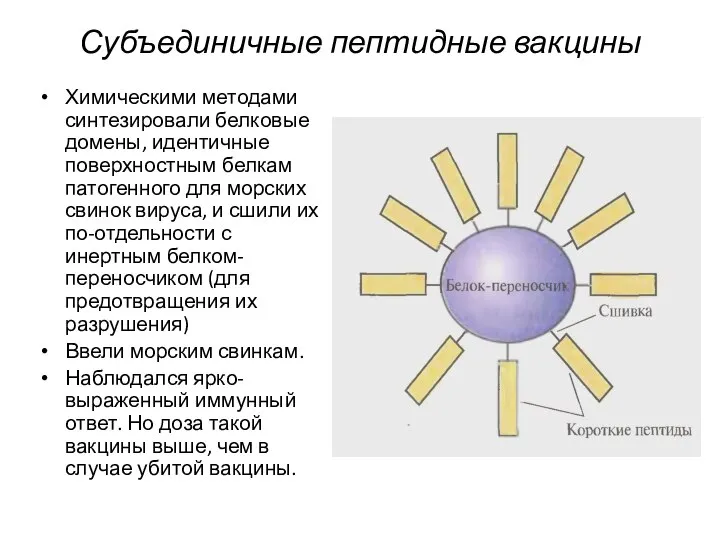
- 21. Субъединичные пептидные вакцины Химическими методами синтезировали белковые домены, идентичные поверхностным белкам патогенного для морских свинок вируса,
- 22. 2. Генетически аттенуированные вакцины Вакцины, содержащие целые живые м/о, но с удаленными генами, кодирующими домены вирулентности
- 23. Создание генетически аттенуированных вакцин Патогенный м/о подвергают генетической модификации: делетируют (delet - удалять) гены, ответственные за
- 24. Создание генетически аттенуированных вакцин Основное требование: эти вакцины, являясь живыми, не должны ревертировать и становиться патогенными.
- 25. Генетически аттенуированная противосальмонеллезная вакцина Разные штаммы Salmonella вызывают острые кишечные инфекции, брюшной тиф, пищевую токсикоинфекцию. Аттенуированные
- 26. Генетически аттенуированная вакцина вибриона холеры Находится в стадии разработки Актуально, т.к. используемая в настоящее время –
- 27. 3. Векторные вакцины Живые вакцины, полученные путем клонирования генов, кодирующих основные АГ патогенного м/о, и встраивания
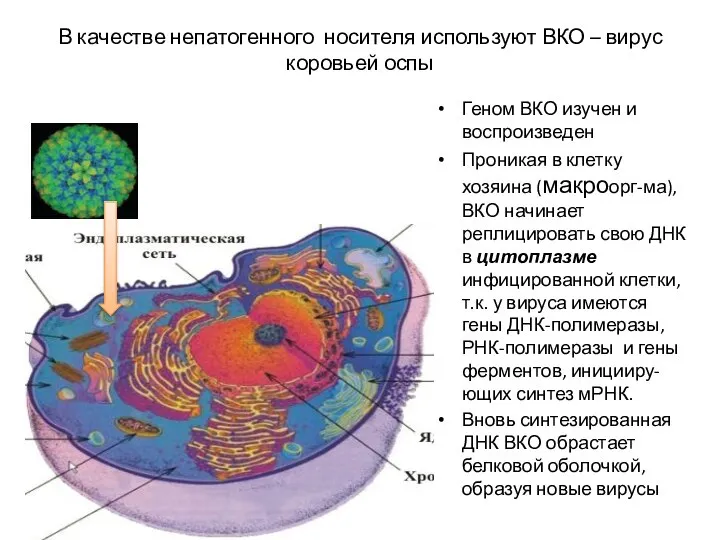
- 28. В качестве непатогенного носителя используют ВКО – вирус коровьей оспы Геном ВКО изучен и воспроизведен Проникая
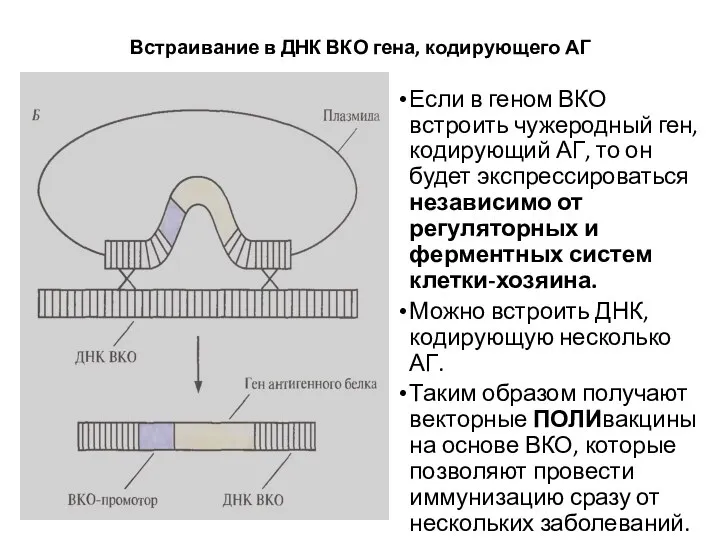
- 29. Встраивание в ДНК ВКО гена, кодирующего АГ Если в геном ВКО встроить чужеродный ген, кодирующий АГ,
- 30. Векторные вакцины на основе ВКО В геном ВКО уже удалось встроить и экспрессировать в культуре животных
- 31. Генная иммунизация Позволяет индуцировать в макроорганизме иммунный ответ без введения АГ Основан на включении в клетки
- 32. Лекарства против СПИДа Вакцина ВИЧ
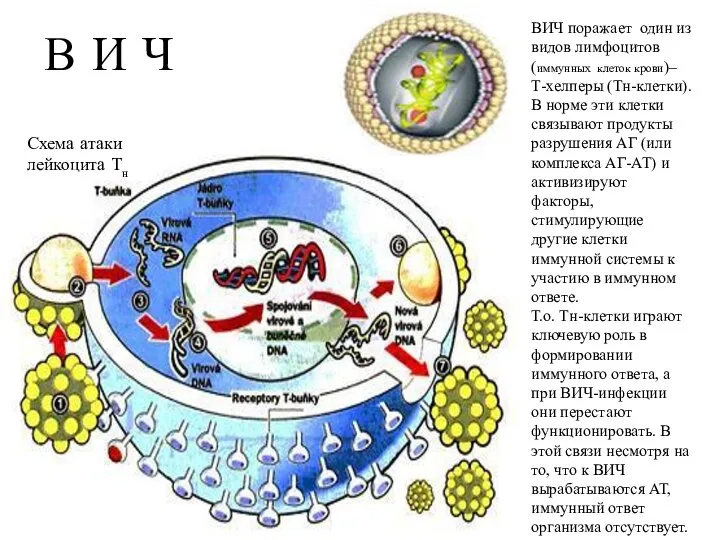
- 33. ВИЧ поражает один из видов лимфоцитов (иммунных клеток крови)– Т-хелперы (Тн-клетки). В норме эти клетки связывают
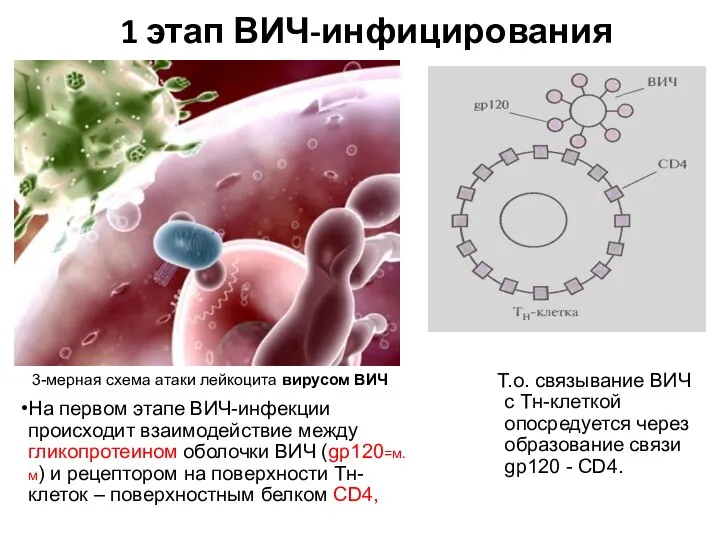
- 34. 1 этап ВИЧ-инфицирования На первом этапе ВИЧ-инфекции происходит взаимодействие между гликопротеином оболочки ВИЧ (gp120=м.м) и рецептором
- 35. 2 этап ВИЧ-инфицирования После связывания с Тн клеткой ВИЧ проникает в нее и становится защищенным от
- 36. Возможные пути защиты Тн-клеток от ВИЧ 1. In vitro поражение вирусом Тн-клеток блокируется антителами к СD4;
- 38. Скачать презентацию























 «РЕБЕНОК УЧИТСЯ ТОМУ, ЧТО ВИДИТ У СЕБЯ В ДОМУ» Родительское собрание в 9 «А» классе 28 февраля 2011 год
«РЕБЕНОК УЧИТСЯ ТОМУ, ЧТО ВИДИТ У СЕБЯ В ДОМУ» Родительское собрание в 9 «А» классе 28 февраля 2011 год Кровь - 2 Защитные системы организма Функции лейкоцитов
Кровь - 2 Защитные системы организма Функции лейкоцитов  Язык и речь
Язык и речь  Проверка параметрических гипотез
Проверка параметрических гипотез Репка. Найди 10 отличий - презентация для начальной школы
Репка. Найди 10 отличий - презентация для начальной школы Презентация Новый год и рождество в Америке
Презентация Новый год и рождество в Америке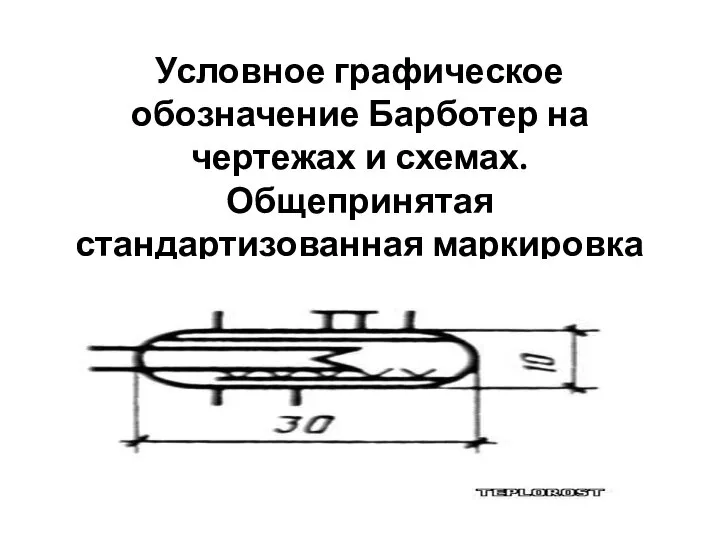 Условное графическое обозначение Барботер на чертежах и схемах
Условное графическое обозначение Барботер на чертежах и схемах Городская ярмарку «ДАРЫ ОСЕНИ» Работы учащихся 3 «Б» класса и их родителей 1 октября 2011 г. г. Пионерский. - презентация
Городская ярмарку «ДАРЫ ОСЕНИ» Работы учащихся 3 «Б» класса и их родителей 1 октября 2011 г. г. Пионерский. - презентация Специальные фильтры
Специальные фильтры Права гражданина РФ. Проверочная работа №7
Права гражданина РФ. Проверочная работа №7 Валютная система и валютный рынок России Выполнили студентки 4 курса группы Э101 Овсянникова Надежда и Орлова Любовь
Валютная система и валютный рынок России Выполнили студентки 4 курса группы Э101 Овсянникова Надежда и Орлова Любовь Презентация на тему "Как не «просмотреть» подростка" - скачать презентации по Педагогике
Презентация на тему "Как не «просмотреть» подростка" - скачать презентации по Педагогике Cоставные части программы, локальные и глобальные переменные. Функции
Cоставные части программы, локальные и глобальные переменные. Функции Город Благовещенск
Город Благовещенск Заработная плата Рынок труда Профсоюзные объединения
Заработная плата Рынок труда Профсоюзные объединения Научно-исследовательская работа по физической культуре на тему «Баскетбол»
Научно-исследовательская работа по физической культуре на тему «Баскетбол» Принципы и приемы практического решения реконструкции. Реконструкция застройки исторического центра города
Принципы и приемы практического решения реконструкции. Реконструкция застройки исторического центра города Проектно - исследовательская работа Мой прадед Выполнила: Ученица 2а класса Школы 7 Гайдышева Екатерина Руководитель проекта: Л.В. Л
Проектно - исследовательская работа Мой прадед Выполнила: Ученица 2а класса Школы 7 Гайдышева Екатерина Руководитель проекта: Л.В. Л Презентация "Немонетаристские методы борьбы с инфляцией" - скачать презентации по Экономике
Презентация "Немонетаристские методы борьбы с инфляцией" - скачать презентации по Экономике Презентация на тему "Кожа и похидни кожи" - скачать презентации по Медицине
Презентация на тему "Кожа и похидни кожи" - скачать презентации по Медицине Включение в работу числовых данных. (Урок 7-8)
Включение в работу числовых данных. (Урок 7-8) Векторные графические редакторы
Векторные графические редакторы Выпускной в УдГУ
Выпускной в УдГУ Разработка бизнес-плана инновационного проекта КОТОВА ОЛЬГА ИВАНОВНА
Разработка бизнес-плана инновационного проекта КОТОВА ОЛЬГА ИВАНОВНА Тема проповеди: «Тайна домофона»
Тема проповеди: «Тайна домофона» Муковисцидоз
Муковисцидоз АО Авиакомпания «Россия». ЭЛТ "КАННАД 406 АС"
АО Авиакомпания «Россия». ЭЛТ "КАННАД 406 АС" Землетрясение. Сейсмостойкое строительство
Землетрясение. Сейсмостойкое строительство