Содержание
- 2. Адиабатический процесс в реакционном объеме Режимы идеального вытеснения и периодический идеального смешения Режим проточный идеального смешения
- 3. Теплообмен с окружающей средой отсутствует Показатели процесса определяются свойствами среды Адиабатический процесс в реакционном объеме
- 4. Математическая модель РИВ и РИС-п при τ = 0, С = С0, Т = Т0 Уравнение
- 5. Уравнение теплового баланса (для простой реакции W(C, T) = –r(C, T) и замены С на х)
- 6. Уравнение теплового баланса (В=0, т.к теплообмен с окружающей средой отсутствует) при τ = 0, х =
- 7. Уравнение материального баланса для сложной реакции Уравнение теплового баланса для сложной реакции РИВ и РИС-п Адиабатический
- 8. Зависимость разогрева системы от степени превращения Зависимость Т (х) линейная и не зависит от вида кинетического
- 9. Зависимость Т (х) - характеристическое уравнение адиабаты ΔТад – температурный коэффициент адиабаты С увеличением конверсии при
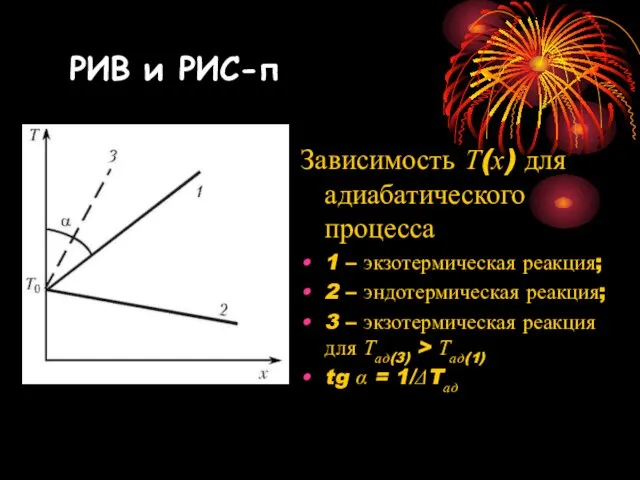
- 10. Зависимость Т(х) для адиабатического процесса 1 – экзотермическая реакция; 2 – эндотермическая реакция; 3 – экзотермическая
- 11. РИВ и РИС-п Величина наклона определяется свойствами системы Чем больше тепловой эффект реакции qp и выше
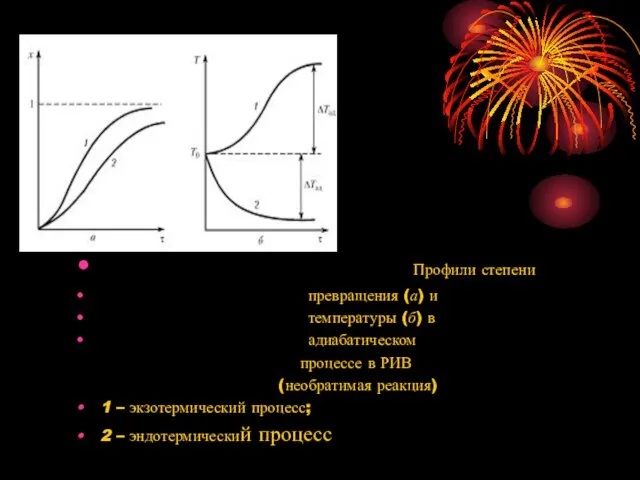
- 12. Профили степени превращения (а) и температуры (б) в адиабатическом процессе в РИВ (необратимая реакция) 1 –
- 13. Для обратимой реакции общий характер зависимостей х(τ) и Т(τ) сохраняется, но процесс будет протекать только до
- 14. Если изотермический процесс будет осуществляться при начальной температуре адиабатического Т0, то адиабатический процесс окажется более интенсивным
- 15. Если температура изотермического процесса будет Т > Т0, то вначале, до достижения в адиабатическом процессе температуры
- 16. Математическая модель РИС-н при τ = 0, С = С0, Т = Т0 Уравнение материального баланса
- 17. Модель адиабатического процесса (при В = 0) Уравнение разогрева системы РИС-н
- 18. Уравнение разогрева в РИС-н совпадает с аналогичным уравнением для РИВ и РИС-н. Во всех режимах при
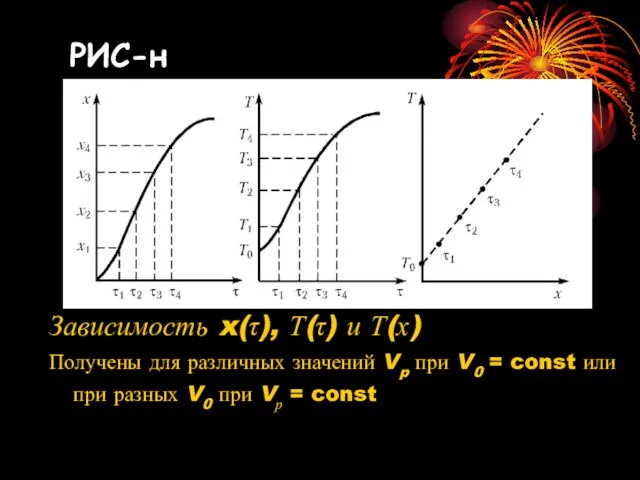
- 19. Зависимость x(τ), Т(τ) и Т(х) Получены для различных значений Vp при V0 = const или при
- 20. Для реакции первого порядка Получаем уравнение, увязывающее устанавливающийся в процессе температурный режим Т с продолжительностью протекания
- 21. Стационарные температурные режимы (1-3) в РИС-н РИС-н
- 22. При низких значениях Т0 будет реализоваться низкотемпературный процесс, при высоких — высокотемпературный. Предельные значения Т0 определяются
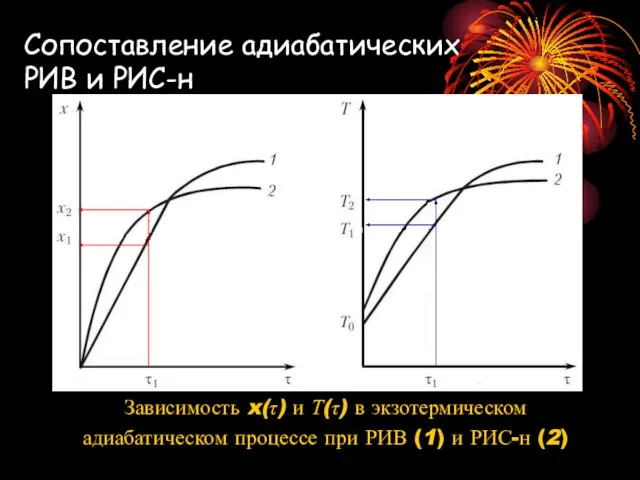
- 23. Сопоставление адиабатических РИВ и РИС-н Зависимость x(τ) и Т(τ) в экзотермическом адиабатическом процессе при РИВ (1)
- 24. Сопоставление адиабатических РИВ и РИС-н В РИС-н процесс протекает при постоянных конечных условиях (температура и концентрация),
- 25. Сопоставление адиабатических РИВ и РИС-н Экзотермический процесс: при одинаковом значении τ1 (Vp = const) в РИС-н
- 26. Сопоставление адиабатических РИВ и РИС-н Эндотермический процесс: Средняя температура в РИВ выше, чем при РИС-н, поэтому
- 27. В адиабатических процессах температурный режим устанавливается самопроизвольно, как следствие протекания реакции без внешнего регулирования. Для практического
- 28. Стационарный режим считается устойчивым, если после устранения источника внесенного возмущения самопроизвольно восстанавливается первоначальное стационарное состояние процесса.
- 29. Расположение зависимостей Qр(Т) и QТ(Т) в стационарном режиме Критические тепловые явления в адиабатическом гетерогенном процессе Стационарный
- 30. Вариант I Если по каким-либо причинам температура процесса Т1 увеличится до Т'1 , то увеличится также
- 31. Вариант II Повышение температуры процесса от Т2 до Т‘2 приведет к более сильному возрастанию тепловыделения Qp,
- 32. Условие устойчивости (вариант I) характерно для низкотемпературных и высокотемпературных режимов (линии 1 и 3), тогда как
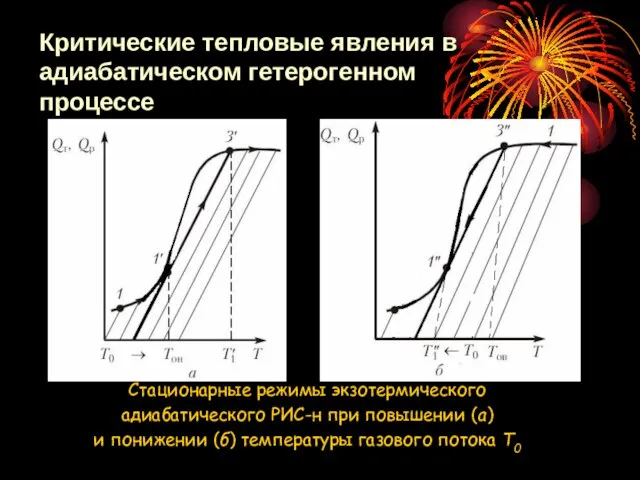
- 33. Стационарные режимы экзотермического адиабатического РИС-н при повышении (а) и понижении (б) температуры газового потока T0 Критические
- 34. Зависимость температуры адиабатического гетерогенного процесса в РИС-н TП от температуры входящего потока T0 TПН – Температура
- 36. Скачать презентацию




























 Презентация по физике "«Криволинейное движение»" - скачать _
Презентация по физике "«Криволинейное движение»" - скачать _ Сила. Явление тяготения. Сила тяжести. Урок физики в 7 классе
Сила. Явление тяготения. Сила тяжести. Урок физики в 7 классе Теория струн и квантовая хромодинамика. Александр Горский, ИТЭФ
Теория струн и квантовая хромодинамика. Александр Горский, ИТЭФ  Массспектрометрическое (МС) секвенирование белков
Массспектрометрическое (МС) секвенирование белков Водяной пар и его свойства
Водяной пар и его свойства Презентация Люминесцентный анализ
Презентация Люминесцентный анализ  Funnel and ball
Funnel and ball Физика пәнінде оптиканың орны және басқа пәндермен байланысы. Жарықтың электромагниттік табиғаты. Лекция 1
Физика пәнінде оптиканың орны және басқа пәндермен байланысы. Жарықтың электромагниттік табиғаты. Лекция 1 Презентация «Рулевое управление»
Презентация «Рулевое управление»  Результаты ЕГЭ по физике по России и в Самарской области
Результаты ЕГЭ по физике по России и в Самарской области Теорема о параллельных осях
Теорема о параллельных осях Линейные цепи постоянного тока
Линейные цепи постоянного тока Физика и детская игрушка (урок – выставка) Гриневич Л.А., учитель физики МОУ СОШ № 1 г. Богданович
Физика и детская игрушка (урок – выставка) Гриневич Л.А., учитель физики МОУ СОШ № 1 г. Богданович Лабораторные работы по физике 8 класс Учитель сош№53 г.Краснодар Меденюк О.В. 2010г г.Краснодар
Лабораторные работы по физике 8 класс Учитель сош№53 г.Краснодар Меденюк О.В. 2010г г.Краснодар Решение задач по теме «Законы Ньютона»
Решение задач по теме «Законы Ньютона» Преобразования сигналов и Вейвлет-преобразование
Преобразования сигналов и Вейвлет-преобразование Задачи по статике. (10 класс)
Задачи по статике. (10 класс) Аттестационная работа. Создание элективного курса «Физика в военной археологии, при проведении поисковых работ»
Аттестационная работа. Создание элективного курса «Физика в военной археологии, при проведении поисковых работ» Генератор, для проверки автомобильных тахометров
Генератор, для проверки автомобильных тахометров Урок физики «Изучение природы гравитационных сил» 9- 10 класс. Игнатова Е.С. Учитель физики МОУ СОШ № 16 г.Кропоткин Краснодарский кр
Урок физики «Изучение природы гравитационных сил» 9- 10 класс. Игнатова Е.С. Учитель физики МОУ СОШ № 16 г.Кропоткин Краснодарский кр Рубка металла
Рубка металла Кристалл және кристалл құрылысы заңдылықтарының физикалық
Кристалл және кристалл құрылысы заңдылықтарының физикалық Звук и его характеристики. (9 класс)
Звук и его характеристики. (9 класс) Трансмиссия в автомобиле
Трансмиссия в автомобиле Источники света. Лекция 12
Источники света. Лекция 12 Пограничный слой и способы управления этим слоем
Пограничный слой и способы управления этим слоем Закон всемирного тяготения. Искусственные спутники Земли. Решение задач
Закон всемирного тяготения. Искусственные спутники Земли. Решение задач Сила упругости. Закон Гука
Сила упругости. Закон Гука