Содержание
- 2. Введено в 1865 году Клаузиусом приведенное количество теплоты, сообщаемое телу на бесконечно малом участке процесса, когда
- 3. Приведенная теплота – функция состояния, для которой не важен путь, по которому идет процесс Термодинамическая энтропия
- 4. Энтропия определяется c точностью до некоторой постоянной Физический смысл имеет разность энтропий
- 7. Адиабатический процесс
- 8. Энтропия обладает свойством аддитивности: энтропия нескольких газов равна сумме энтропий каждого газа в отдельности
- 9. Рассмотрим теплоизолированный сосуд, разделенный перегородкой на 2 части. 1- 2-
- 10. Перегородку убирают Газы перемешиваются Найдем температуру после перемешивания (равновесного состояния)
- 11. Если то
- 12. Для 1 газа изменение энтропии Для 2 газа изменение энтропии
- 14. Если то Энтропия увеличилась!
- 15. Статистическое определение энтропии Пусть имеется сосуд, разделенный перегородкой на 2 части и 2 молекулы
- 17. Если молекул N, то их можно распределить между двумя половинками способами
- 18. Термодинамической вероятностью (W) наз число способов, с помощью которых может быть реализовано данное макросостояние системы. Пример:
- 19. Энтропия Больцман Мера вероятности данного состояния газа Указывает направление протекания самопроизвольных процессов
- 20. Первое начало термодинамики – закон сохранения энергии Не указывает направление протекания процессов Из определения энтропии следует,
- 21. В замкнутых системах при необратимых процессах энтропия всегда возрастает Процесс идет от менее вероятного к более
- 22. Закон возрастания энтропии Второе начало термодинамики указывает направление протекания обратимых и необратимых процессов Неравенство Клаузиуса
- 23. ЦИКЛ КАРНО Наиболее экономичный цикл теплового двигателя. Состоит из 2 изотерм и двух адиабат
- 24. P V T1 T2 1 2 3 4 12-изотермическое расширение 23-адиабатичческое расширение 34-изотермическое сжатие 41-адиабатичческое сжатие
- 29. К.п.д. цикла Карно определяется только температурами нагревателя и холодильника
- 30. Т S Q Tеплота в осях температура и энтропия – это площадь под кривой
- 31. Пример: Найти к.п.д. цикла Т S 1 2 3 12- Тепло получается Q1 23- Тепло отдается
- 32. Т S 1 2 3 T1 T2 Q1
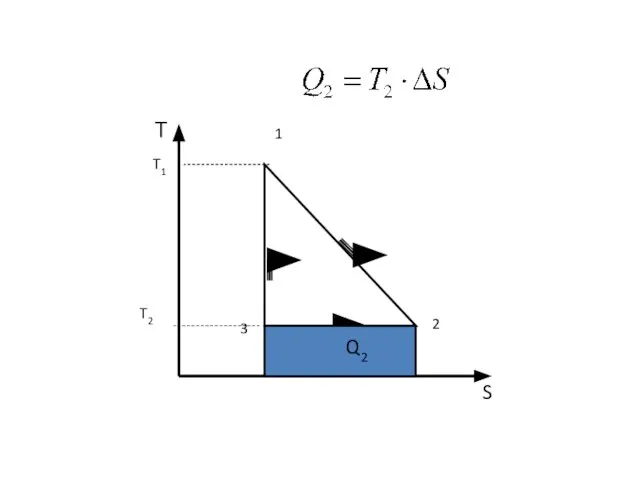
- 33. Т S 1 2 3 T1 T2 Q2
- 35. Цикл Карно в осях температура и энтропия Т S T1 T2 Q1 Q2
- 36. Т S T1 Q1
- 37. S T2
- 39. Скачать презентацию











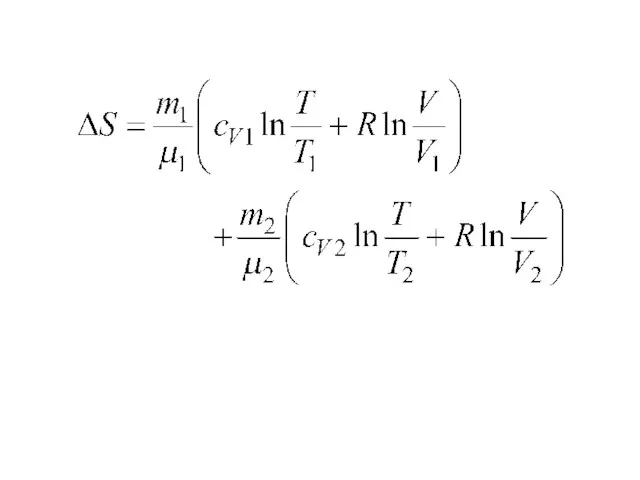











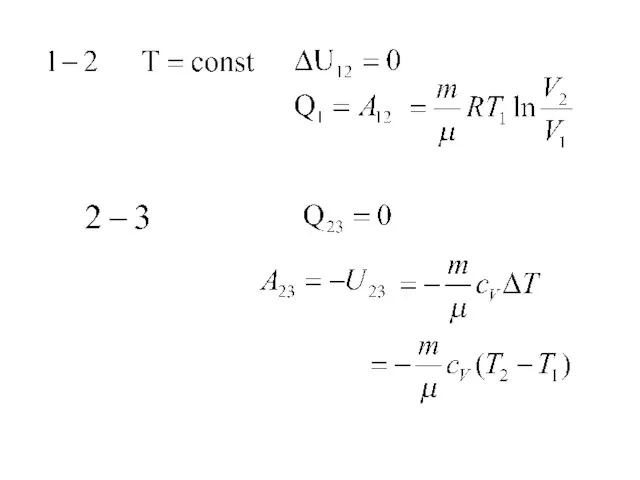

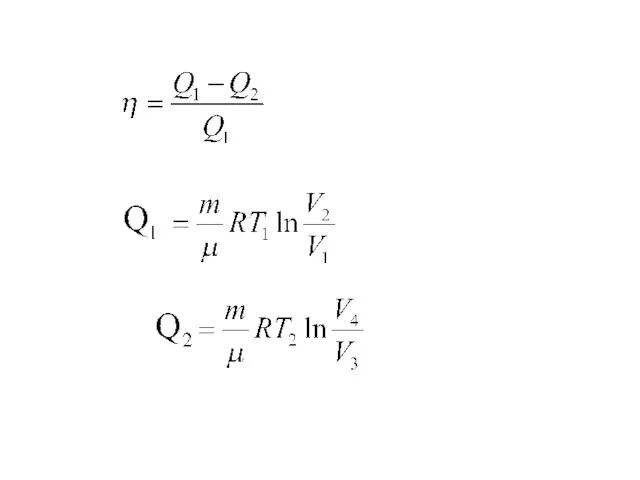









 Електричне поле. Напруженість електричного поля
Електричне поле. Напруженість електричного поля Упругие волны. Электромагнитные волны
Упругие волны. Электромагнитные волны Система дизельного впрыска
Система дизельного впрыска Электропроводность кристаллов
Электропроводность кристаллов Малоразмерный газотурбинный двигатель мощностью 150 кВт
Малоразмерный газотурбинный двигатель мощностью 150 кВт Принцип возможных перемещений (§1 - §6)
Принцип возможных перемещений (§1 - §6) Вакуумные приборы
Вакуумные приборы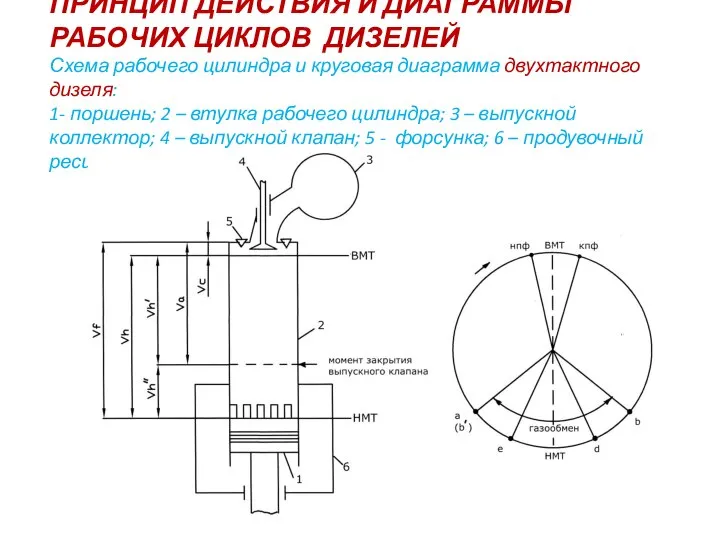 Принцип действия и диаграммы рабочих циклов дизелей. Схема рабочего цилиндра и круговая диаграмма двухтактного дизеля
Принцип действия и диаграммы рабочих циклов дизелей. Схема рабочего цилиндра и круговая диаграмма двухтактного дизеля Динаміка матеріальної точки та поступального руху
Динаміка матеріальної точки та поступального руху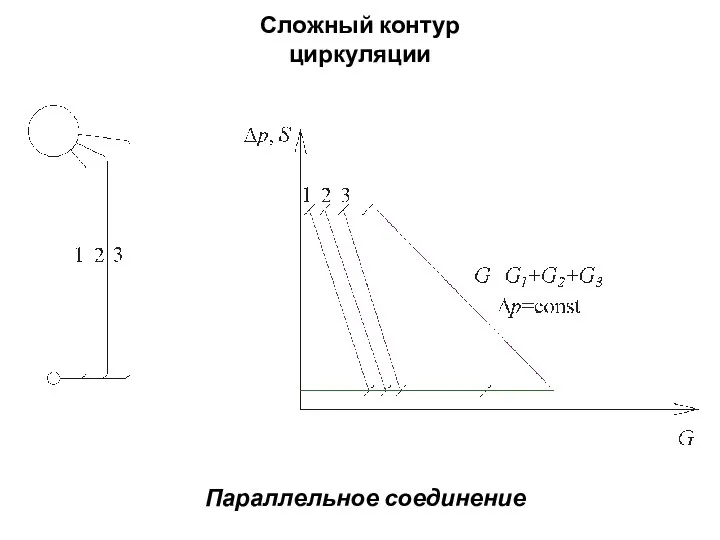 Сложный контур циркуляции
Сложный контур циркуляции Механика. Механическое движение
Механика. Механическое движение Динамика материальной точки
Динамика материальной точки Брейн-ринг «Юные знатоки физики»
Брейн-ринг «Юные знатоки физики» Молекулярно-кинетическая теория газов. (Лекция 2)
Молекулярно-кинетическая теория газов. (Лекция 2) Моделирование равноускоренного движения в электронных таблицах Интегрированный урок в 9-ом классе по темам: Физика – «Равноуско
Моделирование равноускоренного движения в электронных таблицах Интегрированный урок в 9-ом классе по темам: Физика – «Равноуско Энергия. Кинетическая и потенциальная энергия
Энергия. Кинетическая и потенциальная энергия Электромагнитное взаимодействие
Электромагнитное взаимодействие Влияние солнечных рентгеновских вспышек на изменения атмосферного электрического поля и прохождение волн СДВ диапазона
Влияние солнечных рентгеновских вспышек на изменения атмосферного электрического поля и прохождение волн СДВ диапазона Сила трения
Сила трения Озоновый слой атмосферы и озоновые дыры
Озоновый слой атмосферы и озоновые дыры Радиоактивность. Строение атома
Радиоактивность. Строение атома Кинематика. Вращательное движение
Кинематика. Вращательное движение Сталь марки 38ха
Сталь марки 38ха Электродинамика. Электрические и магнитные явления
Электродинамика. Электрические и магнитные явления Задачи на смеси, сплавы и растворы
Задачи на смеси, сплавы и растворы Ядерная геофизика
Ядерная геофизика Методы решения задач теплопроводности
Методы решения задач теплопроводности Анализ питьевых вод
Анализ питьевых вод