Содержание
- 2. ХТП с взаимодействием газообразных и жидких компонентов очень разнообразны. К ним относят: 1. Абсорбцию газов жидкостями,
- 3. Пусть газовая смесь, содержащая вещество А, взаимодействует с жидкостью, содержащей вещество В. При этом А и
- 4. I V
- 5. В рассматриваемой системе реакции протекают в основном в жидкой фазе. В общем случае химической реакции предшествует
- 6. На рис. показан характер изменения концентраций реагентов А и В и продукта D в пограничных пленках
- 7. . Продукт D накапливается в слое толщиной а до некоторой концентрации и диффундирует в поток жидкости.
- 8. Процесс
- 9. Коэффициент массопередачи Кm равен где βg –коэффициент массоотдачи со стороны газа; βL- коэффициент массоотдачи со стороны
- 11. Скачать презентацию
Слайд 2
ХТП с взаимодействием газообразных и жидких компонентов очень разнообразны. К ним
относят: 1. Абсорбцию газов жидкостями, в том числе сопровождающуюся химической реакцией; десорбцию газов.
2. Процессы, сопровождающиеся химической реакцией при взаимодействии несмешивающихся жидкостей, используют во многих производствах органического синтеза. Например, к ним относятся процессы сульфирования и нитрования, ароматических соединений растворами неорганических кислот.
2. Процессы, сопровождающиеся химической реакцией при взаимодействии несмешивающихся жидкостей, используют во многих производствах органического синтеза. Например, к ним относятся процессы сульфирования и нитрования, ароматических соединений растворами неорганических кислот.
Слайд 3
Пусть газовая смесь, содержащая вещество А, взаимодействует с жидкостью, содержащей вещество
Пусть газовая смесь, содержащая вещество А, взаимодействует с жидкостью, содержащей вещество
В. При этом А и В должны химически прореагировать между собой:
А (г.) + В (ж.) =D(ж.)
А (г.) + В (ж.) =D(ж.)
Слайд 4
I
V
I
V
Слайд 5
В рассматриваемой системе реакции протекают в основном в жидкой фазе. В
В рассматриваемой системе реакции протекают в основном в жидкой фазе. В
общем случае химической реакции предшествует стадия доставки газообразных реагентов диффузией их в газовой смеси к поверхности раздела фаз и растворение в жидкости.
Такова простейшая мысленная модель протекания основных этапов процесса.
Для количественного описания таких процессов широко используют пленочную модель, согласно которой по обе стороны межфазной поверхности Г(Ж)-Ж существует ламинарная пограничная пленка. Скорость диффузии через пленку прямо пропорциональна разности концентраций по обе стороны пленки и обратно пропорциональна ее толщине. Предполагается, что на поверхности контакта фаз устанавливается равновесие между концентрацией поглощаемого компонента в жидкой и газовой фазе.
Такова простейшая мысленная модель протекания основных этапов процесса.
Для количественного описания таких процессов широко используют пленочную модель, согласно которой по обе стороны межфазной поверхности Г(Ж)-Ж существует ламинарная пограничная пленка. Скорость диффузии через пленку прямо пропорциональна разности концентраций по обе стороны пленки и обратно пропорциональна ее толщине. Предполагается, что на поверхности контакта фаз устанавливается равновесие между концентрацией поглощаемого компонента в жидкой и газовой фазе.
Слайд 6
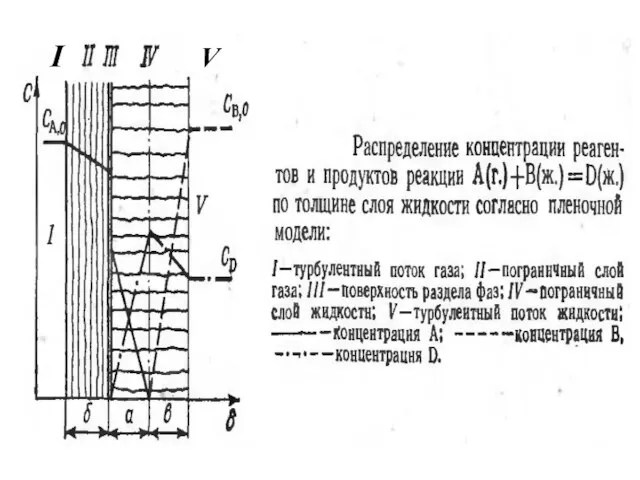
На рис. показан характер изменения концентраций реагентов А и В и
На рис. показан характер изменения концентраций реагентов А и В и
продукта D в пограничных пленках согласно пленочной модели для случая, когда скорость диффузии соизмерима со скоростью реакции. Концентрация В в жидкости равна Св.о, компонента А-отсутствует. Вследствие этого он диффундирует через пограничный слой газа II, поверхность раздела фаз III, пограничный слой жидкости IV и в нем вступает в химическую реакцию с В, образуя продукт D При этом концентрация А уменьшается до нуля к моменту окончания реакции на расстоянии а от поверхности раздела фаз. Компонент В диффундирует сквозь жидкий пограничный слой в направлении поверхности раздела фаз. Его концентрация уменьшается и на расстоянии b становится равна нулю
Слайд 7
. Продукт D накапливается в слое толщиной а до некоторой концентрации
. Продукт D накапливается в слое толщиной а до некоторой концентрации
и диффундирует в поток жидкости.
При увеличении скорости химической реакции и уменьшении скорости диффузии а стремиться к нулю. При малой скорости реакции и высокой скорости диффузии реакция заканчивается в зоне турбулентного потока жидкости (зона V).
Расчет процесса сводится к составлению и решению системы уравнений скорости диффузии реагентов А и В через пограничные слои и скорости химической реакции при соответствующих граничных условиях.
При увеличении скорости химической реакции и уменьшении скорости диффузии а стремиться к нулю. При малой скорости реакции и высокой скорости диффузии реакция заканчивается в зоне турбулентного потока жидкости (зона V).
Расчет процесса сводится к составлению и решению системы уравнений скорости диффузии реагентов А и В через пограничные слои и скорости химической реакции при соответствующих граничных условиях.
Слайд 8
Процесс
Процесс
Слайд 9
Коэффициент массопередачи Кm равен
где βg –коэффициент массоотдачи со стороны газа;
βL-
Коэффициент массопередачи Кm равен
где βg –коэффициент массоотдачи со стороны газа;
βL-
коэффициент массоотдачи со стороны жидкости;
НL- константа Генри;
ε- коэффициент ускорения при наличии химической реакции (пропорционален константе скорости реакции k).
НL- константа Генри;
ε- коэффициент ускорения при наличии химической реакции (пропорционален константе скорости реакции k).
- Предыдущая
Working PlanСледующая -
Путешествие по стране творчества ДЕКУПАЖ






 Спин и магнитный момент электрона
Спин и магнитный момент электрона Методы микроскопии
Методы микроскопии Переменные, влияющие на экспозицию
Переменные, влияющие на экспозицию Сила взаимодействия молекул
Сила взаимодействия молекул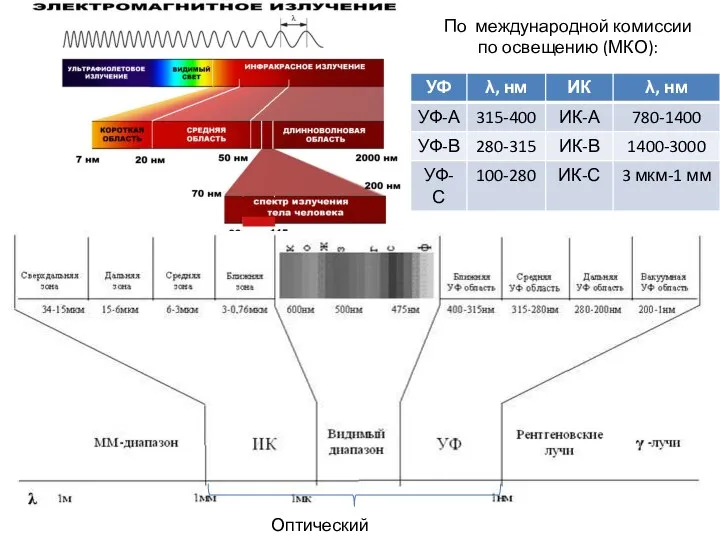 Электромагнитное излучение
Электромагнитное излучение Специальная теория относительности
Специальная теория относительности Антивещество. Античастицы. Получение и свойства антивещества
Антивещество. Античастицы. Получение и свойства антивещества Роль физико-химических методов анализа потребительских товаров при установлении их безопасности и качества
Роль физико-химических методов анализа потребительских товаров при установлении их безопасности и качества Создание фонтанов
Создание фонтанов Сушка обмоток после пропитки
Сушка обмоток после пропитки Атом водорода в квантовой механике
Атом водорода в квантовой механике Электростатика, как раздел электродинамики
Электростатика, как раздел электродинамики Технологии, применяемые при ремонте автомобилей. Ремонт коробок передач, раздаточных коробок и карданных валов. (Тема 9.7)
Технологии, применяемые при ремонте автомобилей. Ремонт коробок передач, раздаточных коробок и карданных валов. (Тема 9.7) Кравцова Инна Александровна учитель 1 квалификационной категории МБОУ СОШ № 151 Г.Новосибирск
Кравцова Инна Александровна учитель 1 квалификационной категории МБОУ СОШ № 151 Г.Новосибирск  Движение тел по наклонной плоскости. Решение задач
Движение тел по наклонной плоскости. Решение задач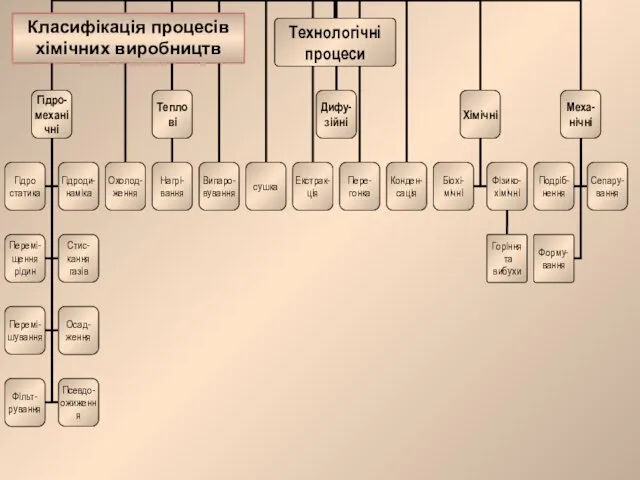 Класифікація процесів хімічних виробництв
Класифікація процесів хімічних виробництв Молекулы. Молекулярные спектры излучения и поглощения. Адиабатическое приближение. Термы двухатомной молекул
Молекулы. Молекулярные спектры излучения и поглощения. Адиабатическое приближение. Термы двухатомной молекул Расчетно-графическая работа №2
Расчетно-графическая работа №2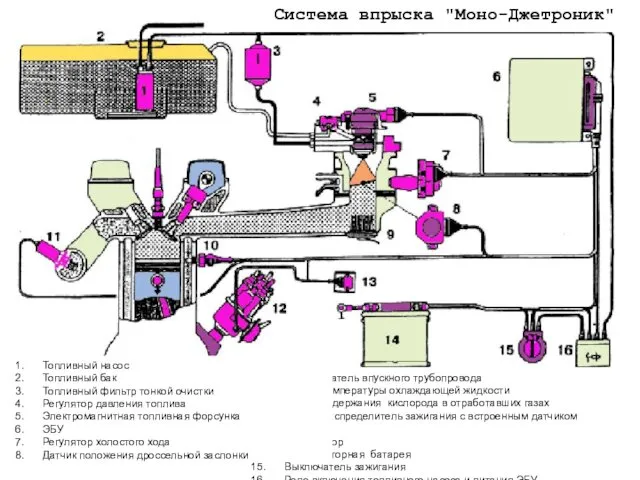 Система впрыска Моно-Джетроник
Система впрыска Моно-Джетроник Строение атома Квантовая теория строения атома
Строение атома Квантовая теория строения атома Атомно-абсорбционная спектрометрия
Атомно-абсорбционная спектрометрия Презентация по физике "Знакомые незнакомцы (влияние звуков природы на состояние человека)" - скачать
Презентация по физике "Знакомые незнакомцы (влияние звуков природы на состояние человека)" - скачать  Динамика. Введение.Основные законы динамики. Две задачи динамики
Динамика. Введение.Основные законы динамики. Две задачи динамики Пути повышения качества физической подготовки обучающихся на уроках физической культуры и во внеурочное время
Пути повышения качества физической подготовки обучающихся на уроках физической культуры и во внеурочное время Ньютон. Совершенны ли законы Ньютона?
Ньютон. Совершенны ли законы Ньютона? История создания швейной машины, их виды
История создания швейной машины, их виды Итоговый проект «Радиация вокруг нас»
Итоговый проект «Радиация вокруг нас» Аттестационная работа. Практика проектно-исследовательской деятельности по физике и астрономии
Аттестационная работа. Практика проектно-исследовательской деятельности по физике и астрономии