Содержание
- 2. Молекулярно-кинетическая теория Молекулярно-кинетической теорией называют учение о строении и свойствах вещества на основе представления о существовании
- 3. Наиболее ярким экспериментальным подтверждением представлений молекулярно-кинетической теории о беспорядочном движении атомов и молекул является броуновское движение.
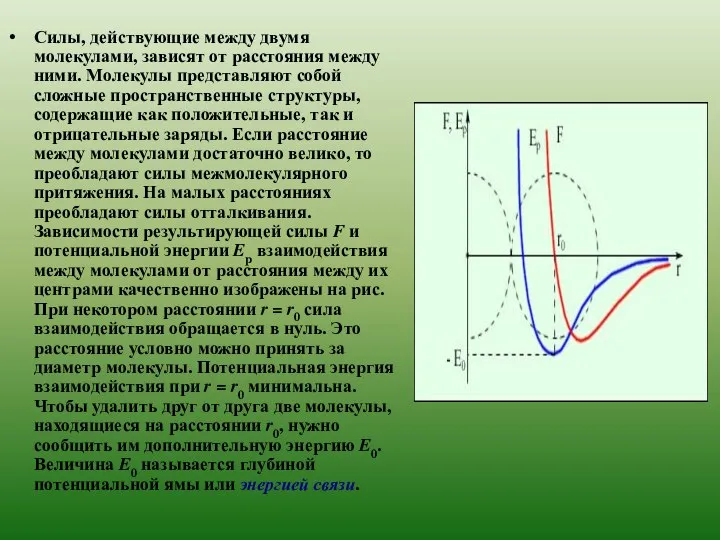
- 4. Силы, действующие между двумя молекулами, зависят от расстояния между ними. Молекулы представляют собой сложные пространственные структуры,
- 5. Беспорядочное хаотическое движение молекул называется тепловым движением. Кинетическая энергия теплового движения растет с возрастанием температуры. При
- 6. В газах расстояния между молекулами обычно значительно больше их размеров. Силы взаимодействия между молекулами на таких
- 7. Количество вещества ν определяется как отношение числа N частиц (молекул) вещества к постоянной Авогадро NA: Массу
- 8. Основное уравнение МКТ газов. Температура Простейшей моделью молекулярно-кинетической теории является модель идеального газа. В кинетической модели
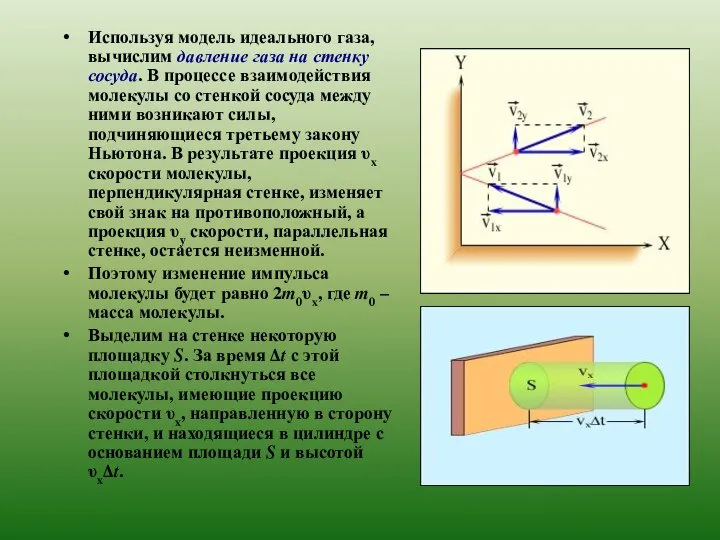
- 9. Используя модель идеального газа, вычислим давление газа на стенку сосуда. В процессе взаимодействия молекулы со стенкой
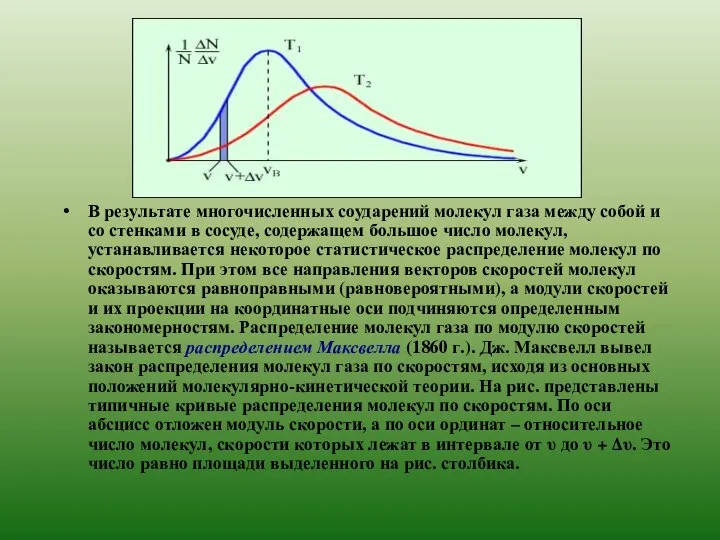
- 10. В результате многочисленных соударений молекул газа между собой и со стенками в сосуде, содержащем большое число
- 11. Характерными параметрами распределения Максвелла являются наиболее вероятная скорость υв, соответствующая максимуму кривой распределения, и среднеквадратичная скорость
- 12. Формула для среднего давления газа на стенку сосуда запишется в виде Это уравнение устанавливает связь между
- 13. Тепловое равновесие – это такое состояние системы тел, находящихся в тепловом контакте, при котором не происходит
- 14. Особое место в физике занимают газовые термометры (рис.), в которых термометрическим веществом является разреженный газ (гелий,
- 15. В системе СИ принято единицу измерения температуры по шкале Кельвина называть кельвином и обозначать буквой K.
- 17. Скачать презентацию
Молекулярно-кинетическая теория
Молекулярно-кинетической теорией называют учение о строении и свойствах вещества на
Молекулярно-кинетическая теория
Молекулярно-кинетической теорией называют учение о строении и свойствах вещества на
В основе молекулярно-кинетической теории лежат три основных положения:
1. Все вещества – жидкие, твердые и газообразные – образованы из мельчайших частиц – молекул, которые сами состоят из атомов («элементарных молекул»). Молекулы химического вещества могут быть простыми и сложными и состоять из одного или нескольких атомов. Молекулы и атомы представляют собой электрически нейтральные частицы. При определенных условиях молекулы и атомы могут приобретать дополнительный электрический заряд и превращаться в положительные или отрицательные ионы.
2. Атомы и молекулы находятся в непрерывном хаотическом движении.
3. Частицы взаимодействуют друг с другом силами, имеющими электрическую природу. Гравитационное взаимодействие между частицами пренебрежимо мало.
Наиболее ярким экспериментальным подтверждением представлений молекулярно-кинетической теории о беспорядочном движении атомов
Наиболее ярким экспериментальным подтверждением представлений молекулярно-кинетической теории о беспорядочном движении атомов
Силы, действующие между двумя молекулами, зависят от расстояния между ними. Молекулы
Силы, действующие между двумя молекулами, зависят от расстояния между ними. Молекулы
Беспорядочное хаотическое движение молекул называется тепловым движением. Кинетическая энергия теплового движения
Беспорядочное хаотическое движение молекул называется тепловым движением. Кинетическая энергия теплового движения
В твердых телах молекулы совершают беспорядочные колебания около фиксированных центров (положений равновесия). Эти центры могут быть расположены в пространстве нерегулярным образом (аморфные тела) или образовывать упорядоченные объемные структуры (кристаллические тела).
В жидкостях молекулы имеют значительно большую свободу для теплового движения. Они не привязаны к определенным центрам и могут перемещаться по всему объему жидкости. Этим объясняется текучесть жидкостей. Близко расположенные молекулы жидкости также могут образовывать упорядоченные структуры, содержащие несколько молекул. Это явление называется ближним порядком в отличие от дальнего порядка, характерного для кристаллических тел.
В газах расстояния между молекулами обычно значительно больше их размеров. Силы
В газах расстояния между молекулами обычно значительно больше их размеров. Силы
В молекулярно-кинетической теории количество вещества принято считать пропорциональным числу частиц. Единица количества вещества называется молем (моль).
Моль – это количество вещества, содержащее столько же частиц (молекул), сколько содержится атомов в 0,012 кг углерода 12C. Молекула углерода состоит из одного атома.
Таким образом, в одном моле любого вещества содержится одно и то же число частиц (молекул). Это число называется постоянной Авогадро NA:
NA = 6,02·1023 моль–1.
Количество вещества ν определяется как отношение числа N частиц (молекул) вещества
Количество вещества ν определяется как отношение числа N частиц (молекул) вещества
Массу одного моля вещества принято называть молярной массой M. Молярная масса равна произведению массы m0 одной молекулы данного вещества на постоянную Авогадро:
M = NA · m0.
Молярная масса выражается в килограммах на моль (кг/моль). Для веществ, молекулы которых состоят из одного атома, часто используется термин атомная масса.
За единицу массы атомов и молекул принимается 1/12 массы атома изотопа углерода 12C (с массовым числом 12). Она называется атомной единицей массы (а. е. м.):
1 а. е. м. = 1,66·10–27 кг.
Основное уравнение МКТ газов. Температура
Простейшей моделью молекулярно-кинетической теории является модель
Основное уравнение МКТ газов. Температура
Простейшей моделью молекулярно-кинетической теории является модель
Используя модель идеального газа, вычислим давление газа на стенку сосуда. В
Используя модель идеального газа, вычислим давление газа на стенку сосуда. В
Поэтому изменение импульса молекулы будет равно 2m0υx, где m0 – масса молекулы.
Выделим на стенке некоторую площадку S. За время Δt с этой площадкой столкнуться все молекулы, имеющие проекцию скорости υx, направленную в сторону стенки, и находящиеся в цилиндре с основанием площади S и высотой υxΔt.
В результате многочисленных соударений молекул газа между собой и со стенками
В результате многочисленных соударений молекул газа между собой и со стенками
Характерными параметрами распределения Максвелла являются наиболее вероятная скорость υв, соответствующая максимуму
Характерными параметрами распределения Максвелла являются наиболее вероятная скорость υв, соответствующая максимуму
С ростом температуры максимум кривой распределения смещается в сторону больших скоростей, при этом υв и υкв увеличиваются.
Чтобы уточнить формулу для давления газа на стенку сосуда, предположим, что все молекулы, содержащиеся в единице объема, разбиты на группы, содержащие n1, n2, n3 и т. д. молекул с проекциями скоростей υx1, υx2, υx3 и т. д. соответственно. Каждая группа молекул вносит свой вклад в давление газа. В результате соударений со стенкой молекул с различными значениями проекций υxi скоростей возникает суммарное давление
Формула для среднего давления газа на стенку сосуда запишется в виде
Формула для среднего давления газа на стенку сосуда запишется в виде
Это уравнение устанавливает связь между давлением p идеального газа, массой молекулы m0, концентрацией молекул n, средним значением квадрата скорости и средней кинетической энергией поступательного движения молекул. Его называют основным уравнением молекулярно-кинетической теории газов.
давление газа равно двум третям средней кинетической энергии поступательного движения молекул, содержащихся в единице объема.
Тепловое равновесие – это такое состояние системы тел, находящихся в тепловом
Тепловое равновесие – это такое состояние системы тел, находящихся в тепловом
Для измерения температуры используются физические приборы – термометры, в которых о величине температуры судят по изменению какого-либо физического параметра. Для создания термометра необходимо выбрать термометрическое вещество (например, ртуть, спирт) и термометрическую величину, характеризующую свойство вещества (например, длина ртутного или спиртового столбика). В различных конструкциях термометров используются разнообразные физические свойства вещества (например, изменение линейных размеров твердых тел или изменение электрического сопротивления проводников при нагревании).
Особое место в физике занимают газовые термометры (рис.), в которых термометрическим
Особое место в физике занимают газовые термометры (рис.), в которых термометрическим
В системе СИ принято единицу измерения температуры по шкале Кельвина называть
В системе СИ принято единицу измерения температуры по шкале Кельвина называть
Температурная шкала Кельвина называется абсолютной шкалой температур. Она оказывается наиболее удобной при построении физических теорий.
Кроме точки нулевого давления газа, которая называется абсолютным нулем температуры, достаточно принять еще одну фиксированную опорную точку. В шкале Кельвина в качестве такой точки используется температура тройной точки воды (0,01° С), в которой в тепловом равновесии находятся все три фазы – лед, вода и пар. По шкале Кельвина температура тройной точки принимается равной 273,16 К.
Таким образом, давление разреженного газа в сосуде постоянного объема V изменяется прямо пропорционально его абсолютной температуре: p ~ T. С другой стороны, опыт показывает, что при неизменных объеме V и температуре T давление газа изменяется прямо пропорционально отношению количества вещества ν в данном сосуде к объему V сосуда











 Спин и магнитный момент электрона
Спин и магнитный момент электрона Методы микроскопии
Методы микроскопии Переменные, влияющие на экспозицию
Переменные, влияющие на экспозицию Сила взаимодействия молекул
Сила взаимодействия молекул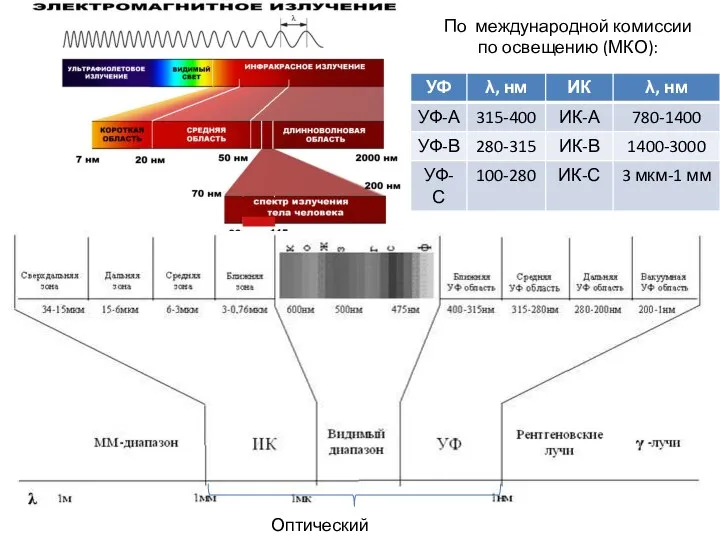 Электромагнитное излучение
Электромагнитное излучение Специальная теория относительности
Специальная теория относительности Антивещество. Античастицы. Получение и свойства антивещества
Антивещество. Античастицы. Получение и свойства антивещества Роль физико-химических методов анализа потребительских товаров при установлении их безопасности и качества
Роль физико-химических методов анализа потребительских товаров при установлении их безопасности и качества Создание фонтанов
Создание фонтанов Сушка обмоток после пропитки
Сушка обмоток после пропитки Атом водорода в квантовой механике
Атом водорода в квантовой механике Электростатика, как раздел электродинамики
Электростатика, как раздел электродинамики Технологии, применяемые при ремонте автомобилей. Ремонт коробок передач, раздаточных коробок и карданных валов. (Тема 9.7)
Технологии, применяемые при ремонте автомобилей. Ремонт коробок передач, раздаточных коробок и карданных валов. (Тема 9.7) Кравцова Инна Александровна учитель 1 квалификационной категории МБОУ СОШ № 151 Г.Новосибирск
Кравцова Инна Александровна учитель 1 квалификационной категории МБОУ СОШ № 151 Г.Новосибирск  Движение тел по наклонной плоскости. Решение задач
Движение тел по наклонной плоскости. Решение задач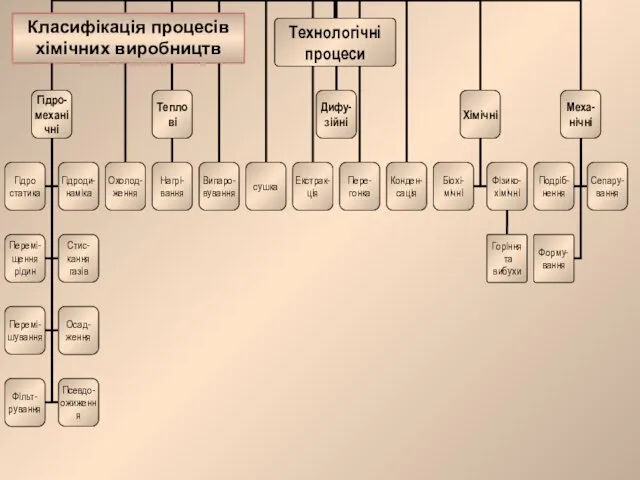 Класифікація процесів хімічних виробництв
Класифікація процесів хімічних виробництв Молекулы. Молекулярные спектры излучения и поглощения. Адиабатическое приближение. Термы двухатомной молекул
Молекулы. Молекулярные спектры излучения и поглощения. Адиабатическое приближение. Термы двухатомной молекул Расчетно-графическая работа №2
Расчетно-графическая работа №2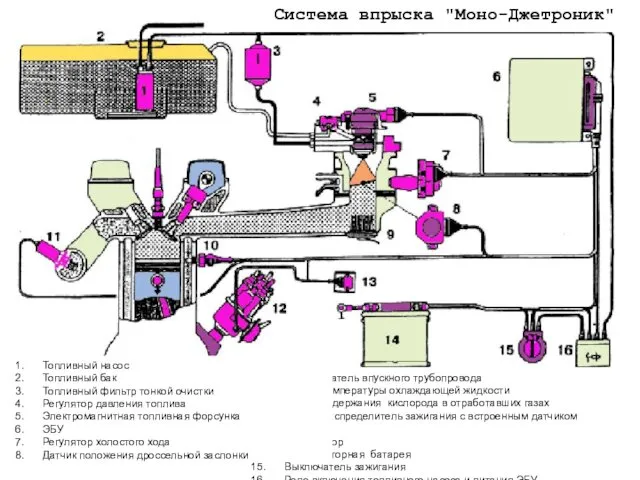 Система впрыска Моно-Джетроник
Система впрыска Моно-Джетроник Строение атома Квантовая теория строения атома
Строение атома Квантовая теория строения атома Атомно-абсорбционная спектрометрия
Атомно-абсорбционная спектрометрия Презентация по физике "Знакомые незнакомцы (влияние звуков природы на состояние человека)" - скачать
Презентация по физике "Знакомые незнакомцы (влияние звуков природы на состояние человека)" - скачать  Динамика. Введение.Основные законы динамики. Две задачи динамики
Динамика. Введение.Основные законы динамики. Две задачи динамики Пути повышения качества физической подготовки обучающихся на уроках физической культуры и во внеурочное время
Пути повышения качества физической подготовки обучающихся на уроках физической культуры и во внеурочное время Ньютон. Совершенны ли законы Ньютона?
Ньютон. Совершенны ли законы Ньютона? История создания швейной машины, их виды
История создания швейной машины, их виды Итоговый проект «Радиация вокруг нас»
Итоговый проект «Радиация вокруг нас» Аттестационная работа. Практика проектно-исследовательской деятельности по физике и астрономии
Аттестационная работа. Практика проектно-исследовательской деятельности по физике и астрономии