Содержание
- 2. Цель урока: Установить взаимосвязь между макроскопическими и микроскопическими параметрами Научиться решать вычислительные задачи с использованием основного
- 3. Макроскопические – параметры, которые можно измерить с помощью приборов. Микроскопические – параметры, которые измеряются косвенным путем.
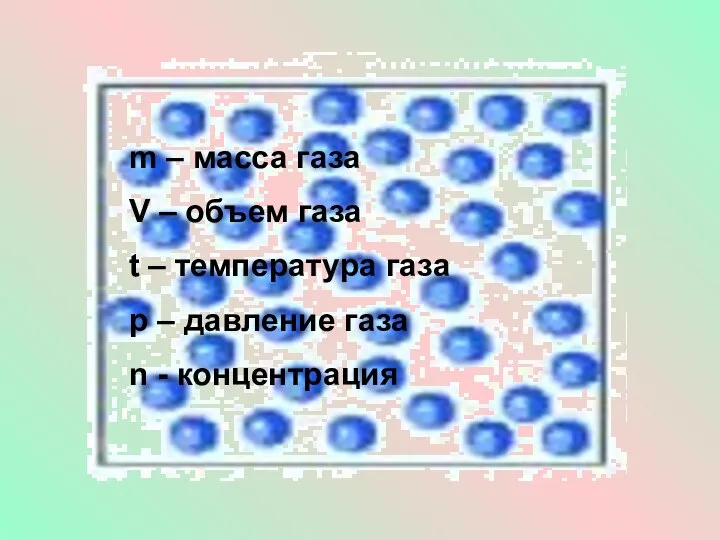
- 4. m – масса газа V – объем газа t – температура газа p – давление газа
- 6. Модель идеального газа 1. Межмолекулярные силы притяжения отсутствуют (можно пренебречь потенциальной энергией) 2. Взаимодействия молекул газа
- 8. Это уравнение, выведенное впервые немецким физиком Р. Клаузиусом, называется основным уравнением молекулярно-кинетической теории идеального газа. Оно
- 9. Учитывая, что - средняя кинетическая энергия молекулы газа, получим:
- 10. Давление идеального газа прямо пропорционально средней кинетической энергии поступательного движения молекул, содержащихся в единице объема газа.
- 12. Задача №1. Каково давление азота, если средняя квадратичная скорость его молекул 500 м/с, а его плотность
- 14. Задача №2. Имеются два одинаковых сосуда. В одном из них находится кислород, а в другом азот.
- 16. Скачать презентацию







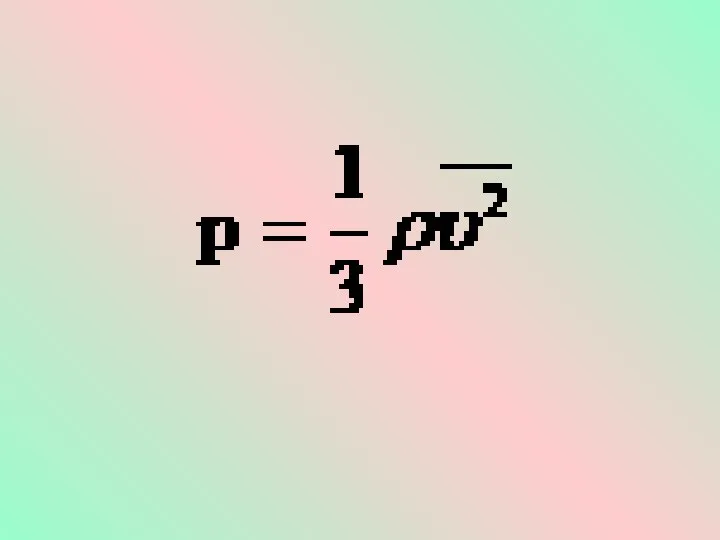



 Исследование термоЭДС, магнетотермоЭДС и электросопротивления в манганите Pr0,65(Ca0,8Sr0,2)0,35MnO3
Исследование термоЭДС, магнетотермоЭДС и электросопротивления в манганите Pr0,65(Ca0,8Sr0,2)0,35MnO3 Электрическая цепь. Электрический ток
Электрическая цепь. Электрический ток induction motor
induction motor Электрические схемы КЭС
Электрические схемы КЭС Размер и форма Земли
Размер и форма Земли Дыбыс тербелістері
Дыбыс тербелістері Петрофизика и геофизические исследования скважин (ГИС)
Петрофизика и геофизические исследования скважин (ГИС) Презентация ИНЕРЦИЯ ТЕЛ. ВЗАИМОДЕЙСТВИЕ ТЕЛ.
Презентация ИНЕРЦИЯ ТЕЛ. ВЗАИМОДЕЙСТВИЕ ТЕЛ. Презентация по физике "Динамика" - скачать бесплатно
Презентация по физике "Динамика" - скачать бесплатно Частные случаи движения точки
Частные случаи движения точки Лазерно-информационные технологии для медицины
Лазерно-информационные технологии для медицины Уроки физики в 11 классе Учитель физики МОУ СОШ п.Мирный Ажгалиева Асия Амангельдеевна
Уроки физики в 11 классе Учитель физики МОУ СОШ п.Мирный Ажгалиева Асия Амангельдеевна Формирование УУД на уроках физики с помощью работы с учебником
Формирование УУД на уроках физики с помощью работы с учебником Тензор деформаций. Тензор скоростей деформации
Тензор деформаций. Тензор скоростей деформации Тепловое излучение тел
Тепловое излучение тел Физика. Вводный урок
Физика. Вводный урок Техническое обслуживание и ремонт с/х машин и оборудования
Техническое обслуживание и ремонт с/х машин и оборудования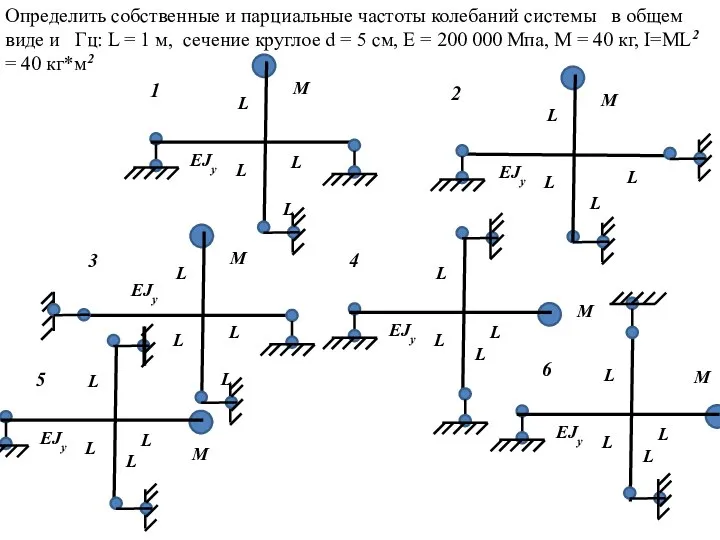 Динамика сооружений
Динамика сооружений Презентация по физике "Компьютерные технологии в процессе обучения физики" - скачать
Презентация по физике "Компьютерные технологии в процессе обучения физики" - скачать  Гидростатическое давление. Билет 20. Получение формулы для расчета давления жидкости
Гидростатическое давление. Билет 20. Получение формулы для расчета давления жидкости Исследование радиационного фона
Исследование радиационного фона Презентация по физике Колебания и волны
Презентация по физике Колебания и волны Новая модель заданий КИМ ЕГЭ по физике в 2022 году
Новая модель заданий КИМ ЕГЭ по физике в 2022 году Курс задач
Курс задач Техническое обслуживание и ремонт автотранспорта МДК 01.01. Устройство автомобилей
Техническое обслуживание и ремонт автотранспорта МДК 01.01. Устройство автомобилей Масса? Что-то знакомое… Масса тела - физическая величина, равная отношению действующей на тело силы к приобретенному им ускорению: m= F/a ( учебник «Физика-9»)
Масса? Что-то знакомое… Масса тела - физическая величина, равная отношению действующей на тело силы к приобретенному им ускорению: m= F/a ( учебник «Физика-9») Презентация по физике "Изображения, даваемые линзой" - скачать
Презентация по физике "Изображения, даваемые линзой" - скачать  Рентген сәулесін алу және қолдану
Рентген сәулесін алу және қолдану