Содержание
- 2. Молекулярная физика и термодинамика – разделы физики, в которых изучают макропроцессы в телах, связанные с большим
- 3. Молекулярная физика – раздел науки, в котором изучаются свойства тел на основе трех положений молекулярно –
- 4. Существование молекул и их непрерывное движение доказывает броуновское движение. Броун наблюдал под микроскопом беспорядочное движение цветочной
- 5. Термодинамика – раздел физики, изучающий общие свойства макроскопических систем, находящихся в состоянии термодинамического равновесия, и процессы
- 6. Термодинамические параметры состояния. Любая термодинамическая система может находится в различных состояниях, характеризующихся так называемыми параметрами состояния:
- 7. Измерение давления
- 8. Объём =1 м3, 1 л =10-3 м3. Объём газа совпадает с объемом занимаемого им сосуда.
- 10. Температура – физ. величина, характеризующая состояние термодинамического равновесия макроскопической системы. T=t+273 (K) Абсурдно говорить о температуре
- 12. Макросистема находится в состоянии термодинамического равновесия, если её состояние с течением времени не меняется, т.е. не
- 13. Опытные законы идеального газа. Уравнение состояния идеального газа Идеальным называется газ 1) между молекулами которого отсутствуют
- 14. Идеальный газ
- 15. Французский физик и инженер Б.Клайперон (1799-1864) вывел уравнение, связывающее три параметра. – уравнение состояния идеального газа.
- 16. Изопроцессы – изменение состояния идеального газа при котором один из трёх его параметров остаётся постоянным, а
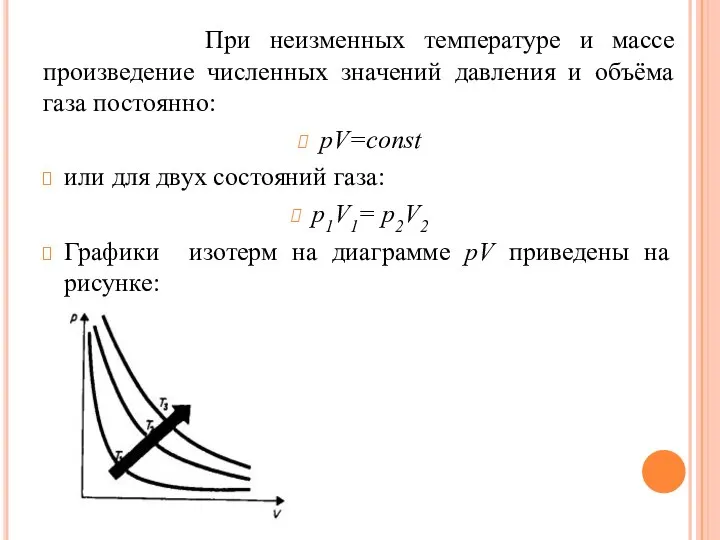
- 17. При неизменных температуре и массе произведение численных значений давления и объёма газа постоянно: pV=const или для
- 18. Закон Гей-Люссака (1778-1850 г фран. физик) описывает изобарный процесс p=const, m=const) При постоянном давлении объём данной
- 19. Закон Шарля ( изохорный процесс: V=const, m=const) При постоянном объёме давление данной массы газа прямо пропорционально
- 20. Русский ученый Д. И. Менделеев (1834-1907г) объединил уравнение Клапейрона с законом Авогадро, согласно которому моли всех
- 21. p=nkT - уравнение состояния идеального газа. Для смеси идеальных газов выполняется закон Дальтона: , где -
- 22. или , где – соответственно количество вещества, число молекул, масса и молекулярная масса i-ого компонента смеси.
- 23. Основное уравнение молекулярно-кинетической теории. Молекулярно-кинетическая теория объясняет давление газа на стенки сосуда как результат соударения молекул
- 24. Т.к. реально молекулы движутся под разными направлениями и скорости их различны, то примем для простоты следующие
- 25. Т.к. =>pV= т.к. Nm0=m pV= ,(*) где - суммарная кинетическая энергия. Кинетическая энергия одной молекулы одноатомного
- 26. Закон Максвелла о распределений молекул идеального газа по скоростям и энергии теплового движения. При выводе основного
- 27. Это объясняется тем, что в газе, находящимся в состоянии равновесия, устанавливается некоторое стационарное, не меняющееся со
- 28. Если разбить диапазон скоростей молекул на малые интервалы, равные dυ, то на каждый интервал скорости будет
- 29. Видно, что конкретный вид функции зависит от рода газа (массы молекул) и от параметров состояния (от
- 31. Из формулы следует, что при повышении температуры максимум функции распределения по скоростям сместиться вправо (значение υв
- 32. Средняя скорость молекулы (средняя арифметическая скорость): Подставляя f(υ) и интегрируя, получаем: Функция распределения молекул по энергиям
- 33. Барометрическая формула. Распределение Больцмана. При выводе основного уравнения молекулярно-кинетической теории газов и макcвелловского распределения молекул по
- 34. Молекулы любого газа находятся в потенциальном поле тяготения Земли. Тяготение, с одной стороны, и тепловое движение
- 40. Скачать презентацию



































 Задачи на движение
Задачи на движение Разборка – сборка кривошипно шатунного механизма двигателей автомобилей ЗИЛ – 508.10, ВАЗ – 2106 и ВАЗ -21083
Разборка – сборка кривошипно шатунного механизма двигателей автомобилей ЗИЛ – 508.10, ВАЗ – 2106 и ВАЗ -21083 Вынужденные колебания. Резонанс
Вынужденные колебания. Резонанс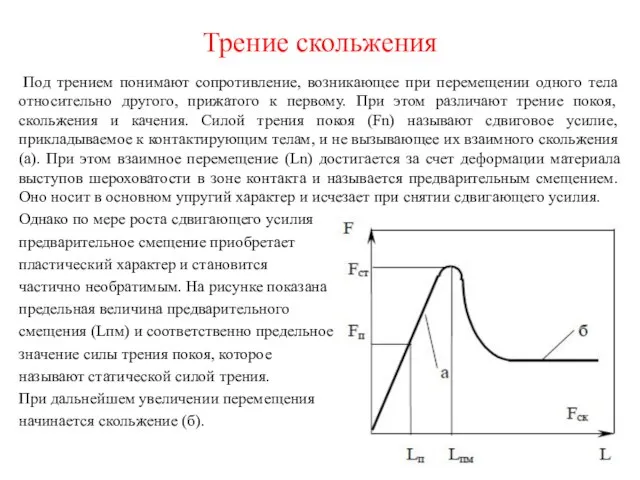 Трение скольжения
Трение скольжения Тепловой расчет полупроводников
Тепловой расчет полупроводников Силы в природе
Силы в природе Решение задач по ядерной физике
Решение задач по ядерной физике Теплопередача при стационарном режиме
Теплопередача при стационарном режиме Оптика. Предмет оптики
Оптика. Предмет оптики Кинематика. Нүкте кинематикасы. Қатты дене кинематикасы
Кинематика. Нүкте кинематикасы. Қатты дене кинематикасы Аттестационная работа. Лабораторная работа как шаг к исследованию. Определение коэффициента жесткости резинового жгута, 10 класс
Аттестационная работа. Лабораторная работа как шаг к исследованию. Определение коэффициента жесткости резинового жгута, 10 класс Содержание Атомная физика 1.Строение атома (Резерфода) 2.Модель атома водорода по Бору 3.Квантовые постулаты Бора 4.Испускание и п
Содержание Атомная физика 1.Строение атома (Резерфода) 2.Модель атома водорода по Бору 3.Квантовые постулаты Бора 4.Испускание и п Основное уравнение молекулярно-кинетической теории
Основное уравнение молекулярно-кинетической теории Управление технологическим процессом технического обслуживания и ремонта ходовой части автомобиля марки SSANGYONG
Управление технологическим процессом технического обслуживания и ремонта ходовой части автомобиля марки SSANGYONG Энергетика: Катушка Тесла
Энергетика: Катушка Тесла Курская АЭС
Курская АЭС Розрахунок опору провідника. Питомий опір речовини. Урок 46
Розрахунок опору провідника. Питомий опір речовини. Урок 46 Основные параметры метода контроля
Основные параметры метода контроля Электрические явления в природе и технике
Электрические явления в природе и технике Вектор. Дії над векторами
Вектор. Дії над векторами Звук. Звуковая шкала
Звук. Звуковая шкала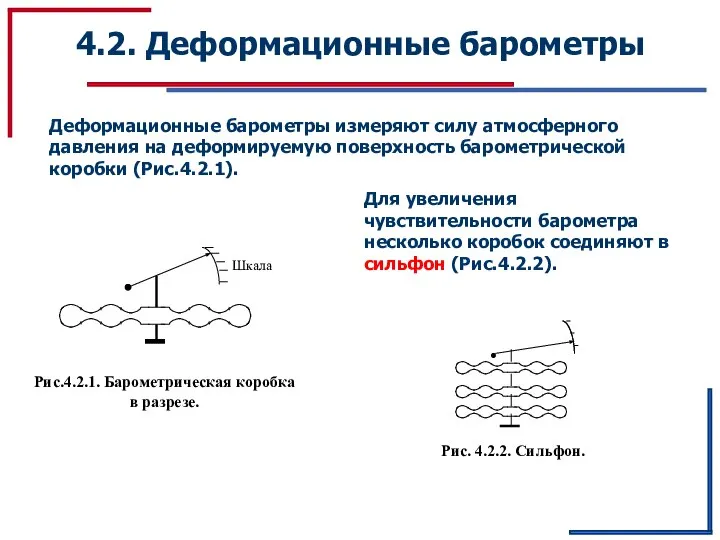 Тема4-2 Деформационные барометры
Тема4-2 Деформационные барометры Оптика Лекция 15
Оптика Лекция 15  Рычаги в быту. Работа гатауллиной амины
Рычаги в быту. Работа гатауллиной амины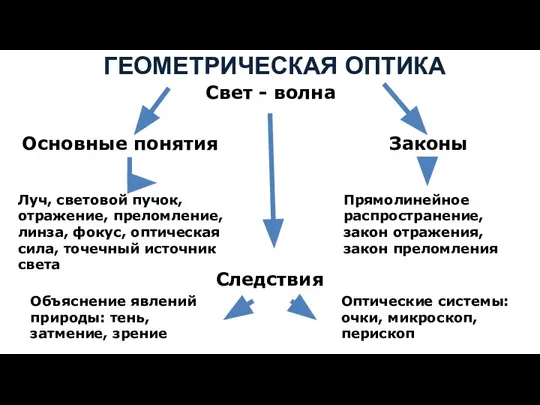 Геометрическая оптика
Геометрическая оптика Презентация по физике Таблицы по физике
Презентация по физике Таблицы по физике  Расчет сопротивления проводника. Удельное сопротивление
Расчет сопротивления проводника. Удельное сопротивление Силы в природе
Силы в природе