Содержание
- 2. 10.2 Уравнение состояния идеального газа Идеальным газом называется газ, в котором можно пренебречь взаимодействием между молекулами.
- 3. Из них следует, что в общем виде связь между P, V, T может быть записана как
- 4. Закон Авогадро Авогадро нашел, что моли любых газов при одинаковых температуре и давлении занимают одинаковые объемы.
- 5. Запишем уравнение состояния идеального газа (10.2.1) при нормальных условиях для 1 - го моля газа где
- 6. Получим уравнение состояния для произвольного объема газа V массой m. Если М – масса одного моля
- 7. Опытным путем найдено, что в 1-м моле вещества содержится число частиц, равное числу Авогадро Из пропорции
- 8. Величина называется постоянной Больцмана. Введем концентрацию молекул Тогда уравнение Клайперона-Менделеева примет вид
- 9. 10.7 Барометрическая формула Найдем закон изменения давления газа с высотой за счет влияния силы тяжести. Считаем
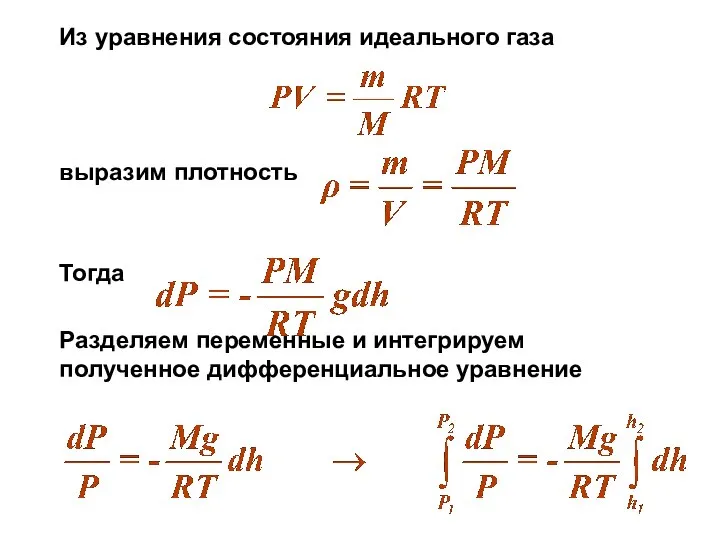
- 10. Из уравнения состояния идеального газа выразим плотность Тогда Разделяем переменные и интегрируем полученное дифференциальное уравнение
- 11. В результате находим Пусть h1 - высота на уровне моря, а Р1 – давление на уровне
- 12. 10.8 Распределение Больцмана Согласно уравнению состояния идеального газа P = nkT давление пропорционально концентрации молекул газа
- 13. 11. Основы термодинамики 11.1 Первое начало термодинамики При термодинамическом описании свойств макросистем используют закономерности, наблюдающиеся в
- 14. Внутренняя энергия макросистемы U состоит из двух частей: 1) кинетической энергии хаотического движения молекул в системе
- 15. Разобьем макросистему на достаточно большие части. Поскольку межмолекулярные силы короткодействующие, то потенциальной энергией взаимодействия между частями
- 16. Внутренняя энергия U обладает еще одним свойством – она является функцией состояния. Это значит, что величина
- 17. Из закона сохранения энергии следует, что изменение внутренней энергии системы ΔU при ее переходе из начального
- 18. Если ΔU > 0, то совершенная системой работа меньше полученного количества теплоты, то есть Q >
- 19. Пусть макросистема совершает процесс, в ходе которого она периодически возвращается в исходное состояние, тогда ее внутренняя
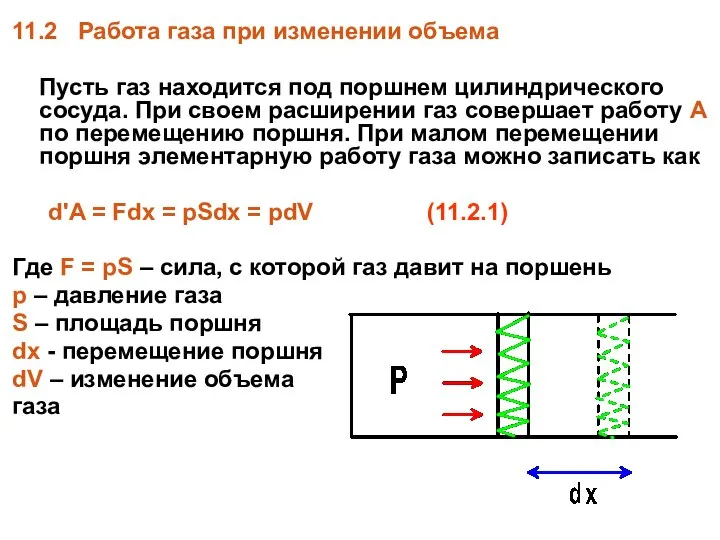
- 20. 11.2 Работа газа при изменении объема Пусть газ находится под поршнем цилиндрического сосуда. При своем расширении
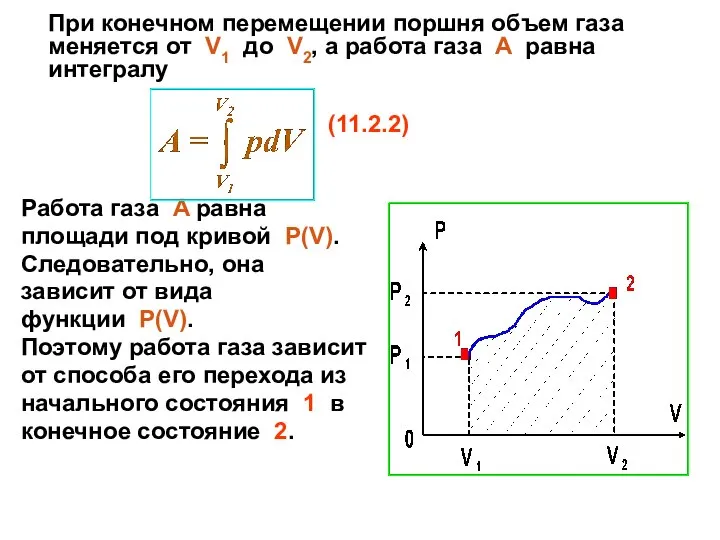
- 21. При конечном перемещении поршня объем газа меняется от V1 до V2, а работа газа A равна
- 22. 11.3 Теплоемкость идеального газа Теплоемкость равна количеству теплоты, которое нужно передать телу, чтобы повысить его температуру
- 23. Молярная теплоемкость – количество теплоты, необходимое для нагревания 1 моля вещества на 1° К (11.3.3) где
- 24. Теплоемкость зависит от условий измерения. Различают молярную теплоемкость при постоянном объеме cV и постоянном давлении cP
- 25. Введем отношение Величина γ называется постоянной адиабаты.
- 26. 11.4 Число степеней свободы Числом степеней свободы механической системы называется число независимых величин, с помощью которых
- 27. У системы из N невзаимодействующих материальных точек имеется 3N степеней свободы. Если между 2-мя точками имеется
- 28. У системы из N упруго связанных точек имеется 3N степеней свободы, из которых: 3 степени –
- 29. Теперь рассмотрим молекулы. При определении числа степеней свободы молекулы входящие в нее атомы надо рассматривать как
- 30. Если два атома в двухатомной молекуле связаны не жестко, а упруго, то расстояние между атомами может
- 31. среднее значение кинетической энергии поступательного движения молекулы идеального газа равно Так как все 3 поступательные степени
- 32. Например, на 1 вращательную степень свободы тоже приходится энергия, равная . У молекулы, испытывающей колебания, имеется
- 33. В идеальном газе молекулы не взаимодействуют друг с другом, поэтому его внутренняя энергия равна сумме энергий
- 34. Учтем, что для идеального газа сР = сV + R , поэтому (11.4.6) Следовательно, обе молярные
- 35. 11.9 Цикл Карно Рассмотрим прямой обратимый процесс, состоящий из двух изотерм и двух адиабат. Такой цикл
- 36. Следовательно, КПД в цикле Карно зависит только от температур нагревателя Т1 и холодильника T2 , но
- 37. 11.10 Энтропия. 2-е начало термодинамики Рассмотрим соотношение (11.9.2), полученное для цикла Карно где Т1 – температура
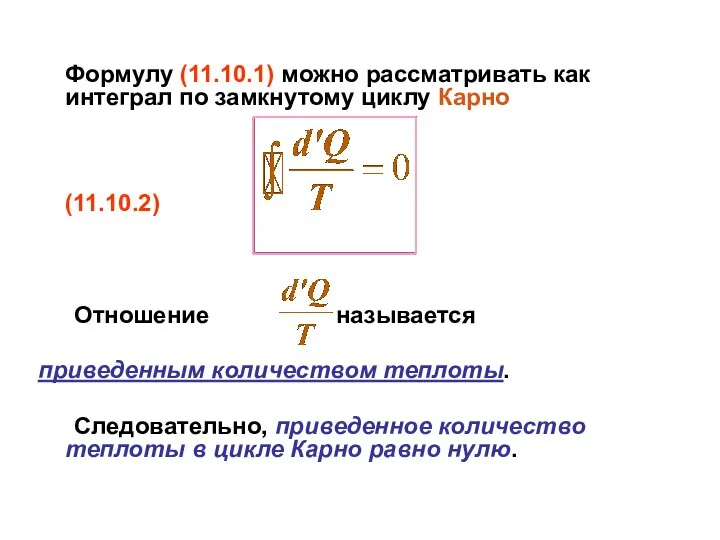
- 38. Формулу (11.10.1) можно рассматривать как интеграл по замкнутому циклу Карно (11.10.2) Отношение называется приведенным количеством теплоты.
- 39. Обозначим его как (11.10.3) где функция S называется энтропией. Понятие энтропии ввел Клаузиус в 1865 г.
- 40. Если процесс не замкнутый, то при переходе из начального состояния 1 в конечное состояние 2 энтропия
- 41. Для изолированной (замкнутой) системы, не обменивающейся теплом с окружающими телами Если при этом процесс, совершаемый замкнутой
- 42. Если же изолированная система совершает необратимый процесс, то ее энтропия всегда возрастает Объединяя результаты для обратимого
- 43. Все реальные процессы необратимы, поэтому они протекают так, что энтропия замкнутой системы возрастает. Второе начало термодинамики
- 45. Скачать презентацию






































 Спин и магнитный момент электрона
Спин и магнитный момент электрона Методы микроскопии
Методы микроскопии Переменные, влияющие на экспозицию
Переменные, влияющие на экспозицию Сила взаимодействия молекул
Сила взаимодействия молекул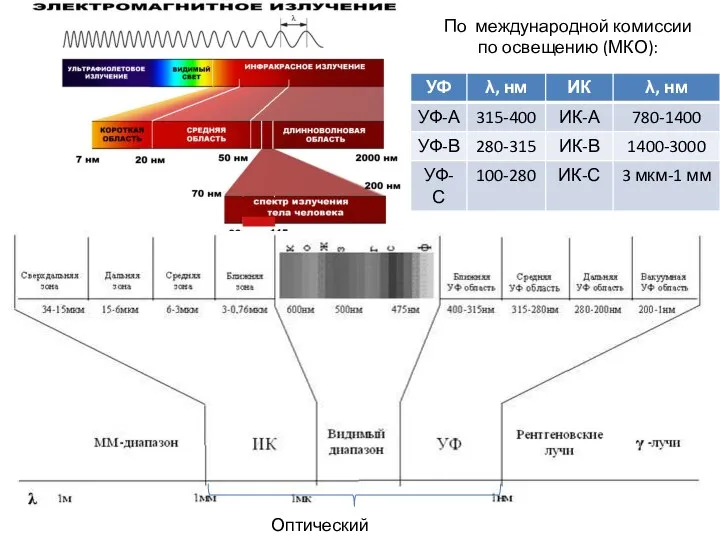 Электромагнитное излучение
Электромагнитное излучение Специальная теория относительности
Специальная теория относительности Антивещество. Античастицы. Получение и свойства антивещества
Антивещество. Античастицы. Получение и свойства антивещества Роль физико-химических методов анализа потребительских товаров при установлении их безопасности и качества
Роль физико-химических методов анализа потребительских товаров при установлении их безопасности и качества Создание фонтанов
Создание фонтанов Сушка обмоток после пропитки
Сушка обмоток после пропитки Атом водорода в квантовой механике
Атом водорода в квантовой механике Электростатика, как раздел электродинамики
Электростатика, как раздел электродинамики Технологии, применяемые при ремонте автомобилей. Ремонт коробок передач, раздаточных коробок и карданных валов. (Тема 9.7)
Технологии, применяемые при ремонте автомобилей. Ремонт коробок передач, раздаточных коробок и карданных валов. (Тема 9.7) Кравцова Инна Александровна учитель 1 квалификационной категории МБОУ СОШ № 151 Г.Новосибирск
Кравцова Инна Александровна учитель 1 квалификационной категории МБОУ СОШ № 151 Г.Новосибирск  Движение тел по наклонной плоскости. Решение задач
Движение тел по наклонной плоскости. Решение задач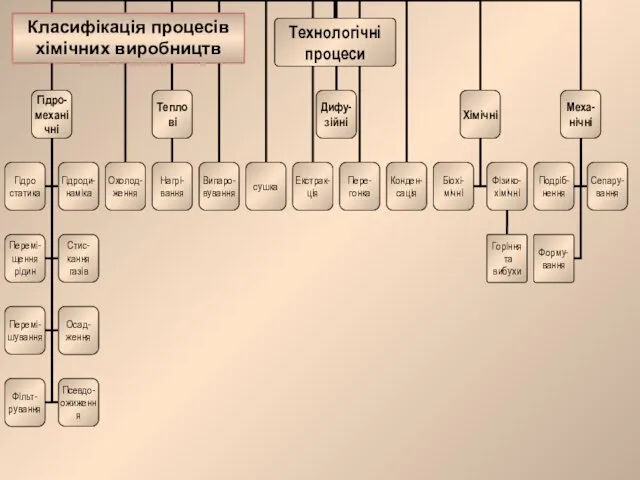 Класифікація процесів хімічних виробництв
Класифікація процесів хімічних виробництв Молекулы. Молекулярные спектры излучения и поглощения. Адиабатическое приближение. Термы двухатомной молекул
Молекулы. Молекулярные спектры излучения и поглощения. Адиабатическое приближение. Термы двухатомной молекул Расчетно-графическая работа №2
Расчетно-графическая работа №2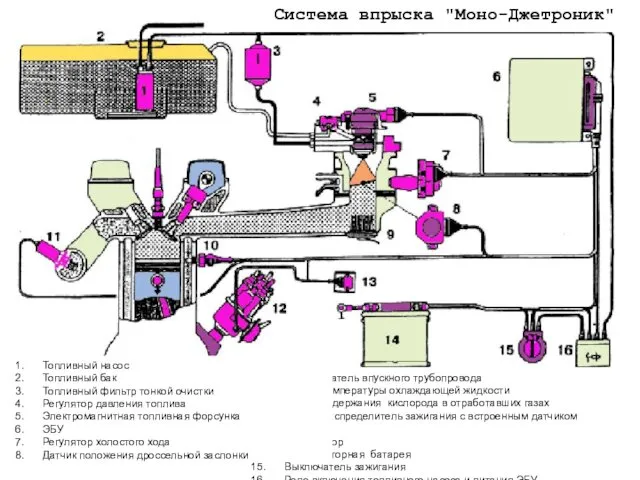 Система впрыска Моно-Джетроник
Система впрыска Моно-Джетроник Строение атома Квантовая теория строения атома
Строение атома Квантовая теория строения атома Атомно-абсорбционная спектрометрия
Атомно-абсорбционная спектрометрия Презентация по физике "Знакомые незнакомцы (влияние звуков природы на состояние человека)" - скачать
Презентация по физике "Знакомые незнакомцы (влияние звуков природы на состояние человека)" - скачать  Динамика. Введение.Основные законы динамики. Две задачи динамики
Динамика. Введение.Основные законы динамики. Две задачи динамики Пути повышения качества физической подготовки обучающихся на уроках физической культуры и во внеурочное время
Пути повышения качества физической подготовки обучающихся на уроках физической культуры и во внеурочное время Ньютон. Совершенны ли законы Ньютона?
Ньютон. Совершенны ли законы Ньютона? История создания швейной машины, их виды
История создания швейной машины, их виды Итоговый проект «Радиация вокруг нас»
Итоговый проект «Радиация вокруг нас» Аттестационная работа. Практика проектно-исследовательской деятельности по физике и астрономии
Аттестационная работа. Практика проектно-исследовательской деятельности по физике и астрономии