Содержание
- 2. Лекция № 2 Первое начало термодинамики 1. Внутренняя энергия. Макроскопическая работа. Количество теплоты. 2. Первое начало
- 3. Внутренняя энергия Наряду с механической энергией любое тело (или система) обладает внутренней энергией. Внутренняя энергия –
- 4. В термодинамических процессах изменяется только кинетическая энергия движущихся молекул (тепловой энергии недостаточно, чтобы изменить строение атома,
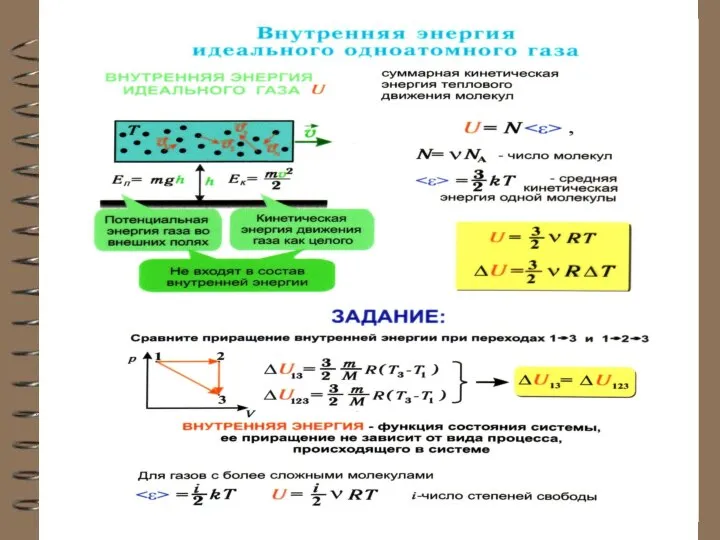
- 5. Внутренняя энергия U одного моля идеального одноатомного газа равна: или Таким образом, внутренняя энергия зави-сит только
- 6. В каждом состоянии система обладает определенным и только таким значением внутренней энергии, поэтому можно записать: Так
- 7. Внутренняя энергия U ν молей идеального одноатомного газа равна: Для многоатомного идеального газа, у которого i
- 10. Работа и теплота Термодинамическая система может обладать как внутренней, так и механичес-кой энергией и разные системы
- 13. При переходе из состояния 1 в состояние 2 (конечном изменении объема) давление может изменяться Геометрическая интерпретация
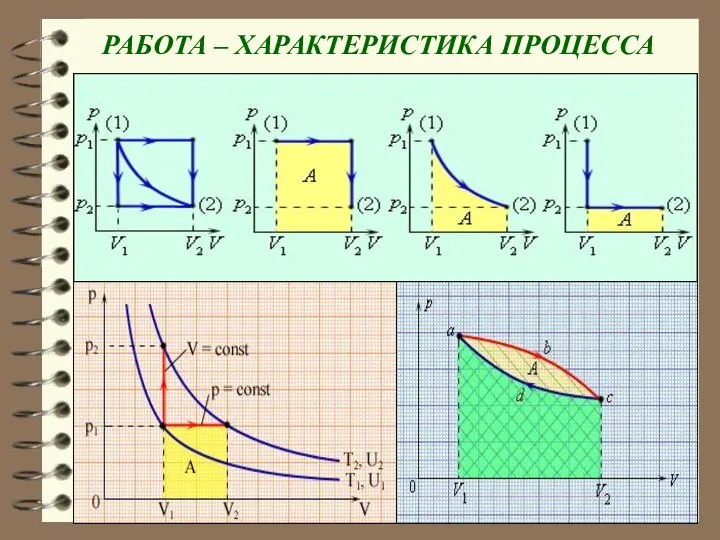
- 14. РАБОТА ПРИ ИЗОПРОЦЕССАХ
- 15. РАБОТА – ХАРАКТЕРИСТИКА ПРОЦЕССА
- 16. Количество теплоты Q , представляет собой энергию, которая передаётся от одного тела к другому при их
- 18. Первое начало термодинамики (закон сохранения энергии при тепловых процессах) Количество теплоты, сообщаемой телу, идёт на увеличение
- 19. Закон сохранения энергии для малого изменения состояния системы будет иметь вид: U – функция состояния системы;
- 20. Теплота Q и работа А зависят от того, каким образом совершен переход из состояния 1 в
- 21. Теплотой называется энергия, передаваемая от тела с более высокой температурой телу с мень- шей температурой при
- 22. Если идеальный газ, получив теплоту, изотермически расширится от объёма V1 до объёма V2 , то при
- 23. Если то согласно первому началу термодинамики т.е. нельзя построить периодически действующий двигатель, который совершал бы бóльшую
- 24. Особое значение в термодинамике имеют круговые или циклические процессы, при которых система, пройдя ряд состояний, возвращается
- 25. Цикл, совершаемый идеальным газом, можно разбить на процессы: расширения (1 – 2) сжатия (2 – 1)
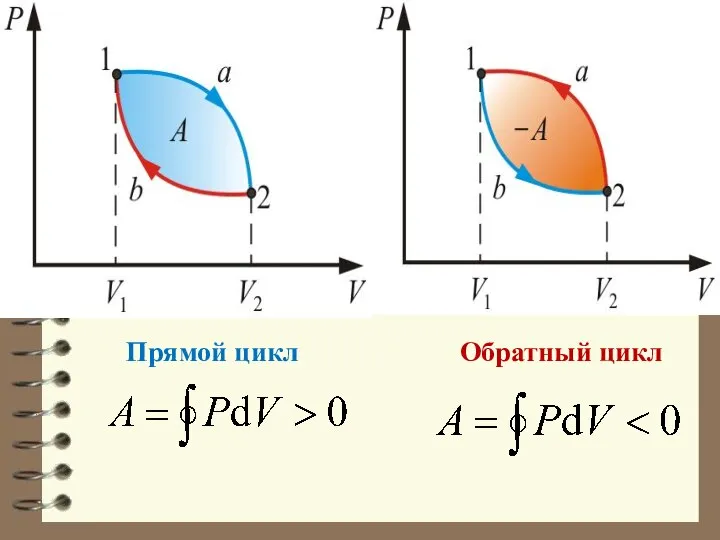
- 26. Если за цикл совершается положительная работа (цикл протекает по часовой стрелке), то он называется прямым. Если
- 27. Прямой цикл Обратный цикл
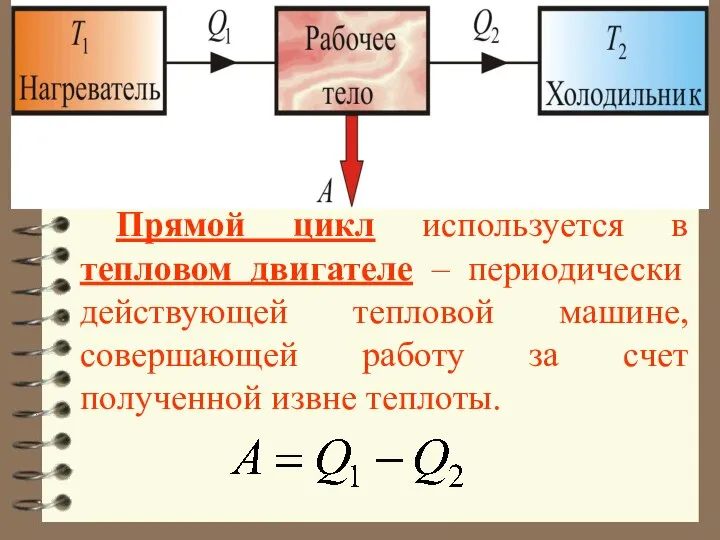
- 28. Прямой цикл используется в тепловых двигателях – периодически действующих установках, совершающих работу за счет получения извне
- 29. Т.о. работа, совершаемая за цикл, равна количеству полученной извне теплоты. Однако в результате кругового процесса система
- 30. Термический коэффициент полезного действия ( КПД ) для кругового процесса: Все термодинамические процессы, в том числе
- 31. Термический процесс называется обратимым, если он может происходить как в прямом, так и в обратном направлении.
- 32. Реальные процессы сопровождаются диссипацией энергии (из-за трения, теплопроводности и т.д.) и являются необратимыми. Обратимые процессы -
- 33. При адиабатическом расширении газа условие теплоизолированности системы исключает непосредственный теплообмен между системой и средой. Поэтому, производя
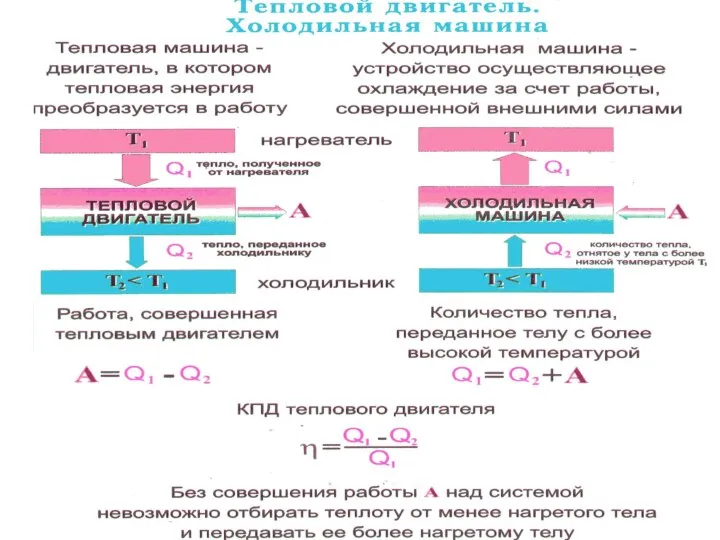
- 34. Тепловые машины Тепловой машиной называется периодический действующий двига-тель, совершающий работу за счет получаемого извне тепла. При
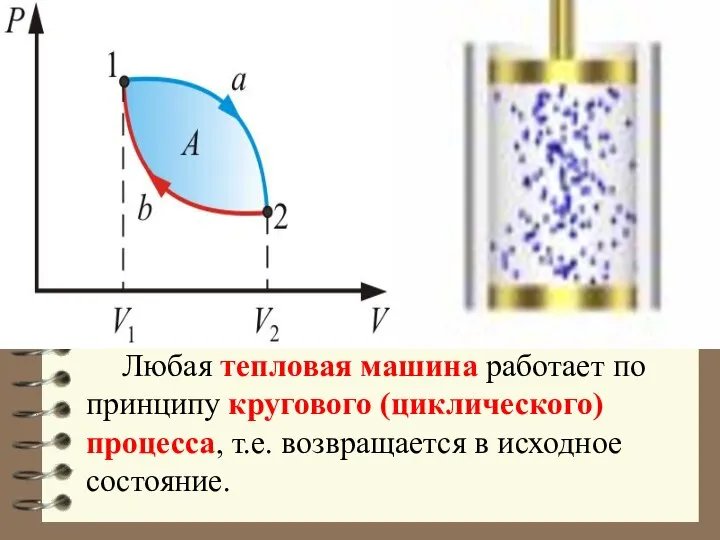
- 35. Любая тепловая машина работает по принципу кругового (циклического) процесса, т.е. возвращается в исходное состояние.
- 36. Но чтобы при этом была совершена полезная работа, возврат должен быть произведен с наименьшими затратами. Полезная
- 38. Принцип действия тепловых двигателей
- 39. Зачем холодильник? Так как в тепловой машине реализуется круговой процесс, то вернуться в исходное состояние можно
- 40. Прямой цикл используется в тепловом двигателе – периодически действующей тепловой машине, совершающей работу за счет полученной
- 41. От термостата с более высокой температурой Т1, называемого нагревателем, за цикл отнимается количество теплоты Q1, а
- 42. КПД тепловых двигателей
- 43. КПД тепловых двигателей
- 44. КПД тепловых двигателей
- 45. КПД тепловых двигателей
- 46. КПД тепловых двигателей
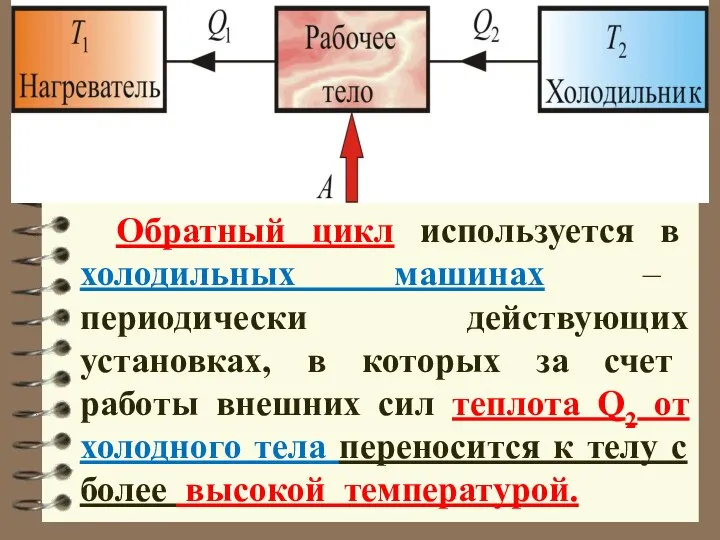
- 47. Обратный цикл используется в холодильных машинах – периодически действующих установках, в которых за счет работы внешних
- 50. Цикл Карно (обратимый). Карно теоретически про-анализировал обратимый наиболее экономичный цикл, состоящий из двух изотерм и двух
- 51. Карно Никола Леонард Сади (1796 – 1832) – французский физик и инженер, один из создателей термодинамики.
- 52. Цикл Карно является самым экономичным и представляет собой круговой процесс, состоящий из двух изотерм и двух
- 54. ТЕОРЕМА КАРНО Из всех периодически действующих тепловых машин, имеющих одинаковые температуры нагревателей и холодильников, наибольшим КПД
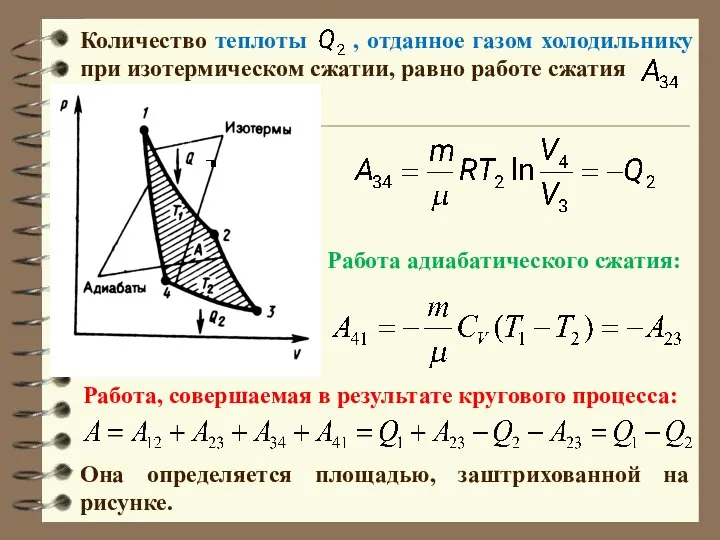
- 55. Поэтому количество теплоты , полученное газом от нагревателя, равно работе расширения , совершаемой газом при переходе
- 56. Количество теплоты , отданное газом холодильнику при изотермическом сжатии, равно работе сжатия Она определяется площадью, заштрихованной
- 57. Применив уравнение для адиабат 2-3 и 4-1, получим: и , откуда Термический КПД цикла Карно:
- 58. Видно, что η
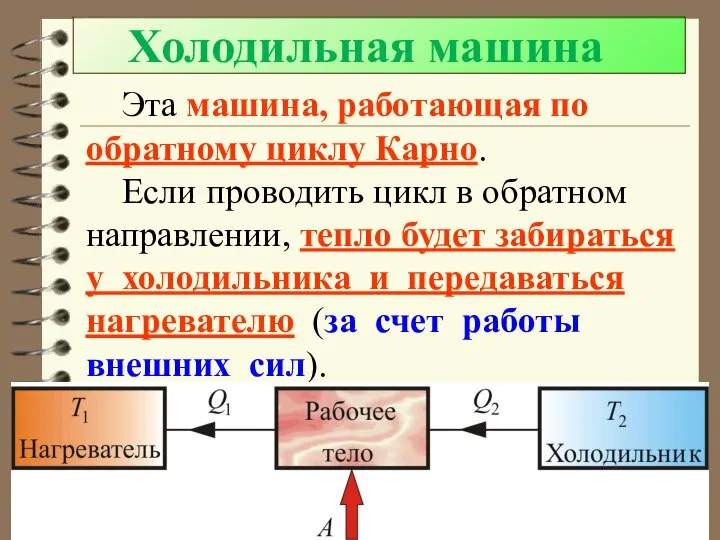
- 60. Холодильная машина Эта машина, работающая по обратному циклу Карно. Если проводить цикл в обратном направлении, тепло
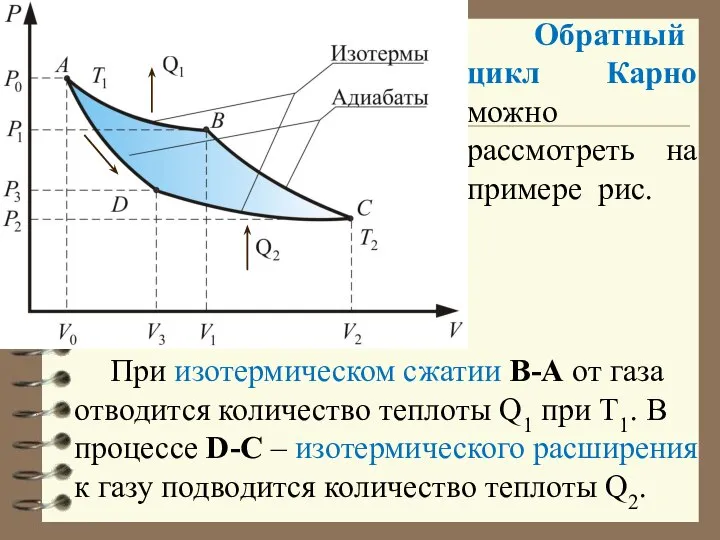
- 61. Обратный цикл Карно можно рассмотреть на примере рис. При изотермическом сжатии В-А от газа отводится количество
- 62. В этом цикле , и работа, совершаемая над газом – отрицательна, т.е. Если рабочее тело совершает
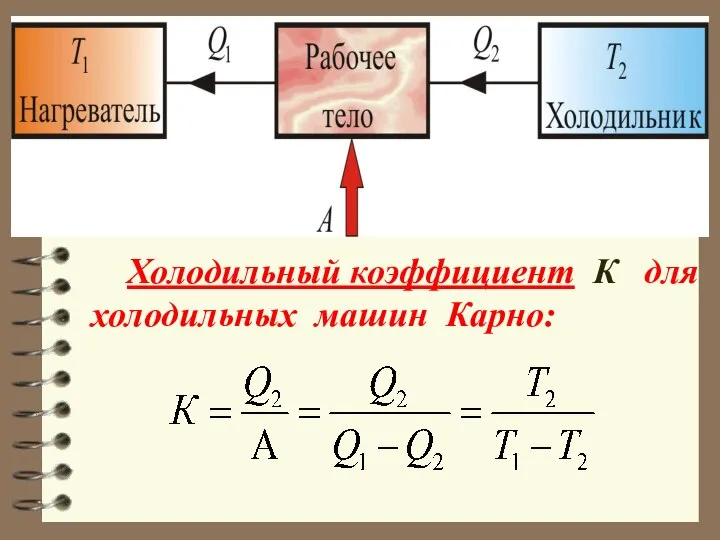
- 63. Холодильный коэффициент К для холодильных машин Карно:
- 64. Теплоёмкость идеального газа Теплоёмкость тела характеризуется количеством теплоты, необходимой для нагревания этого тела на один градус
- 65. Удельная теплоёмкость Суд – есть количество теплоты, необходимое для нагревания единицы массы вещества на 1 градус
- 66. Теплоёмкость термодинамической системы зависит от того, как изменяется состояние системы при нагревании. Если газ нагревать при
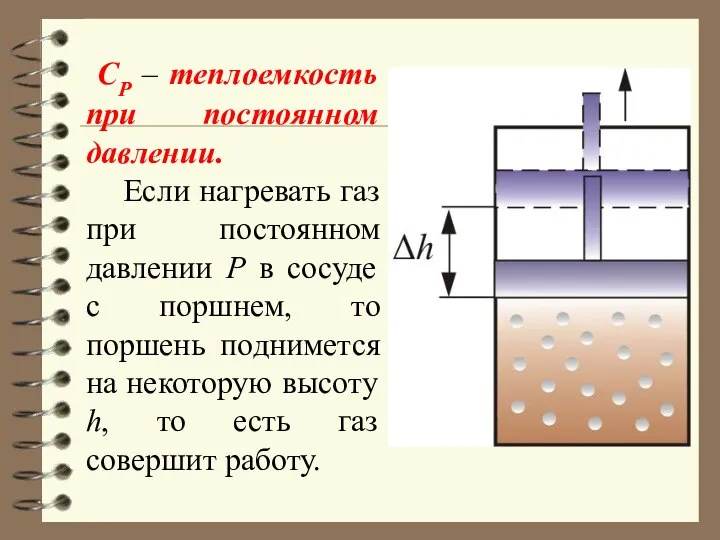
- 67. СР – теплоемкость при постоянном давлении. Если нагревать газ при постоянном давлении Р в сосуде с
- 68. Следовательно, проводимое тепло затрачивается и на нагревание и на совершение работы. Отсюда ясно, что Итак, проводимое
- 69. При изобарическом процессе кроме увеличения внутренней энергии происходит совершение работы газом (из I начала ТД): (для
- 70. Это уравнение Роберта Майера для одного моля газа. Из него следует, что физический смысл универсальной газовой
- 71. В общем случае так как внутренняя энергия U может зависеть только от температуры. В случае 1
- 72. Внутренняя энергия идеального газа является только функцией температуры (и не зависит от V, Р и тому
- 73. Внутренняя энергия одного моля идеального одноатомного газа равна: - молярная теплоемкость при постоянном объеме СV –
- 74. Внутренняя энергия одного моля идеального газа c i степенями свободы равна: молярная теплоемкость при постоянном объеме
- 75. Учитывая физический смысл R для изобарических процессов можно записать: (для одного моля). Отсюда для одноатомного: Тогда,
- 76. Для одного моля идеального газа: Постоянная адиабаты (коэффициент Пуассона) для идеального газа: Для одноатомного идеаль- ного
- 78. Адиабатный (адиабатический) процесс Это процесс, происходящий без теплообмена с окружающей средой, т.е. При адиабатном процессе работа
- 79. Подставляя dT в уравнение: Группируя PdV: Делим на где Т.к. γ = const ( для одноатомного
- 80. уравнение Пуассона или уравнение адиабаты для идеального газа Или в переменных Т и V уравнение адиабаты
- 82. Здесь уместно рассмотреть еще и политропный процесс – такой процесс, при котором изменяются все основные параметры
- 83. С помощью показателя n можно легко описать любой изопроцесс: 1. Изобарный процесс Р = const, n
- 84. 4. Адиабатический процесс ΔQ = 0, n = γ, Сад = 0. Во всех этих процессах
- 85. γ
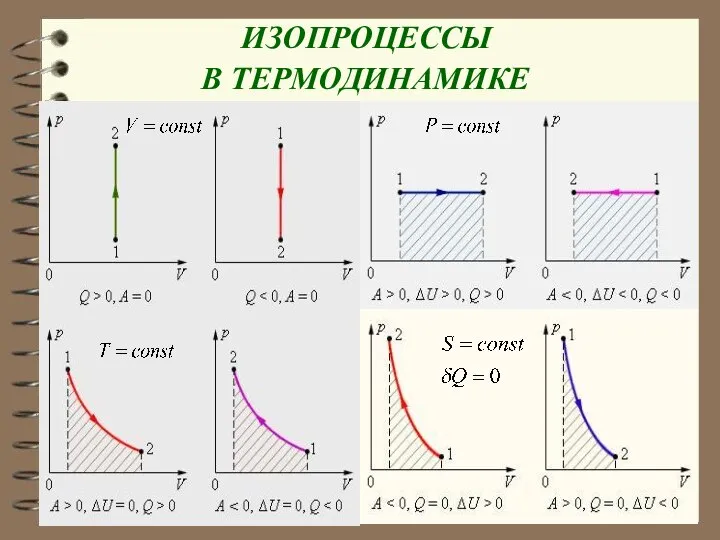
- 86. ИЗОПРОЦЕССЫ В ТЕРМОДИНАМИКЕ
- 90. Скачать презентацию










































































 The possibility of modifying the elements of the metal powder assembly with nanoparticles in order to reduce the friction
The possibility of modifying the elements of the metal powder assembly with nanoparticles in order to reduce the friction История изобретения паровых машин. Работу выполнила ученица 8б класса МКОУ СОШ пгт Подосиновец Пунченко Анастасия
История изобретения паровых машин. Работу выполнила ученица 8б класса МКОУ СОШ пгт Подосиновец Пунченко Анастасия Опиливание металла
Опиливание металла Электромагнитные взаимодействия, размеры и форма ядер
Электромагнитные взаимодействия, размеры и форма ядер Явление электромагнитной индукции. Уравнения Максвелла
Явление электромагнитной индукции. Уравнения Максвелла ПОЛНОЕ ВНУТРЕННЕЕ ОТРАЖЕНИЕ СВЕТА
ПОЛНОЕ ВНУТРЕННЕЕ ОТРАЖЕНИЕ СВЕТА Предмет физической химии
Предмет физической химии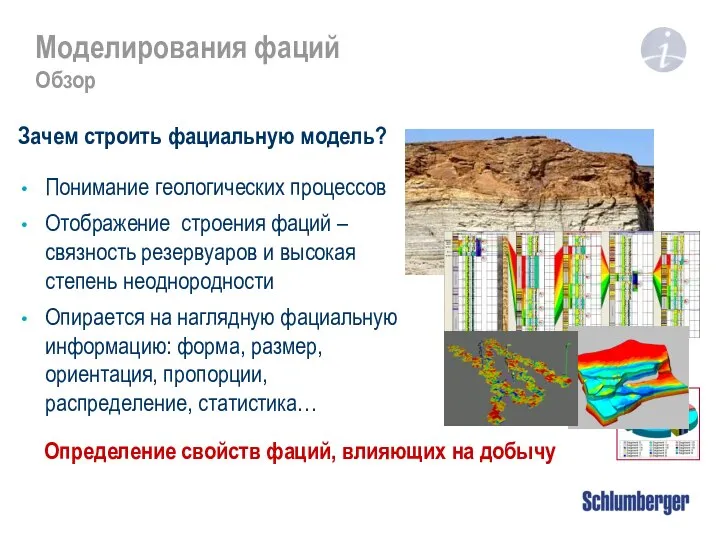 Моделирования фаций. Обзор
Моделирования фаций. Обзор Выполнила учитель физики Омеляшко О.В.
Выполнила учитель физики Омеляшко О.В. Сила трения
Сила трения Соударение твердых тел
Соударение твердых тел Геометрическое движение в физике
Геометрическое движение в физике Механические колебания и их характеристики. Виды колебаний. Механические волны
Механические колебания и их характеристики. Виды колебаний. Механические волны Собственность и доходы
Собственность и доходы Самолеты, используемые в работах по активным воздействиям на атмосферные процессы. Тема 6
Самолеты, используемые в работах по активным воздействиям на атмосферные процессы. Тема 6 Економетричні моделі динаміки
Економетричні моделі динаміки Теория подобия и моделирования
Теория подобия и моделирования Явление электромагнитной индукции
Явление электромагнитной индукции Количественный анализ. Хроматографические методы
Количественный анализ. Хроматографические методы Решение задач: построение изображений в линзах (работа на интерактивной доске)
Решение задач: построение изображений в линзах (работа на интерактивной доске) Давление света
Давление света Статическое электричество, защита от него. Молниеотвод
Статическое электричество, защита от него. Молниеотвод Магнитное поле.Вектор магнитной индукции.
Магнитное поле.Вектор магнитной индукции. Основы электродинамики напрвляющих систем. Уравнения Максвелла
Основы электродинамики напрвляющих систем. Уравнения Максвелла Склокомпозиційні матеріали для спаювання з широким інтервалом ТКЛР
Склокомпозиційні матеріали для спаювання з широким інтервалом ТКЛР Электростатическое поле в диэлектриках
Электростатическое поле в диэлектриках Фотополимерные материалы
Фотополимерные материалы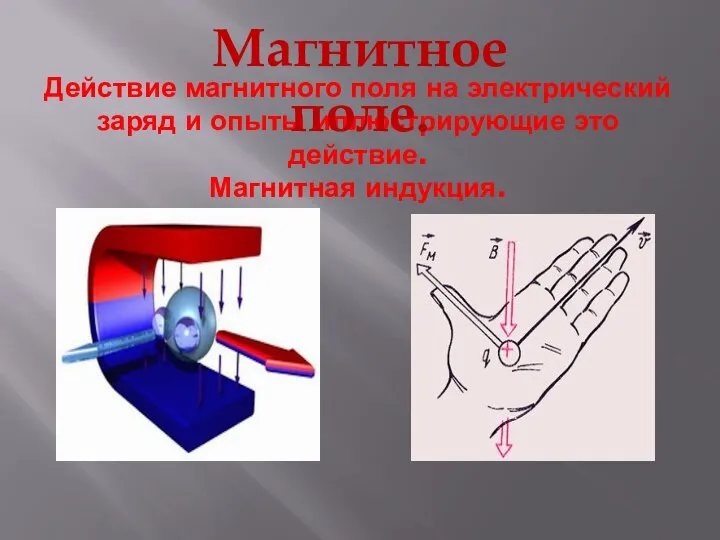 Магнитное поле. Действие магнитного поля на электрический заряд и опыты, иллюстрирующее это действие. Магнитная индукция
Магнитное поле. Действие магнитного поля на электрический заряд и опыты, иллюстрирующее это действие. Магнитная индукция