Содержание
- 2. НЕМНОГО ИСТОРИИ В 1884-1887гг. Сванте Аррениус разработал данную теорию, однако в момент создания она не была
- 3. Электролиты – вещества, растворы и расплавы которых проводят электрический ток. Соли, щелочи, кислоты Неэлектролиты – вещества,
- 4. СТЕПЕНЬ ДИССОЦИАЦИИ Степень диссоциации (α) – отношение количества вещества электролита, распавшегося на ионы (nд), к общему
- 5. СТЕПЕНЬ ДИССОЦИАЦИИ ЗАВИСИТ ОТ Природы электролита Концентрации (при разбавлении степень диссоциации увеличивается)
- 6. Сильные электролиты – это соединения, которые в водных растворах практически полностью диссоциируют на ионы. Слабые электролиты
- 7. ЭЛЕКТРОЛИТЫ Сильные Соли Основания (образованные щелочными и щелочноземельными металлами Многие неорганические кислоты HClO4, HNO3, HMnO4, HCl,
- 8. ПЕРВОЕ ПОЛОЖЕНИЕ При растворении в воде электролиты диссоциируют но положительные и отрицательные ионы Ионы различаются По
- 9. ВТОРОЕ ПОЛОЖЕНИЕ Причиной диссоциации электролита в водном растворе является его гидратация, т.е. взаимодействие электролита с молекулами
- 10. ТРЕТЬЕ ПОЛОЖЕНИЕ Беспорядочное (хаотичное) движение ионов в растворе под действием электрического поля становится направленным: положительно заряженные
- 11. ЧЕТВЕРТОЕ ПОЛОЖЕНИЕ Электролитическая диссоциация – обратимый для слабых электролитов Ассоциация – процесс обратный диссоциации (соединение ионов)
- 12. ЭЛЕКТРОПРОВОДНОСТЬ РАСТВОРОВ ЭЛЕКТРОЛИТОВ И НЕЭЛЕКТРОЛИТОВ В панель с клеммами вставляются электроды. Загнутый конец электрода находится сверху.
- 13. ЭЛЕКТРОПРОВОДНОСТЬ РАСПЛАВОВ Для проведения опыта нужен стакан на 100 мл, заполненный калийной селитрой на 1/3 (Tпл
- 14. ЭЛЕКТРОПРОВОДНОСТЬ ЭЛЕКТРОЛИТОВ РАЗЛИЧНОЙ СТЕПЕНИ ДИССОЦИАЦИИ Для сравнения электропроводности берут растворы одинаковой концентрации (100 мл, 2 моль/л)
- 15. ЭЛЕКТРОПРОВОДНОСТЬ РАСТВОРОВ СОЛИ, ОБРАЗОВАВШЕЙСЯ ИЗ ДВУХ СЛАБЫХ ЭЛЕКТРОЛИТОВ Опускают электроды в 50 мл раствора аммиака с
- 16. ЗАВИСИМОСТЬ ЭЛЕКТРОПРОВОДНОСТИ РАСТВОРА ОТ ИЗМЕНЕНИЯ КОНЦЕНТРАЦИИ ЭЛЕКТРОЛИТА Электроды прибора погружаются в стакан со 100 мл концентрированной
- 17. ДЕМОНСТРАЦИЯ ДВИЖЕНИЯ ИОНОВ. ВАРИАНТ 1 На крышку-панель помещают фильтровальную бумагу, смоченную бесцветным раствором соли (сульфата натрия,
- 18. Опыт движения анионов можно проводить и с другими веществами: А) смочить фильтровальную бумагу раствором хлорида натрия
- 20. Скачать презентацию

















 The possibility of modifying the elements of the metal powder assembly with nanoparticles in order to reduce the friction
The possibility of modifying the elements of the metal powder assembly with nanoparticles in order to reduce the friction История изобретения паровых машин. Работу выполнила ученица 8б класса МКОУ СОШ пгт Подосиновец Пунченко Анастасия
История изобретения паровых машин. Работу выполнила ученица 8б класса МКОУ СОШ пгт Подосиновец Пунченко Анастасия Опиливание металла
Опиливание металла Электромагнитные взаимодействия, размеры и форма ядер
Электромагнитные взаимодействия, размеры и форма ядер Явление электромагнитной индукции. Уравнения Максвелла
Явление электромагнитной индукции. Уравнения Максвелла ПОЛНОЕ ВНУТРЕННЕЕ ОТРАЖЕНИЕ СВЕТА
ПОЛНОЕ ВНУТРЕННЕЕ ОТРАЖЕНИЕ СВЕТА Предмет физической химии
Предмет физической химии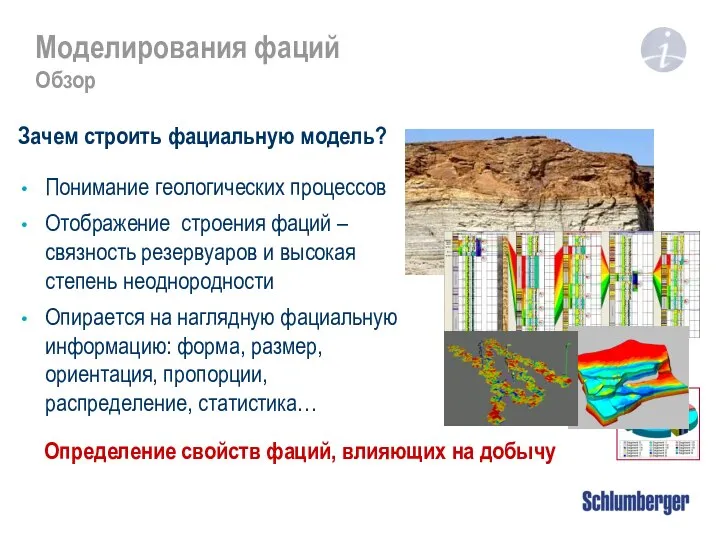 Моделирования фаций. Обзор
Моделирования фаций. Обзор Выполнила учитель физики Омеляшко О.В.
Выполнила учитель физики Омеляшко О.В. Сила трения
Сила трения Соударение твердых тел
Соударение твердых тел Геометрическое движение в физике
Геометрическое движение в физике Механические колебания и их характеристики. Виды колебаний. Механические волны
Механические колебания и их характеристики. Виды колебаний. Механические волны Собственность и доходы
Собственность и доходы Самолеты, используемые в работах по активным воздействиям на атмосферные процессы. Тема 6
Самолеты, используемые в работах по активным воздействиям на атмосферные процессы. Тема 6 Економетричні моделі динаміки
Економетричні моделі динаміки Теория подобия и моделирования
Теория подобия и моделирования Явление электромагнитной индукции
Явление электромагнитной индукции Количественный анализ. Хроматографические методы
Количественный анализ. Хроматографические методы Решение задач: построение изображений в линзах (работа на интерактивной доске)
Решение задач: построение изображений в линзах (работа на интерактивной доске) Давление света
Давление света Статическое электричество, защита от него. Молниеотвод
Статическое электричество, защита от него. Молниеотвод Магнитное поле.Вектор магнитной индукции.
Магнитное поле.Вектор магнитной индукции. Основы электродинамики напрвляющих систем. Уравнения Максвелла
Основы электродинамики напрвляющих систем. Уравнения Максвелла Склокомпозиційні матеріали для спаювання з широким інтервалом ТКЛР
Склокомпозиційні матеріали для спаювання з широким інтервалом ТКЛР Электростатическое поле в диэлектриках
Электростатическое поле в диэлектриках Фотополимерные материалы
Фотополимерные материалы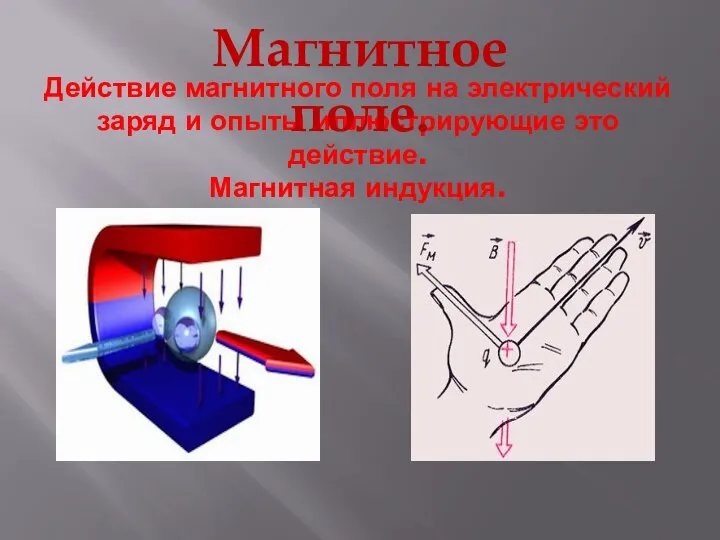 Магнитное поле. Действие магнитного поля на электрический заряд и опыты, иллюстрирующее это действие. Магнитная индукция
Магнитное поле. Действие магнитного поля на электрический заряд и опыты, иллюстрирующее это действие. Магнитная индукция