2. Взаємодія неметалів з неметалами:
а) Cl20 + Р0 = Р
+3Cl3-1 – фосфор (ІІІ) хлорид
Р0 – 3e-→ Р+3 3
3Cl20 + 6(1e-) → 2Cl3−1 6
3. Взаємодія неметалів з киснем:
а) P0 + O20 = P2 +5 O5-2 – фосфор (V) оксид
2Р0– 2(5e- )→ Р2+5 10
5О20 + 5(2e-) → 2О5−2 10
б) S0 + O20 = S+4O−22 – сульфур (ІV) оксид
S0 ─ 4e-→ S+4 4
О20 + 2(2e-) → О2−2 4
в) С0 + O20 = С+4O−22 – карбон (ІV) оксид
С0 ─ 4e-→ S+4 4
О20 + 2(2e-) → О2−2 4
ВІДНОВНИК – неметал з меншою електронегативністю
ОКИСНИК – неметал з більшою електронегативністю
з киснем –
ВІДНОВНИКИ
2 віддав – відновник;
1 одержав – окисник;
3
2
2
1 віддав – відновник;
1 одержав – окисник;
4
5
2
1 віддав – відновник;
1 одержав – окисник;
1 віддав – відновник;
1 одержав – окисник;




 Atomic structure and properties. (Chapter 3)
Atomic structure and properties. (Chapter 3) Товароведная характеристика и показатели качества соленой рыбы
Товароведная характеристика и показатели качества соленой рыбы Автомобильный транспорт как источник химического загрязнения тяжелыми металлами
Автомобильный транспорт как источник химического загрязнения тяжелыми металлами Зависимость свойств химических элементов от положения в ПСХЭ
Зависимость свойств химических элементов от положения в ПСХЭ Периодический закон и строение атома
Периодический закон и строение атома Ситуационная задача по биохимии
Ситуационная задача по биохимии Качественные реакции на ионы железа Fe2+ и Fe3+
Качественные реакции на ионы железа Fe2+ и Fe3+ Харчові добавки Підготували: Возна Руслана Таран Ірина
Харчові добавки Підготували: Возна Руслана Таран Ірина  Аттестационная работа. Химия в нашей жизни
Аттестационная работа. Химия в нашей жизни Сульфаниламидные препараты. Хинолоны
Сульфаниламидные препараты. Хинолоны Создание косметических средств
Создание косметических средств Горные породы и минералы. Камни-самоцветы
Горные породы и минералы. Камни-самоцветы Получение и приминение этилена
Получение и приминение этилена Элементы химической кинетики
Элементы химической кинетики Вода та її властивості
Вода та її властивості Цвет и другие диагностические признаки осадочных пород
Цвет и другие диагностические признаки осадочных пород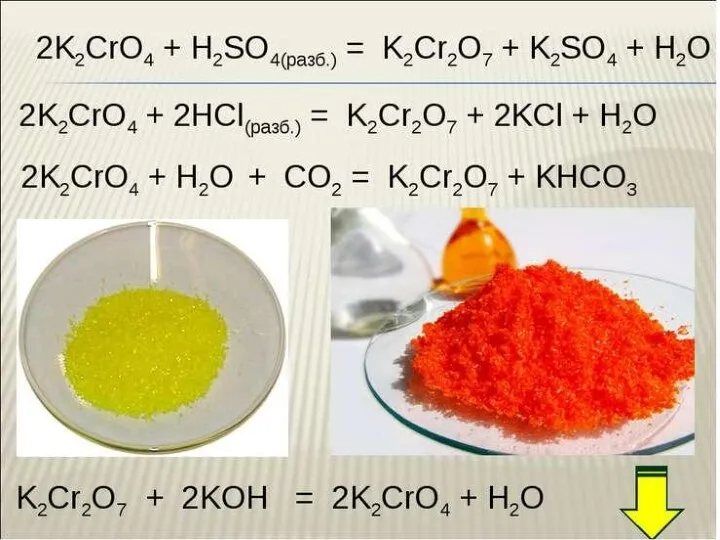 Хром. Соединения хрома
Хром. Соединения хрома Ароматические амины
Ароматические амины Ароматические оксисоединения. Фенолы
Ароматические оксисоединения. Фенолы Синтетичні речовини у сільському господарстві, медицині та промисловості Презентація на тему:
Синтетичні речовини у сільському господарстві, медицині та промисловості Презентація на тему:  Металлы. Классификация металлов
Металлы. Классификация металлов Вклад М.В. Ломоносова в дидактику химии
Вклад М.В. Ломоносова в дидактику химии Періодична система Д.І.Менделєєва
Періодична система Д.І.Менделєєва Карбонильные соединения
Карбонильные соединения Генетика. Лекция 5 Генотип. Геном. Кариотип. Геномные мутации. Генный баланс. Компенсация доз генов. Эволюция генома.
Генетика. Лекция 5 Генотип. Геном. Кариотип. Геномные мутации. Генный баланс. Компенсация доз генов. Эволюция генома.  Основы органической химии
Основы органической химии ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ А. М. БУТЛЕРОВА Становление органической химии. Предпосылки теории строения
ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ А. М. БУТЛЕРОВА Становление органической химии. Предпосылки теории строения  Ферменты 3. Медицинская энзимология. (Лекция 3)
Ферменты 3. Медицинская энзимология. (Лекция 3)