Содержание
- 2. Химическая кинетика – раздел химии, изуча-ющий закономерности протекания химичес-ких процессов во времени Основное понятие химической кинетики
- 3. 7.2. Типы химических реакций I. Элементарные реакции (одностадийные, простые) протекают в одну стадию: 2NO + O2
- 4. II Гомоенные реакции – протекают в объеме одной фазы: NaOH (раствор)+ НCl (раствор) = NaCl (раствор)+H2O
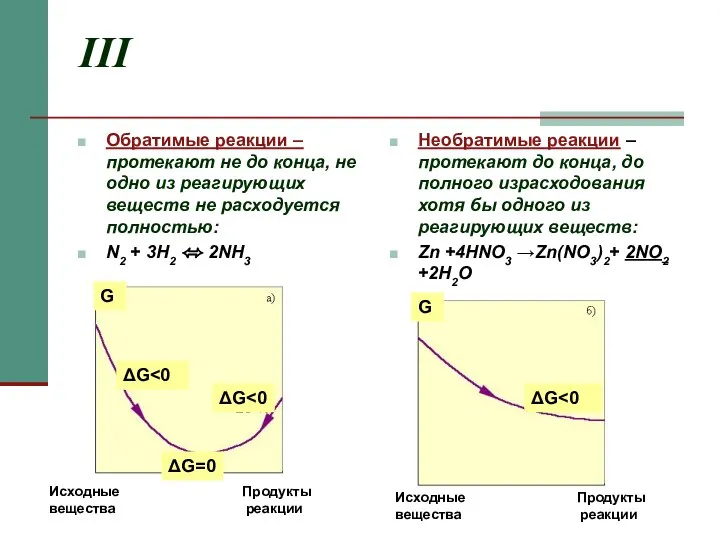
- 5. III Обратимые реакции – протекают не до конца, не одно из реагирующих веществ не расходуется полностью:
- 6. 6.3. Скорость химической реакции Скорость химической реакции – это число элементар-ных актов взаимодействия между молекулами реаги-рующих
- 7. 6.4. Факторы, влияющие на скорость химических реакций. Закон действующих масс. Опыт: Na2S2O3 +H2SO4= Na2SO4 +S↓+SO2 +
- 8. Скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ в степенях их стехиометрических коэффициентов. aA +
- 9. Закон действующих масс безусловно выполняется только для элементарных химических реакций, протекающих в одну стадию. В других
- 10. 6.5. Влияние температуры на скорость химической реакции Опыт: Na2S2O3 +H2SO4= Na2SO4 +S↓+SO2 + H2O Вывод: Чем
- 11. Правило Вант-Гоффа (1884 г.) При повышении температуры на каждые десять градусов скорость химической реакции возрастает в
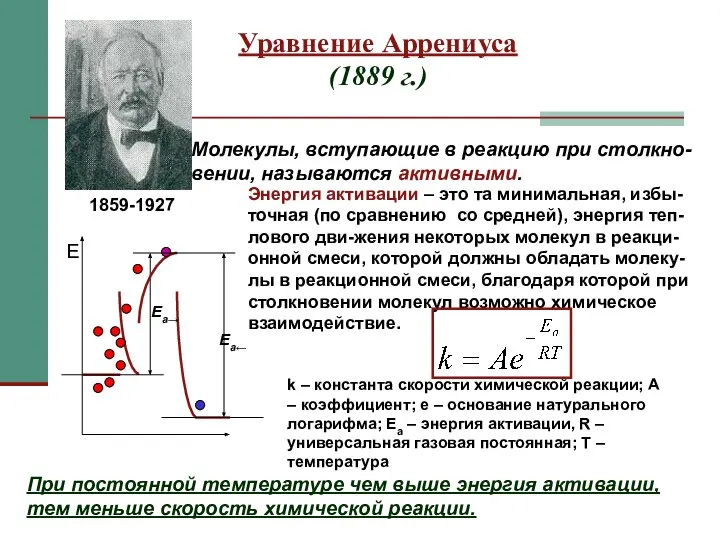
- 12. Уравнение Аррениуса (1889 г.) 1859-1927 Молекулы, вступающие в реакцию при столкно- вении, называются активными. Энергия активации
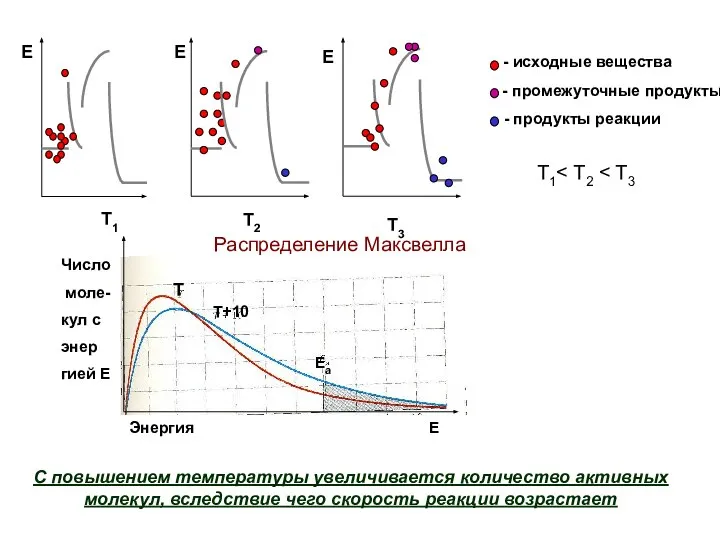
- 13. Т1 С повышением температуры увеличивается количество активных молекул, вследствие чего скорость реакции возрастает Распределение Максвелла
- 14. 6.6. Представление о катализе Вещество, которое увеличивает скорость реакции, оставаясь по окончании реакции химически неизмен-ным, называется
- 15. 6.7. Представление о лимитирующей стадии химического процесса. При k1 >> k2 все исходное ве-щество может превратиться
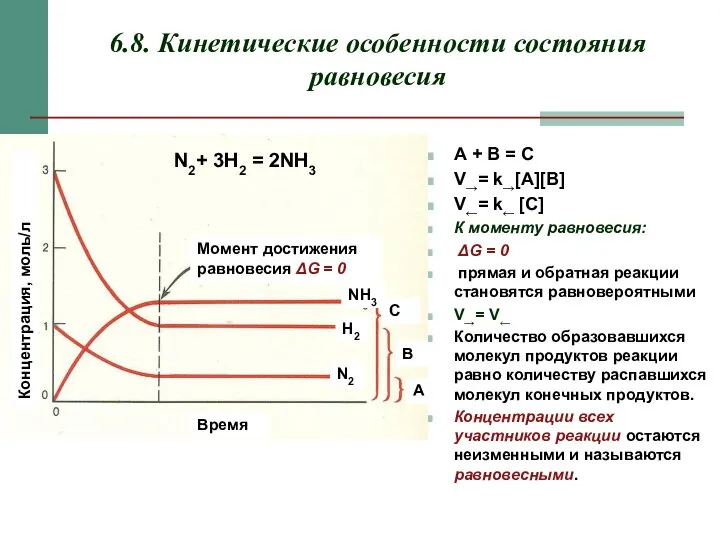
- 16. 6.8. Кинетические особенности состояния равновесия А + B = C V→= k→[A][B] V←= k← [C] К
- 17. Отношение констант скоростей прямой и обратной реакции в состоянии равновесия при фиксированной температуре есть величина постоянная
- 18. Константы равновесия некоторых реакций
- 19. Принцип Ле Шателье (1884 г.) Опыт: FeCl3 +6KCNS ⬄ K3[Fe(CNS)6] + 3KCl Оранж. Кроваво-красный Вывод: добавление
- 20. N2O4(г)⬄ 2NO2(г); Δ H = +57,2 кДж бесцвет коричнев Равно- весие Равно- весие нарушено Равно- весие
- 22. Скачать презентацию













![Принцип Ле Шателье (1884 г.) Опыт: FeCl3 +6KCNS ⬄ K3[Fe(CNS)6] +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394967/slide-18.jpg)

 Общие электронные конфигурации элементов главных подгрупп
Общие электронные конфигурации элементов главных подгрупп Аминокислоты. Свойства
Аминокислоты. Свойства Классификация металлов в соответствии с ионным потенциалом и параметром мягкости
Классификация металлов в соответствии с ионным потенциалом и параметром мягкости Сульфаниламидные препараты. (Тема 5)
Сульфаниламидные препараты. (Тема 5) Химия. 8 класс. Подготовка к контрольной работе
Химия. 8 класс. Подготовка к контрольной работе Атомный уровень. Химия простых веществ. Молекулярный уровень. Химия соединений. Живое субклеточный уровень
Атомный уровень. Химия простых веществ. Молекулярный уровень. Химия соединений. Живое субклеточный уровень Присадки к маслам
Присадки к маслам Периодический закон и периодическая система Д.И.Менделеева. Лекция 4
Периодический закон и периодическая система Д.И.Менделеева. Лекция 4 Презентация по Химии "Фосфор" - скачать смотреть бесплатно_
Презентация по Химии "Фосфор" - скачать смотреть бесплатно_ Химия в быту
Химия в быту Химия муравьиной кислоты
Химия муравьиной кислоты Количество вещества. Моль. Молярная масса
Количество вещества. Моль. Молярная масса Генетическая связь основных классов неорганических соединений
Генетическая связь основных классов неорганических соединений Подача питательной воды в парогенератор при запроектной аварии
Подача питательной воды в парогенератор при запроектной аварии Именные реакции в органической химии
Именные реакции в органической химии Презентация по Химии "Оксиды получение, свойства, применение" - скачать смотреть бесплатно
Презентация по Химии "Оксиды получение, свойства, применение" - скачать смотреть бесплатно Презентация по Химии "Металлическая связь" - скачать смотреть
Презентация по Химии "Металлическая связь" - скачать смотреть  Углеводы. Дисахариды и полисахариды
Углеводы. Дисахариды и полисахариды Окислительно-восстановительные реакции . Алканолы
Окислительно-восстановительные реакции . Алканолы Тяжёлая вода
Тяжёлая вода Нитраты и нитриты. Азотные удобрения
Нитраты и нитриты. Азотные удобрения ПРЕЗЕНТАЦИЯ «Химия и повседневная жизнь человека»
ПРЕЗЕНТАЦИЯ «Химия и повседневная жизнь человека»  Применение неметаллов
Применение неметаллов Бензойная кислота
Бензойная кислота Окислительно- восстановительные процессы
Окислительно- восстановительные процессы Выполнила: Смирнова Маргарита Ученица: 9-а класса
Выполнила: Смирнова Маргарита Ученица: 9-а класса Тест 1.Тип кристаллической решетки у белого фосфора…. а) молекулярный б) атомный в) ионный а) молекулярный Р4 2. У фосфора…..
Тест 1.Тип кристаллической решетки у белого фосфора…. а) молекулярный б) атомный в) ионный а) молекулярный Р4 2. У фосфора…..  Лекция 1. Топливо. Горение топлива
Лекция 1. Топливо. Горение топлива