Содержание
- 2. Модель фермента нуклеозид-фосфорилазы
- 3. Ферме́нты или энзи́мы (от лат. fermentum, греч., греч. ζύμη, ἔνζυμον — дрожжи, греч. ζύμη, ἔνζυμον —
- 4. Классификация ферментов По типу катализируемых реакций ферменты подразделяются на 6 классов согласно иерархической классификации ферментов (КФПо
- 5. Соглашения о наименовании ферментов Обычно ферменты именуют по типу катализируемой реакции, добавляя суффикс -аза к названию
- 6. Функции ферментов Ферменты — белкиФерменты — белки, являющиеся биологическими катализаторамиФерменты — белки, являющиеся биологическими катализаторами. Ферменты
- 7. Кинетические исследования Простейшим описанием кинетики односубстратных ферментативных реакций является уравнение Михаэлиса — Ментен (см. рис.). На
- 8. Кривая насыщения химической реакции, иллюстрирующая соотношение между концентрацией субстрата [S] и скоростью реакции v
- 9. Специфичность Ферменты обычно проявляют высокую специфичность по отношению к своим субстратам. Это достигается частичной комплементарностью формы,
- 10. Структура и механизм действия ферментов Активность ферментов определяется их трёхмерной структурой[3]. Как и все белки, ферменты
- 11. Модель индуцированного соответствия В 1958 г. Дениел КошландВ 1958 г. Дениел Кошланд предложил модификацию модели «ключ-замок»
- 12. Модель «ключ-замок» В 1890 г. Эмиль ФишерВ 1890 г. Эмиль Фишер предположил, что специфичность ферментов определяется
- 13. Модификации Многие ферменты после синтеза белковой цепи претерпевают модификации, без которых фермент не проявляет свою активность
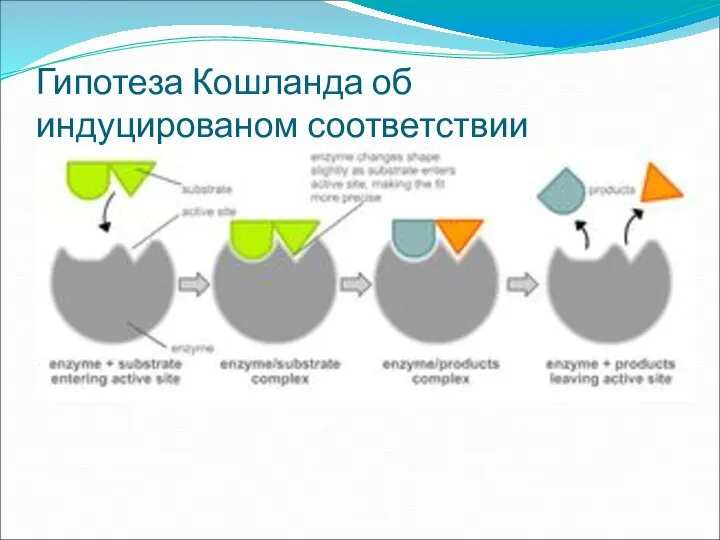
- 14. Гипотеза Кошланда об индуцированом соответствии
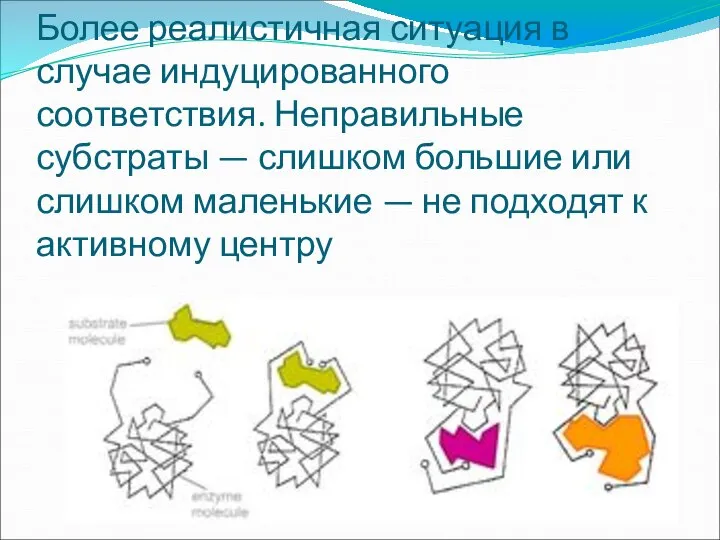
- 15. Более реалистичная ситуация в случае индуцированного соответствия. Неправильные субстраты — слишком большие или слишком маленькие —
- 16. Кофакторы ферментов Некоторые ферменты выполняют каталитическую функцию сами по себе, безо всяких дополнительных компонентов. Однако есть
- 18. Скачать презентацию
Модель фермента нуклеозид-фосфорилазы
Модель фермента нуклеозид-фосфорилазы
Ферме́нты или энзи́мы (от лат. fermentum, греч., греч. ζύμη, ἔνζυμον — дрожжи, греч.
Ферме́нты или энзи́мы (от лат. fermentum, греч., греч. ζύμη, ἔνζυμον — дрожжи, греч.
Термины «фермент» и «энзим» давно используют как синонимы (первый в основном в русской и немецкой научной литературе, второй — в англо- и франкоязычной). Наука о ферментах называется энзимологией, а не ферментологией (чтобы не смешивать корни слов латинского и греческого языков).
Классификация ферментов
По типу катализируемых реакций ферменты подразделяются на 6 классов
Классификация ферментов
По типу катализируемых реакций ферменты подразделяются на 6 классов
КФ 1: Оксидоредуктазы, катализирующие окисление или восстановление. Пример: каталаза, катализирующие окисление или восстановление. Пример: каталаза, алкогольдегидрогеназа
КФ 2: Трансферазы, катализирующие перенос химических групп с одной молекулы субстрата, катализирующие перенос химических групп с одной молекулы субстрата на другую. Среди трансфераз особо выделяют киназы, катализирующие перенос химических групп с одной молекулы субстрата на другую. Среди трансфераз особо выделяют киназы, переносящие фосфатную группу, как правило, с молекулы АТФ.
КФ 3: Гидролазы, катализирующие гидролиз, катализирующие гидролиз химических связей. Пример: эстеразы, катализирующие гидролиз химических связей. Пример: эстеразы, пепсин, катализирующие гидролиз химических связей. Пример: эстеразы, пепсин, трипсин, катализирующие гидролиз химических связей. Пример: эстеразы, пепсин, трипсин, амилаза, катализирующие гидролиз химических связей. Пример: эстеразы, пепсин, трипсин, амилаза, липопротеинлипаза
КФ 4: Лиазы, катализирующие разрыв химических связей без гидролиза с образованием двойной связи в одном из продуктов.
КФ 5: Изомеразы, катализирующие структурные или геометрические изменения в молекуле субстрата.
КФ 6: Лигазы, катализирующие образование химических связей между субстратами за счет гидролиза АТФ, катализирующие образование химических связей между субстратами за счет гидролиза АТФ. Пример: ДНК-полимераза
Будучи катализаторами, ферменты ускоряют как прямую, так и обратную реакции, поэтому, например, лиазы способны катализировать и обратную реакцию — присоединение по двойным связям.
Соглашения о наименовании ферментов
Обычно ферменты именуют по типу катализируемой реакции,
Соглашения о наименовании ферментов
Обычно ферменты именуют по типу катализируемой реакции,
Функции ферментов
Ферменты — белкиФерменты — белки, являющиеся биологическими катализаторамиФерменты — белки, являющиеся биологическими
Функции ферментов
Ферменты — белкиФерменты — белки, являющиеся биологическими катализаторамиФерменты — белки, являющиеся биологическими
Подобно всем катализаторам, ферменты ускоряют как прямую, так и обратную реакцию, понижая энергию активацииПодобно всем катализаторам, ферменты ускоряют как прямую, так и обратную реакцию, понижая энергию активации процесса. Химическое равновесиеПодобно всем катализаторам, ферменты ускоряют как прямую, так и обратную реакцию, понижая энергию активации процесса. Химическое равновесие при этом не смещается ни в прямую, ни в обратную сторону. Отличительной особенностью ферментов по сравнению с небелковыми катализаторами является их высокая специфичностьПодобно всем катализаторам, ферменты ускоряют как прямую, так и обратную реакцию, понижая энергию активации процесса. Химическое равновесие при этом не смещается ни в прямую, ни в обратную сторону. Отличительной особенностью ферментов по сравнению с небелковыми катализаторами является их высокая специфичность — константа связыванияПодобно всем катализаторам, ферменты ускоряют как прямую, так и обратную реакцию, понижая энергию активации процесса. Химическое равновесие при этом не смещается ни в прямую, ни в обратную сторону. Отличительной особенностью ферментов по сравнению с небелковыми катализаторами является их высокая специфичность — константа связывания некоторых субстратов с белком может достигать 10−10 моль/л и менее. См. также Каталитически совершенный фермент
Ферменты широко используются в народном хозяйстве — пищевой, текстильной промышленности, в фармакологии.
Кинетические исследования
Простейшим описанием кинетики односубстратных ферментативных реакций является уравнение Михаэлиса
Кинетические исследования
Простейшим описанием кинетики односубстратных ферментативных реакций является уравнение Михаэлиса
Кривая насыщения химической реакции, иллюстрирующая соотношение между концентрацией субстрата [S] и
Кривая насыщения химической реакции, иллюстрирующая соотношение между концентрацией субстрата [S] и
Специфичность
Ферменты обычно проявляют высокую специфичность по отношению к своим субстратам.
Специфичность
Ферменты обычно проявляют высокую специфичность по отношению к своим субстратам.
Структура и механизм действия ферментов
Активность ферментов определяется их трёхмерной структурой[3].
Как
Структура и механизм действия ферментов
Активность ферментов определяется их трёхмерной структурой[3].
Как
Чтобы катализировать реакцию, фермент должен связаться с одним или несколькими субстратами. Белковая цепь фермента сворачивается таким образом, что на поверхности глобулы образуется щель, или впадина, где связываются субстраты. Эта область называется сайтом связывания субстрата. Обычно он совпадает с активным центром фермента или находится вблизи него. Некоторые ферменты содержат также сайты связывания кофакторов или ионов металлов.
У некоторых ферментов есть сайты связывания малых молекул, они могут быть субстратами или продуктами метаболического пути, в который входит фермент. Они уменьшают или увеличивают активность фермента, что создает возможность для обратной связи.
Для активных центров некоторых ферментов характерно явление кооперативности.
Модель индуцированного соответствия
В 1958 г. Дениел КошландВ 1958 г. Дениел
Модель индуцированного соответствия
В 1958 г. Дениел КошландВ 1958 г. Дениел
Модель «ключ-замок»
В 1890 г. Эмиль ФишерВ 1890 г. Эмиль Фишер
Модель «ключ-замок»
В 1890 г. Эмиль ФишерВ 1890 г. Эмиль Фишер
Модификации
Многие ферменты после синтеза белковой цепи претерпевают модификации, без которых
Модификации
Многие ферменты после синтеза белковой цепи претерпевают модификации, без которых
Еще один распространенный тип посттранляционных модификаций — расщепление полипептидной цепи. Например, химотрипсинЕще один распространенный тип посттранляционных модификаций — расщепление полипептидной цепи. Например, химотрипсин (протеазаЕще один распространенный тип посттранляционных модификаций — расщепление полипептидной цепи. Например, химотрипсин (протеаза, участвующая в пищеваренииЕще один распространенный тип посттранляционных модификаций — расщепление полипептидной цепи. Например, химотрипсин (протеаза, участвующая в пищеварении), получается при выщеплении полипептидного участка из химотрипсиногена. Химотрипсиноген является неактивным предшественником химотрипсина и синтезируется в поджелудочной железеЕще один распространенный тип посттранляционных модификаций — расщепление полипептидной цепи. Например, химотрипсин (протеаза, участвующая в пищеварении), получается при выщеплении полипептидного участка из химотрипсиногена. Химотрипсиноген является неактивным предшественником химотрипсина и синтезируется в поджелудочной железе. Неактивная форма транспортируется в желудок, где превращается в химотрипсин. Такой механизм необходим для того, чтобы избежать расщепления поджелудочной железы и других тканей до поступления фермента в желудок. Неактивный предшественник фермента называют также «зимогеном».
Гипотеза Кошланда об индуцированом соответствии
Гипотеза Кошланда об индуцированом соответствии
Более реалистичная ситуация в случае индуцированного соответствия. Неправильные субстраты — слишком большие
Более реалистичная ситуация в случае индуцированного соответствия. Неправильные субстраты — слишком большие
Кофакторы ферментов
Некоторые ферменты выполняют каталитическую функцию сами по себе, безо
Кофакторы ферментов
Некоторые ферменты выполняют каталитическую функцию сами по себе, безо
Фермент, который требует наличия кофактора для проявления каталитической активности, но не связан с ним, называется апо-фермент. Апо-фермент в комплексе с кофактором носит название холо-фермента. Большинство кофакторов связано с ферментом нековалентными, но довольно прочными взаимодействиями. Есть и такие простетические группы, которые связаны с ферментом ковалентно, например, тиаминпирофосфат в пируватдегидрогеназе.






![Кривая насыщения химической реакции, иллюстрирующая соотношение между концентрацией субстрата [S] и скоростью реакции v](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1191114/slide-7.jpg)

![Структура и механизм действия ферментов Активность ферментов определяется их трёхмерной структурой[3].](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1191114/slide-9.jpg)




 Методы диффузионной металлизации
Методы диффузионной металлизации Основные понятия и определения. Химическая кинетика
Основные понятия и определения. Химическая кинетика Ковалентная связь
Ковалентная связь Свойства карбоновых кислот. (Лекция 4)
Свойства карбоновых кислот. (Лекция 4) Карбонові кислоти. Насичені карбонові кислоти
Карбонові кислоти. Насичені карбонові кислоти Растворы. Теория электролитической диссоциации (лекция 6)
Растворы. Теория электролитической диссоциации (лекция 6) Физические и химические явления
Физические и химические явления Откуда ты, химия ?
Откуда ты, химия ? Оксиды. Основания. Кислоты. 6 класс
Оксиды. Основания. Кислоты. 6 класс Строение атома. Периодический закон Менделеева
Строение атома. Периодический закон Менделеева Характеристики ковалентной связи .Длина связи. Энергия связи. Полярность связи
Характеристики ковалентной связи .Длина связи. Энергия связи. Полярность связи Методические рекомендации по изучению темы «Азот как простое вещество»
Методические рекомендации по изучению темы «Азот как простое вещество» Оценка образовательных достижений школьников при личностно-ориентированном обучении химии
Оценка образовательных достижений школьников при личностно-ориентированном обучении химии Маслянокислые бактерии
Маслянокислые бактерии Взаимное притяжение и отталкивание молекул. Тема 11
Взаимное притяжение и отталкивание молекул. Тема 11 Растворы электролитов
Растворы электролитов Тема 2. Электронный энергетический спектр как фундаментальная характеристика твердого тела. Перестройка энергетического спектра
Тема 2. Электронный энергетический спектр как фундаментальная характеристика твердого тела. Перестройка энергетического спектра Ферменты. Часть II
Ферменты. Часть II Применение неметаллов
Применение неметаллов Липиды. Классификация липидов
Липиды. Классификация липидов Ультразвук к в химической технологии. Лекция 5
Ультразвук к в химической технологии. Лекция 5 ГИА. Вопрос 10. Химические свойства оксидов: основных, амфотерных, кислотных
ГИА. Вопрос 10. Химические свойства оксидов: основных, амфотерных, кислотных Виды пластика, что производят и что можно переработать
Виды пластика, что производят и что можно переработать Выполнил ученик 11-б класса МОУ СОШ №41 Гандилян Армен Руководитель: Изместьева Н.Д. Красноярск 2005
Выполнил ученик 11-б класса МОУ СОШ №41 Гандилян Армен Руководитель: Изместьева Н.Д. Красноярск 2005 Лабораторный штатив
Лабораторный штатив Исследование зон коагуляции и стабилизации золей электролитами. Работа 6
Исследование зон коагуляции и стабилизации золей электролитами. Работа 6 студентка группы ГЭ-1-07 факультета ЭиУ Малышева Е.И. «Биомасса – альтернативный источник энергии» студентка группы ГЭ-1-07 фак
студентка группы ГЭ-1-07 факультета ЭиУ Малышева Е.И. «Биомасса – альтернативный источник энергии» студентка группы ГЭ-1-07 фак Ерітінділер. Ерітінділердің химиялық теориясы
Ерітінділер. Ерітінділердің химиялық теориясы