Содержание
- 2. Растворы электролитов Электролиты – вещества с ионной проводимостью. Это растворы солей, кислоты, оснований, расплавы солей. I
- 3. II закон Рауля ∆Tкип =iEm ∆Tзам=iKm Закон Вант-Гоффа ∆Pосм=icRT
- 4. i – поправочный коэффициент изотонический i – зависит от: природы раствора концентрации раствора i>1 для растворов
- 5. Теория электролитической диссоциации Аррениуса Распад молекул электролитов на ионы в среде растворителя под действием молекул растворителя.
- 6. Количественная характеристика процесса диссоциации выражается степенью электролитической диссоциации – α.
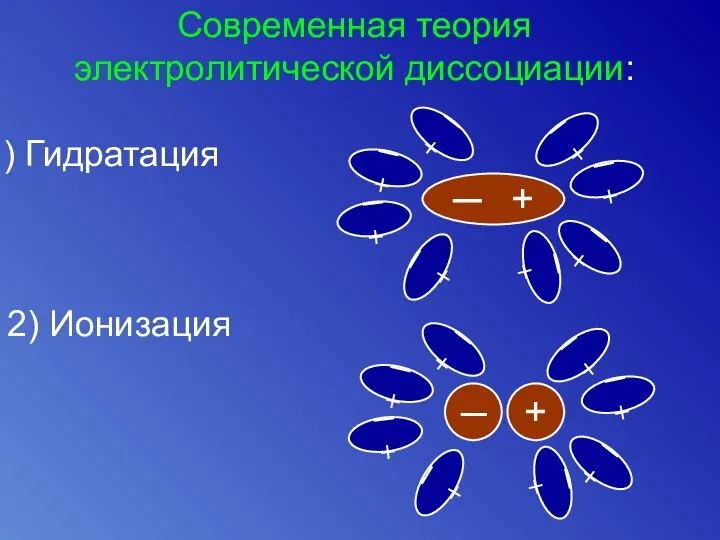
- 7. Современная теория электролитической диссоциации: Гидратация ─ + ─ + ─ + ─ + ─ + ─
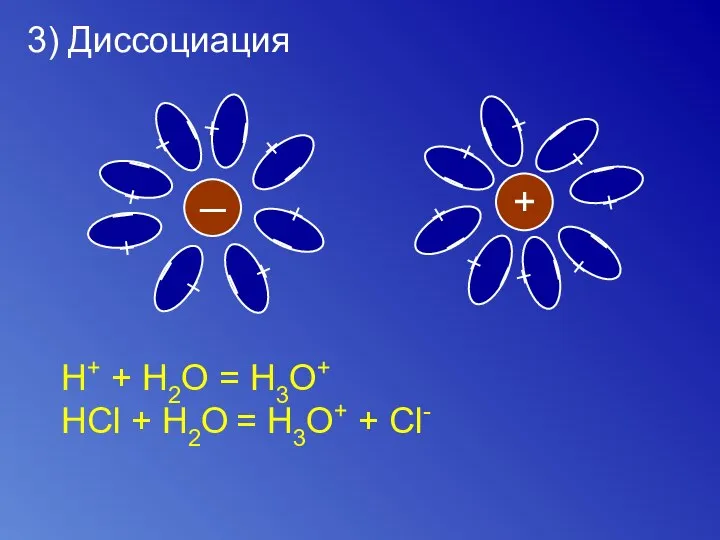
- 8. 3) Диссоциация ─ + ─ + ─ + ─ + ─ + ─ + ─ +
- 9. Способность гидратироваться зависит: - от природы ионов от заряда иона от размера иона от строения электронной
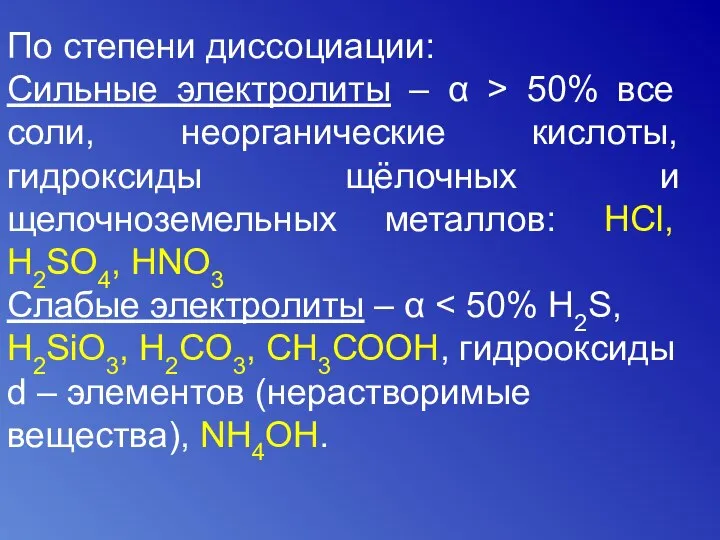
- 10. По степени диссоциации: Сильные электролиты – α > 50% все соли, неорганические кислоты, гидроксиды щёлочных и
- 11. Растворы слабых электролитов Чем больше Кд тем сильнее диссоциирует электролит. NH4OH = NH4+ + OH-
- 12. Закон разбавления Освальда α С – разбавлением раствора степень диссоциации увеличивается. с – молярная концентрация электролита
- 13. Растворы сильных электролитов NaCl i≈2 NaCl → Na+ + Cl- от наличия одноимённых ионов СН3COOH ↔
- 14. 1907 Льюис → активность (а) → эффективная концентрация ионов. а = f·c; f = 1 a
- 15. Коэффициент активности зависит от ионной силы раствора (J). А – коэффициент пропор., зависит от вида растворителя.
- 16. (H2PO4)- ↔ H+ + (HPO4)2- (HPO4)2- ↔ H+ + PO43- K1 > K2 > K3
- 17. Ионное произведение воды. pH – растворов. Н2О ↔ H+ + ОН- Kводы = [H+][OH-] = 1,1⋅10-14
- 18. Нейтральный раствор [H+] = 10-7 г-ион/л [OH-] = 10-7 г-ион/л Кислый раствор [H+] > 10-7 г-ион/л
- 19. В нейтральной среде: [H+] = 10-7 -Lg[10-7] = 7 → pH = 7 В кислой среде:
- 20. Пример 1: [OH-] = 10-11 pH = ? [H+][OH-] = 10-14 x⋅10-11 = 10-14 [H+] =
- 22. Скачать презентацию











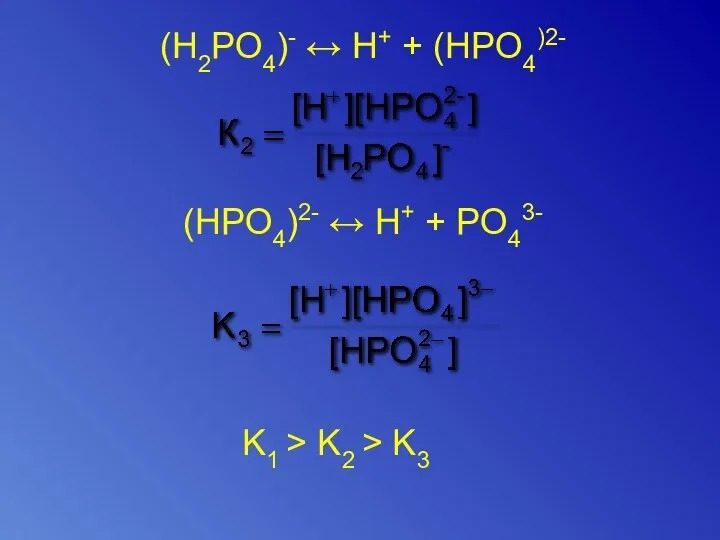

![Нейтральный раствор [H+] = 10-7 г-ион/л [OH-] = 10-7 г-ион/л Кислый](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408383/slide-17.jpg)
![В нейтральной среде: [H+] = 10-7 -Lg[10-7] = 7 → pH](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408383/slide-18.jpg)
![Пример 1: [OH-] = 10-11 pH = ? [H+][OH-] = 10-14](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408383/slide-19.jpg)
 История открытия бензола Впервые бензол описал немецкий химик Иоганн Глаубер. Он получил это соединение в 1649 г. в результате пе
История открытия бензола Впервые бензол описал немецкий химик Иоганн Глаубер. Он получил это соединение в 1649 г. в результате пе Значення хімії у розв’язанні сировинної проблеми
Значення хімії у розв’язанні сировинної проблеми  Аммиак. Строение молекулы. Водородная связь
Аммиак. Строение молекулы. Водородная связь Выращивание кристаллов методом Чохральского
Выращивание кристаллов методом Чохральского Лекція № 2 Білкові системи: характеристика, використання фізико-хімічних властивостей у виробництві харчових продуктів
Лекція № 2 Білкові системи: характеристика, використання фізико-хімічних властивостей у виробництві харчових продуктів Исследовательская работа «Химические свойства чая»
Исследовательская работа «Химические свойства чая» Ртуть. Нахождение в природе. Применение
Ртуть. Нахождение в природе. Применение Презентация по Химии "Продукти харчування" - скачать смотреть бесплатно
Презентация по Химии "Продукти харчування" - скачать смотреть бесплатно Пищевая микробиология. Превращения азотсодержащих веществ
Пищевая микробиология. Превращения азотсодержащих веществ Наглядное пособие «Динамические модели». Химическое равновесие в растворах
Наглядное пособие «Динамические модели». Химическое равновесие в растворах Органические вещества. Белки, аминокислоты
Органические вещества. Белки, аминокислоты Презентация по Химии "Как определить качество меда" - скачать смотреть
Презентация по Химии "Как определить качество меда" - скачать смотреть  Презентация по Химии "Краткий очерк истории развития химии." - скачать смотреть бесплатно
Презентация по Химии "Краткий очерк истории развития химии." - скачать смотреть бесплатно Механизмы образования ковалентной связи
Механизмы образования ковалентной связи Презентация по Химии "Азотсодержащие органические соединения" - скачать смотреть
Презентация по Химии "Азотсодержащие органические соединения" - скачать смотреть  Курс хімії за 11 клас
Курс хімії за 11 клас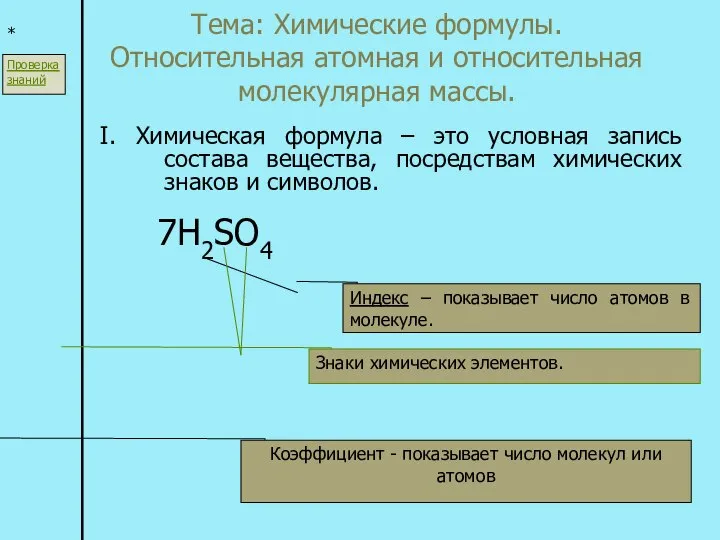 Химические формулы. Относительная атомная и относительная молекулярная массы
Химические формулы. Относительная атомная и относительная молекулярная массы Кинетика химических реакций. (Лекция 12)
Кинетика химических реакций. (Лекция 12) Презентация по Химии "Чипсы - вред или польза?" - скачать смотреть
Презентация по Химии "Чипсы - вред или польза?" - скачать смотреть  Сейсморазведка
Сейсморазведка Синтез олигомеров этиленгликоля и терефталевой кислоты
Синтез олигомеров этиленгликоля и терефталевой кислоты Проектирование стадии окисления этилбензола
Проектирование стадии окисления этилбензола Химические свойства металлов Урок химии в 11 классе
Химические свойства металлов Урок химии в 11 классе Решение задач. Подготовка к контрольной работе по химии
Решение задач. Подготовка к контрольной работе по химии Строение электронных оболочек атомов
Строение электронных оболочек атомов Олово и свинец. (Лекция 2)
Олово и свинец. (Лекция 2) Кам'яне вугілля Тверда горюча корисна копалина, один з видів вугілля викопного, проміжний між бурим вугіллям і антрацитом
Кам'яне вугілля Тверда горюча корисна копалина, один з видів вугілля викопного, проміжний між бурим вугіллям і антрацитом  ГСМ - горюче-смазочные материалы
ГСМ - горюче-смазочные материалы