Промышленное использование пропилена
Пропилен в промышленности применяется, в основном, для синтеза полипропилена(62 %
процента всего выпускаемого объема). Также из него получают кумол, окись пропилена, акрилонитрил, изопропанол, глицерин, масляный альдегид.
В настоящее время мировые мощности по выпуску пропилена составляют около 70 млн тонн в год. По прогнозам специалистов, потребность в пропилене в ближайшем будущем будет существенно превышать объемы его производства, причем, ожидается, что к 2010 году объем его мирового выпуска достигнет 90 млн тонн.




 № 15. Олигосахариды ПОЛИСАХАРИДЫ.
№ 15. Олигосахариды ПОЛИСАХАРИДЫ.  Перекисное окисление липидов. Характеристика, продукты, биологическая и патофизиологическая роль
Перекисное окисление липидов. Характеристика, продукты, биологическая и патофизиологическая роль Изотопная геохимия. U-Pb метод
Изотопная геохимия. U-Pb метод Реакции ионного обмена
Реакции ионного обмена Методи очищення води в побуті
Методи очищення води в побуті Фуллерены Квазикристаллы Использование кристаллов
Фуллерены Квазикристаллы Использование кристаллов Хроматография. Классификации хроматографических методов
Хроматография. Классификации хроматографических методов Обобщение по типам химических реакций
Обобщение по типам химических реакций Химия и биохимия игристых вин
Химия и биохимия игристых вин Углеродистые конструкционные стали
Углеродистые конструкционные стали Методические проблемы преподавания органической химии и ее основные теоретические понятия
Методические проблемы преподавания органической химии и ее основные теоретические понятия Наукові напрямки практичної реалізації принципів «Зеленої» хімії
Наукові напрямки практичної реалізації принципів «Зеленої» хімії Загрязнение почв пестицидами. Проблемы и решения
Загрязнение почв пестицидами. Проблемы и решения Предмет биоорганической химии. Классификация, строение, реакционная способность органических соединений
Предмет биоорганической химии. Классификация, строение, реакционная способность органических соединений Смолы и бальзамы. Воски и структурообразующие вещества в косметическом производстве
Смолы и бальзамы. Воски и структурообразующие вещества в косметическом производстве Презентация Кремень –камень 1824г.Я. Берцелиус
Презентация Кремень –камень 1824г.Я. Берцелиус Выращивание кристаллов в домашних условиях
Выращивание кристаллов в домашних условиях Нуклеиновые кислоты (строение, свойства и синтез). Тема 14
Нуклеиновые кислоты (строение, свойства и синтез). Тема 14 Метасоматический процесс
Метасоматический процесс Измеритель концентрации асфальтенов в нефти с погружной решёткой Брэгга
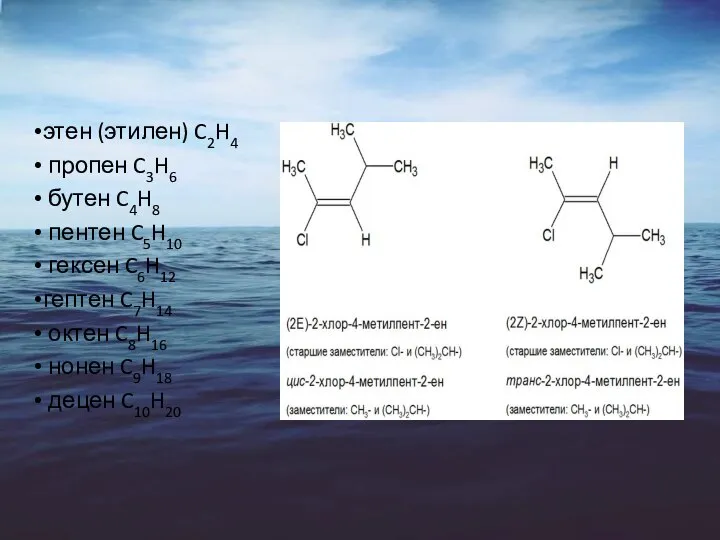
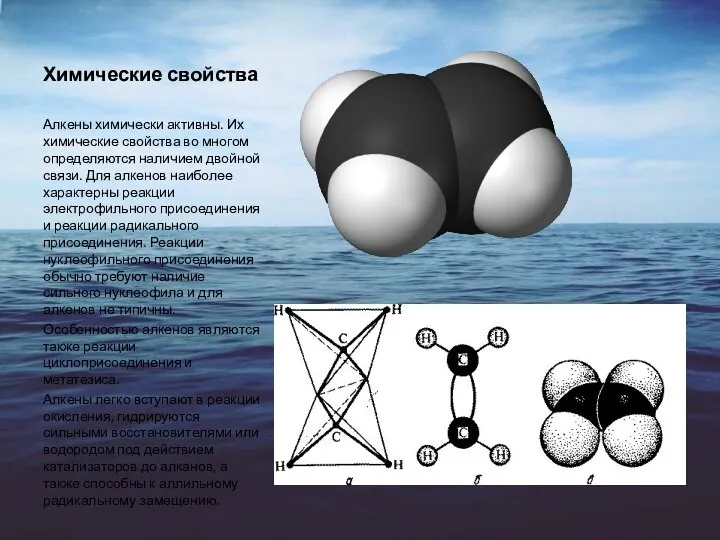
Измеритель концентрации асфальтенов в нефти с погружной решёткой Брэгга Непредельные углеводороды
Непредельные углеводороды Бензофураны и бензотиофены. Общие методы синтеза
Бензофураны и бензотиофены. Общие методы синтеза Алкины. Ацетилены
Алкины. Ацетилены Презентація на тему Карбонові кислоти Підготував студент групи ФК-44-I Галюк Юрій
Презентація на тему Карбонові кислоти Підготував студент групи ФК-44-I Галюк Юрій  Сульфиты. Сульфаты. Кислотные дожди
Сульфиты. Сульфаты. Кислотные дожди Галогены в природе. Хлор, бром, иод
Галогены в природе. Хлор, бром, иод Направление окислительно-восстановительного процесса
Направление окислительно-восстановительного процесса Буферные растворы. Буферная емкость
Буферные растворы. Буферная емкость