Содержание
- 3. ТЕМА УРОКА : АЛКЕНЫ. СТРОЕНИЕ, НОМЕНКЛАТУРА,ИЗОМЕРИЯ, ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА АЛКЕНОВ. АЛКЕНЫ- ЭТО УГЛЕВОДОРОДЫ НЕЦИКЛИЧЕСКОГО СТРОЕНИЯ,
- 4. Гомологический ряд этилена Названия алкенов по системати- ческой номенклатуре образуются от названий соответствующих алканов (с тем
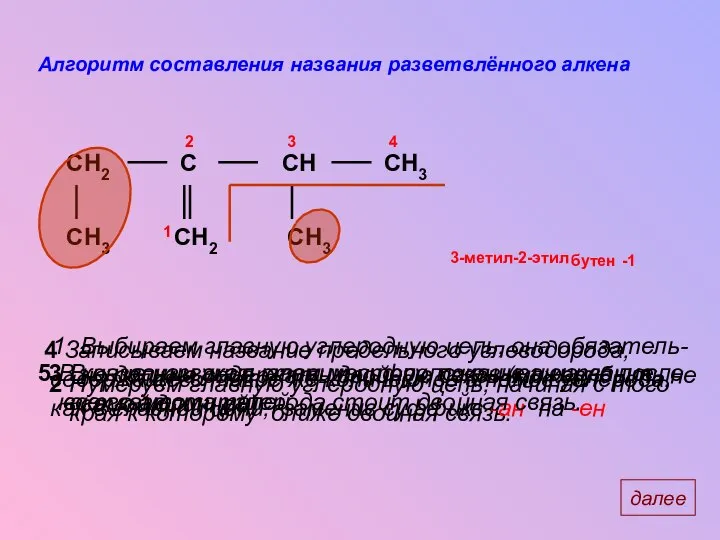
- 5. Алгоритм составления названия разветвлённого алкена СH3 CH2 C CH CH2 СH3 СH3 Выбираем главную углеродную цепь,
- 6. Строение этилена В молекуле этилена между атомами углерода образуется двойная связь, которая является сочетанием σ- и
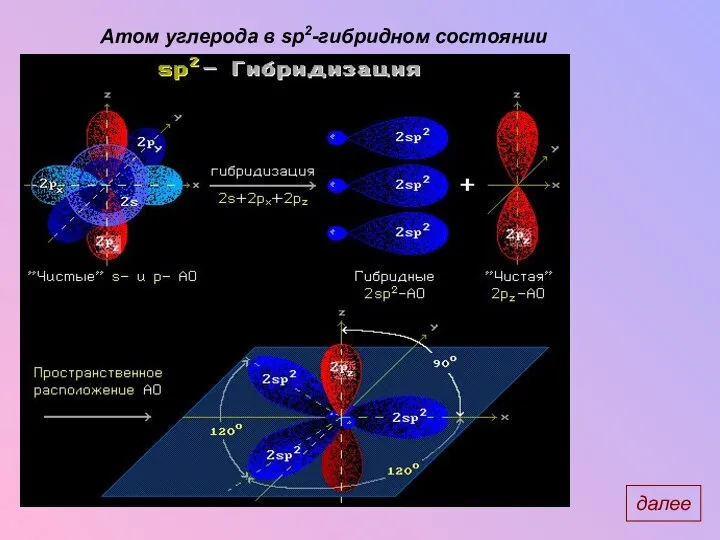
- 7. Атом углерода в sp2-гибридном состоянии далее
- 8. Образование молекулы этилена далее
- 9. π-Связи образуются между атомами, уже соединенными σ-связью. Эта связь слабее σ-связи из-за менее полного перекрывания р-орбиталей.
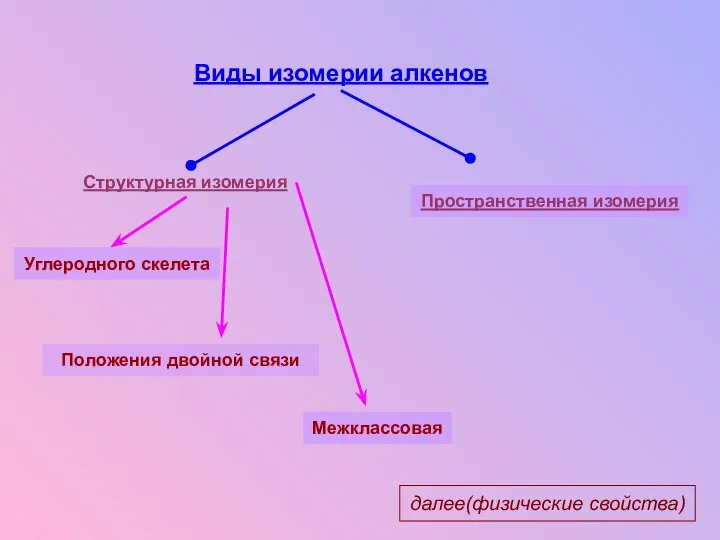
- 10. Виды изомерии алкенов Структурная изомерия Углеродного скелета Положения двойной связи Межклассовая Пространственная изомерия далее(физические свойства)
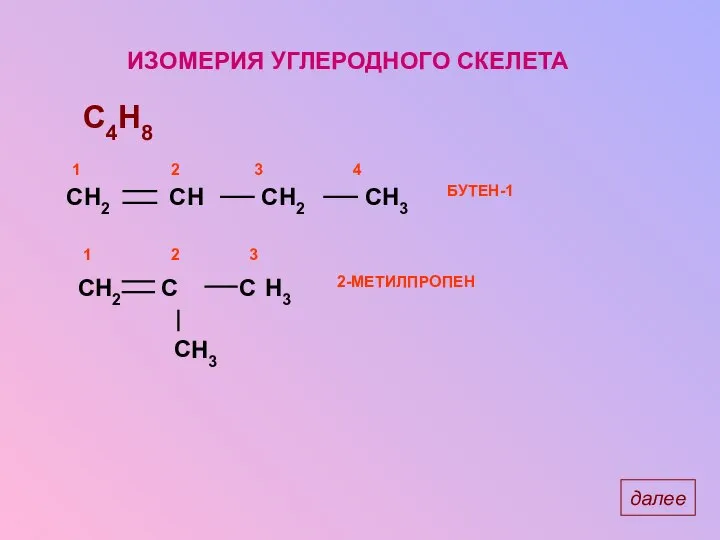
- 11. ИЗОМЕРИЯ УГЛЕРОДНОГО СКЕЛЕТА C4H8 H2 H3 H3 далее
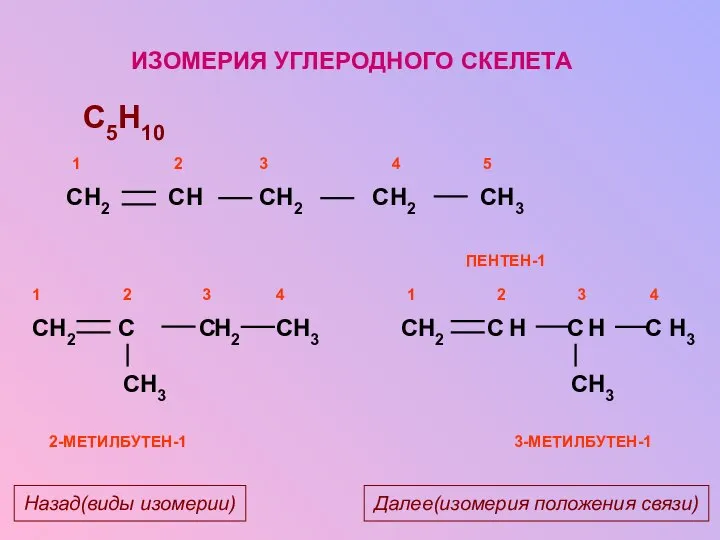
- 12. ИЗОМЕРИЯ УГЛЕРОДНОГО СКЕЛЕТА C5H10 H2 H3 H3 2-МЕТИЛБУТЕН-1 H2 H H H3 H2 H3 3-МЕТИЛБУТЕН-1 Далее(изомерия
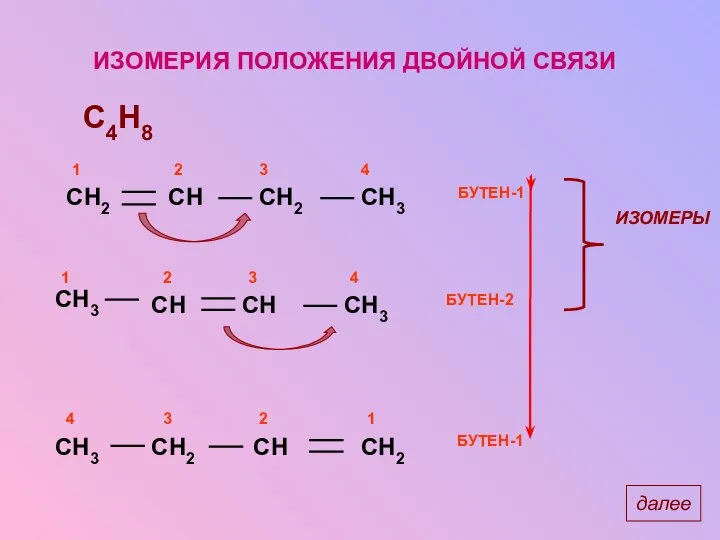
- 13. ИЗОМЕРИЯ ПОЛОЖЕНИЯ ДВОЙНОЙ СВЯЗИ C4H8 далее
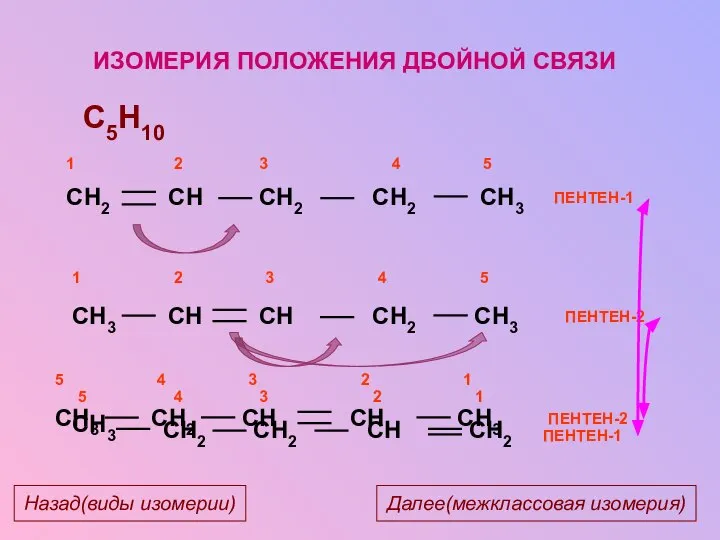
- 14. ПЕНТЕН-2 C5H10 ПЕНТЕН-1 ИЗОМЕРИЯ ПОЛОЖЕНИЯ ДВОЙНОЙ СВЯЗИ ПЕНТЕН-2 ПЕНТЕН-1 Далее(межклассовая изомерия) Назад(виды изомерии)
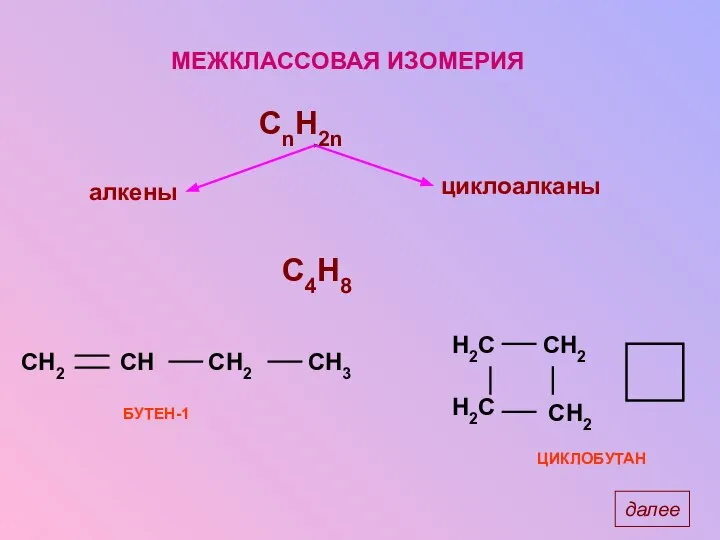
- 15. МЕЖКЛАССОВАЯ ИЗОМЕРИЯ C4H8 БУТЕН-1 ЦИКЛОБУТАН далее
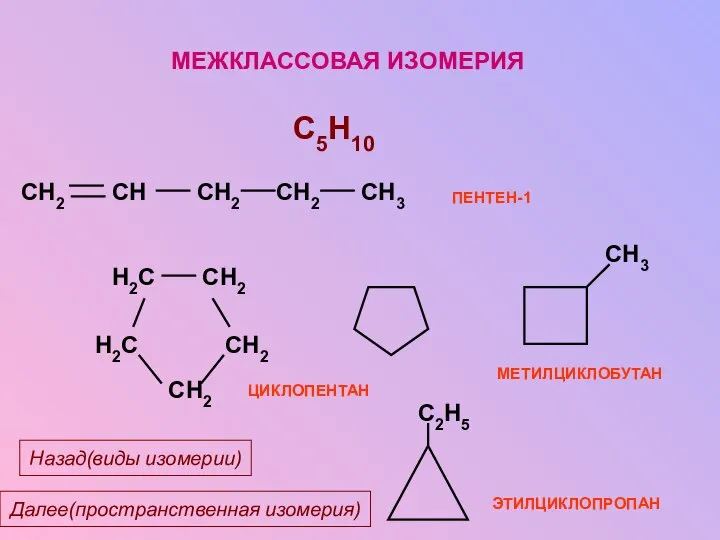
- 16. МЕЖКЛАССОВАЯ ИЗОМЕРИЯ C5H10 ЭТИЛЦИКЛОПРОПАН Далее(пространственная изомерия) Назад(виды изомерии)
- 17. НОМЕНКЛАТУРА АЛКЕНОВ Пространственная изомерия далее(физические свойства) Назад(виды изомерии)
- 18. Физические свойства алкенов закономерно изменяются в гомологическом ряду: от С2Н4 до С4Н8 – газы, начиная с
- 19. Химические свойства алкенов Химические свойства алкенов определяются строением и свойствами двойной связи С=С, которая значительно активнее
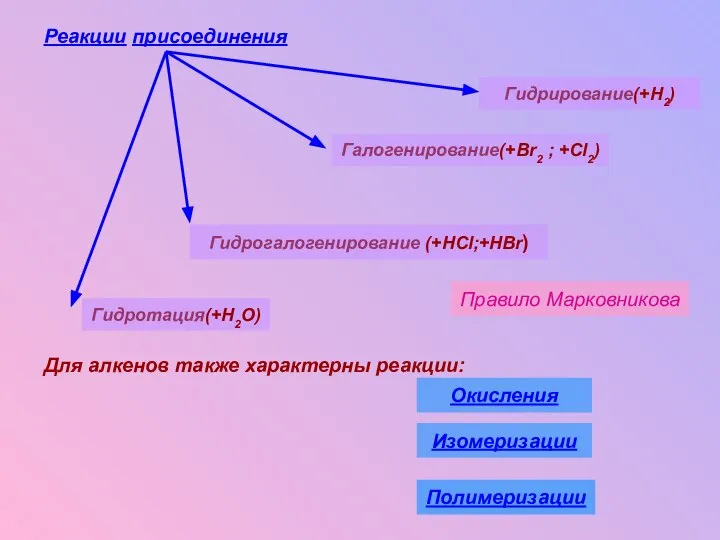
- 20. Реакции присоединения Для алкенов также характерны реакции: Правило Марковникова Гидрирование(+H2) Галогенирование(+Br2 ; +Cl2) Гидрогалогенирование (+HCl;+HBr) Гидротация(+H2O)
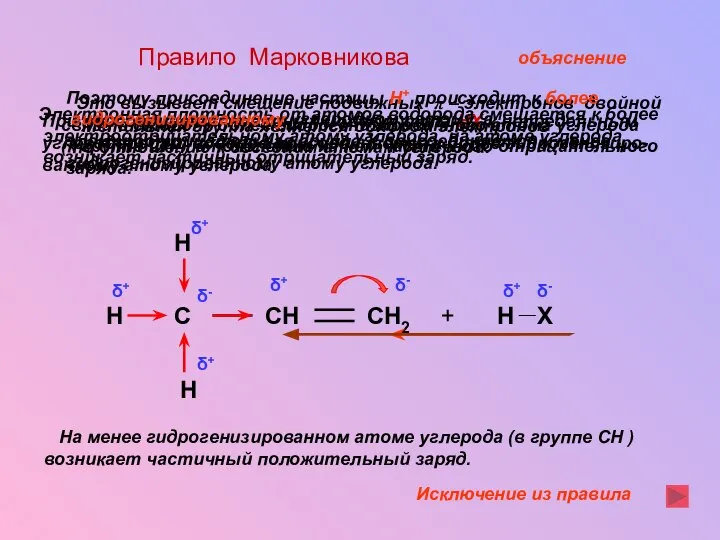
- 21. Правило Марковникова При присоединении полярных молекул типа НХ к непредельным углеводородам, водород присоединяется к более гидрогенизиро-
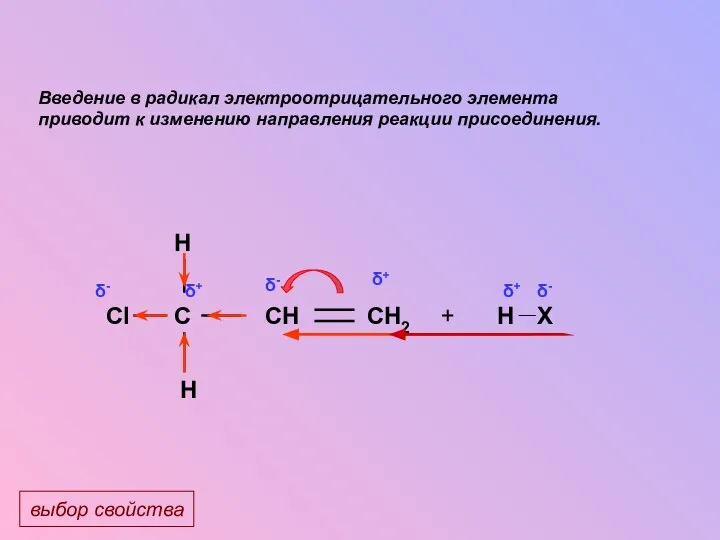
- 22. H Cl C CH2 CH H Введение в радикал электроотрицательного элемента приводит к изменению направления реакции
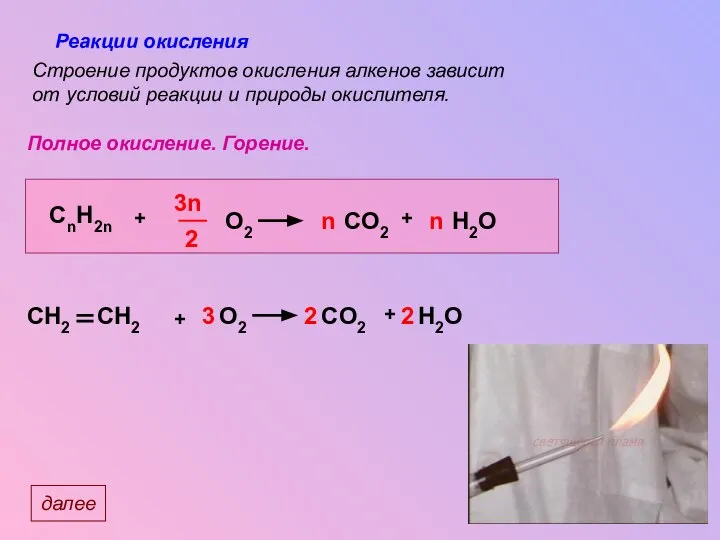
- 23. Реакции окисления Полное окисление. Горение. Строение продуктов окисления алкенов зависит от условий реакции и природы окислителя.
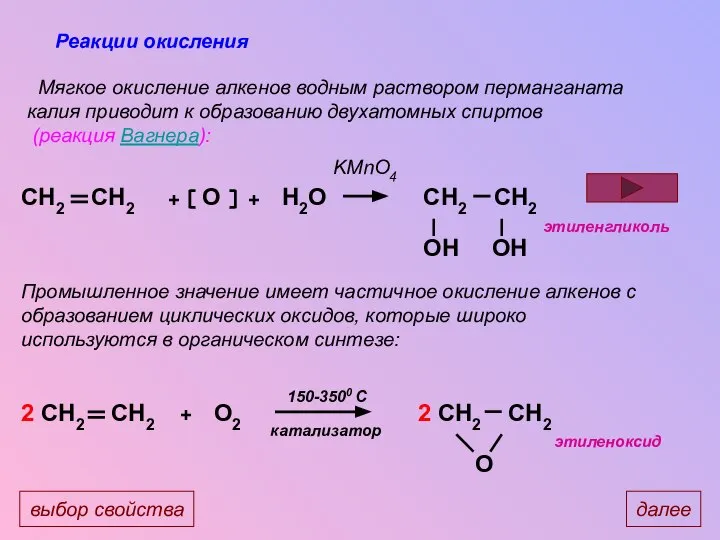
- 24. Реакции окисления Мягкое окисление алкенов водным раствором перманганата калия приводит к образованию двухатомных спиртов (реакция Вагнера):
- 25. далее(гидрирование) выбор свойства Реакция Вагнера (качественная реакция)
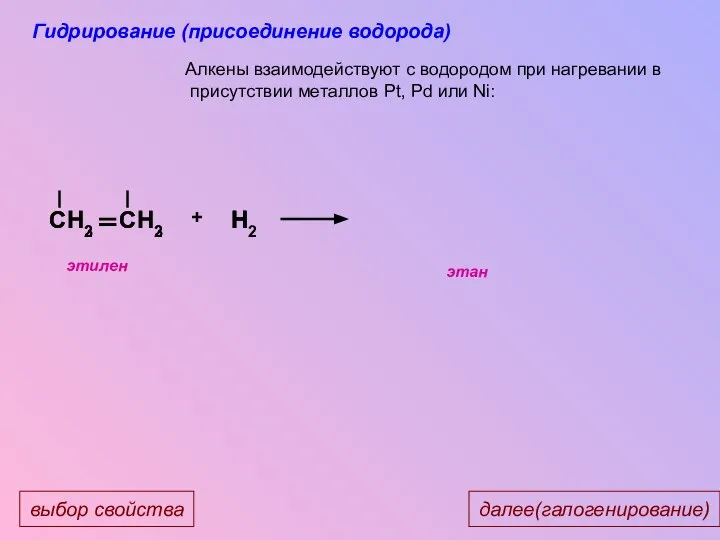
- 26. CH3 CH3 CH2 CH2 H H2 H + Алкены взаимодействуют с водородом при нагревании в присутствии
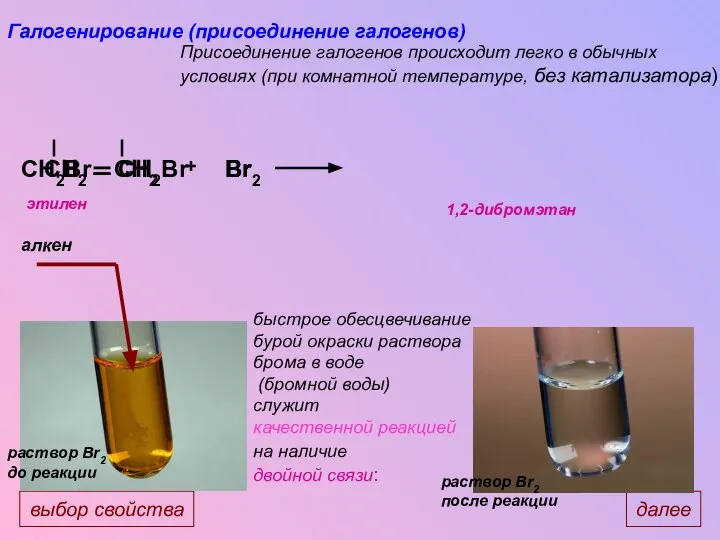
- 27. CH2 CH2 CH2Br CH2Br Br Br2 Br + Галогенирование (присоединение галогенов) Присоединение галогенов происходит легко в
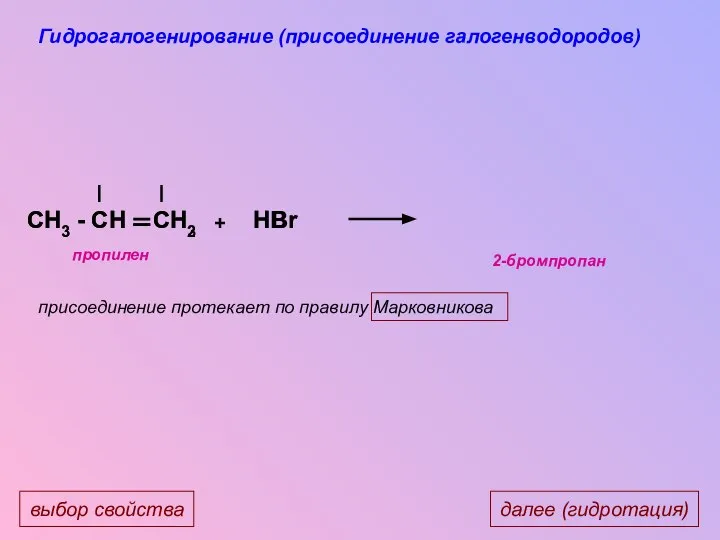
- 28. CH3 - CH CH2 CH3 - CH CH3 H HBr Br + далее (гидротация) выбор свойства
- 29. CH3 - CH CH2 CH3 - CH CH3 H H2O OH + далее (изомеризация) выбор свойства
- 30. Реакции изомеризации Алкены вступают в реакцию изомеризации при нагревании в присутствии катализаторов (Al2O3). Изомеризация алкенов приводит
- 31. Реакции полимеризации Полимеризация – реакция образования высокомолекулярного соединения (полимера) путем последовательного присоединения молекул низкомолекулярного вещества (мономера)
- 33. Скачать презентацию













 Презентация Вещества и их свойства
Презентация Вещества и их свойства Ароматические углеводороды, строение, изомерия, номенклатура
Ароматические углеводороды, строение, изомерия, номенклатура Коллоидная химия наночастиц
Коллоидная химия наночастиц Тотығутотықсыздану титрлеу әдістері. Дәріс № 7
Тотығутотықсыздану титрлеу әдістері. Дәріс № 7 Органічні сполуки: ліпіди
Органічні сполуки: ліпіди Металлические стёкла (аморфные металлы)
Металлические стёкла (аморфные металлы) Химическая связь
Химическая связь Пентозофосфатный цикл
Пентозофосфатный цикл Природный и синтетический каучуки
Природный и синтетический каучуки Интеллектуальная игра «Брейн-ринг
Интеллектуальная игра «Брейн-ринг Зависимость знака заряда белка от pH
Зависимость знака заряда белка от pH Генетическая связь между классами веществ
Генетическая связь между классами веществ Аммиак. Строение атома азота
Аммиак. Строение атома азота Кислота
Кислота ПРИРОДНЫЕ ГОРЮЧИЕ И НЕФТЯНЫЕ ПОПУТНЫЕ ГАЗЫ
ПРИРОДНЫЕ ГОРЮЧИЕ И НЕФТЯНЫЕ ПОПУТНЫЕ ГАЗЫ  Презентация по Химии "«Основания»" - скачать смотреть
Презентация по Химии "«Основания»" - скачать смотреть  Концентрация кобальта
Концентрация кобальта Открытие водорода
Открытие водорода Салыстырмалы тығыздығы мен элементтердің массалық үлестері бойынша газ күйіндегі заттардың молекулалық формулаларын табу
Салыстырмалы тығыздығы мен элементтердің массалық үлестері бойынша газ күйіндегі заттардың молекулалық формулаларын табу Производство бензина
Производство бензина L’introduction a la biochimie. La structure et les proprietes des proteines
L’introduction a la biochimie. La structure et les proprietes des proteines Презентация по Химии "Биополимеры" - скачать смотреть
Презентация по Химии "Биополимеры" - скачать смотреть  The way to prepare gold clusters - Every atom makes a difference
The way to prepare gold clusters - Every atom makes a difference Природні гази
Природні гази Электрохимическая коррозия.
Электрохимическая коррозия. «Предмет органической химии. Особенности органических веществ». По учебнику О. С. Габриеляна. 9 класс
«Предмет органической химии. Особенности органических веществ». По учебнику О. С. Габриеляна. 9 класс Хром. Основні характеристики
Хром. Основні характеристики Моделирование процесса приготовления раствора уксусной кислоты различной концентрации
Моделирование процесса приготовления раствора уксусной кислоты различной концентрации