Содержание
- 2. Электронның тасымалдануымен жүретін тотығу-тотықсыздану реакцияларына негізделген титриметия әдісі редоксиметрия (оксиметрия) деп аталады. Бұл әдістер алынған титранттың
- 3. Тотықтырғыш пен тотықсыздандырғыштың негізгі сипатамаларының бірі – олардың эквиваленттік массалары мен тотығу-тотықсыздану потенциалдарының шамалары: мұнда
- 4. ТТР өткізу барысында сол реакцияның ЭҚК шамасы оған қатысатын тотықтырғыш пен тотықсыздандырғыштың потенциалдарының айырмасына тең: Реакция
- 5. ТТР өздігінен жүруі бос Гиббс энергиясының шамасымен анықталады, ол сол реакцияның тепе-теңдік контантасымен байланысты: Реакция өздігінен
- 6. Тотықтырғыш не тотықсыздандырғыштың потенциалдары температураға, концентрацияға тәуелділіктері Нернст теңдеуімен сипатталанады:
- 7. МЫСАЛЫ: Тотықсыздандырғыштың стандартық потенциалы: Тотықтырғыштың стандартық потенциалы: яғни реакцияның ЭҚК = 1,51 – 0,771 = 0,739В
- 8. Редоксиметрия әдістерін тура, кері және жанама титрлеу жолдарымен өткізуге болады. Тотығу-тотықсыздану титрлеу әдістерінде Э.Н. бақылау үшін
- 9. тотыққан түрі тотықсызданған түрі Индикаторлық жүйенің потенциалы Нернст теңдеуімен сипатталанады:
- 10. Сонда егер индикатордың бір түрінің концентрациясы 10 есе арттса, сол кезде ерітіндіде оның бояуының өзгеруі байқалады:
- 11. Осыдан, индикатордың бояуының ауысу аймағын алуға болады:
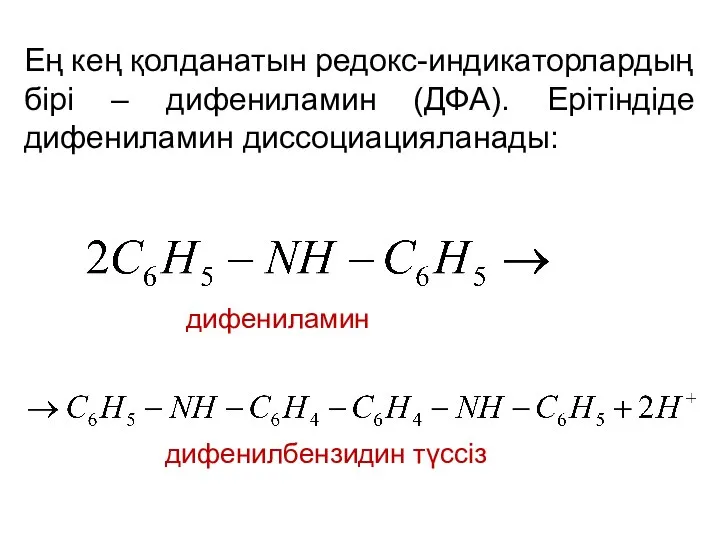
- 12. Ең кең қолданатын редокс-индикаторлардың бірі – дифениламин (ДФА). Ерітіндіде дифениламин диссоциацияланады: дифениламин дифенилбензидин түссіз
- 13. Әрі қарай тотықтырғыштың әсерінен ДФА күлгін дифенилбензидинге (ДФБ) дейін тотығады: дифенилбензидин түссіз (тотыққан түрі) дифенилбензидин күлгін
- 14. ДФА индикатордың бояуының ауысу аймағын есептегенде: Сонда ДФА индикаторының бояуының ауысу аймағы потенциал шамаларының келесі аймағында
- 16. Скачать презентацию












 Коллоидное состояние вещества
Коллоидное состояние вещества Презентация по Химии "Спирты" - скачать смотреть _
Презентация по Химии "Спирты" - скачать смотреть _ Вторая фаза метаболизма ксенобиотиков и эндогенных соединений
Вторая фаза метаболизма ксенобиотиков и эндогенных соединений Диаграмма состояния железо–углерод
Диаграмма состояния железо–углерод Непредельные углеводороды
Непредельные углеводороды Алкены.10 класс
Алкены.10 класс Сплавы. Свойства сплавов
Сплавы. Свойства сплавов Химическая технология органических веществ
Химическая технология органических веществ Алкины
Алкины Начало нанотехнологической эры. Фуллерены
Начало нанотехнологической эры. Фуллерены Фазовое равновесие в насыщенном растворе малорастворимого электролита
Фазовое равновесие в насыщенном растворе малорастворимого электролита Инсулин гормон жизни
Инсулин гормон жизни  Роль химии в сохранении окружающей среды
Роль химии в сохранении окружающей среды Биогеохимия: основные понятия, история развития, практическое значение идей биогеохимии
Биогеохимия: основные понятия, история развития, практическое значение идей биогеохимии Презентация по Химии "Органическая химия" - скачать смотреть
Презентация по Химии "Органическая химия" - скачать смотреть  Коллоидная химия
Коллоидная химия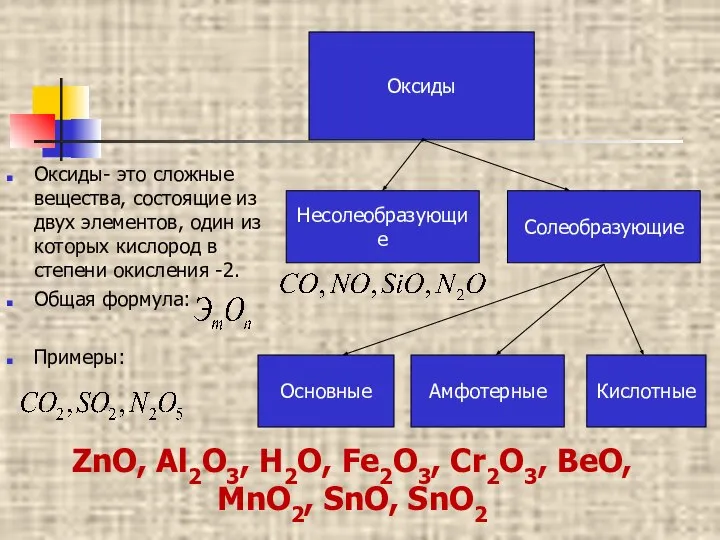 Оксиды. Классификация неорганических веществ
Оксиды. Классификация неорганических веществ Выявление уровня токсичности почв пришкольного участка и прилежащих к нему территорий
Выявление уровня токсичности почв пришкольного участка и прилежащих к нему территорий Технология кварцевого стекла
Технология кварцевого стекла Химиялық тепе-теңдік
Химиялық тепе-теңдік Біохімічний склад кормів - первинний показник їх технологічної й продуктивної можливості
Біохімічний склад кормів - первинний показник їх технологічної й продуктивної можливості Стекла. Структура и свойства
Стекла. Структура и свойства Емтихан сұрақтары
Емтихан сұрақтары Методы разделения белковых смесей. Электрофорез
Методы разделения белковых смесей. Электрофорез Косметические средства. Виды, состав и влияние на организм
Косметические средства. Виды, состав и влияние на организм Зависимость стадии конверсии метана от технологических параметров процесса в производстве метанола
Зависимость стадии конверсии метана от технологических параметров процесса в производстве метанола Получение этилена и изучение его свойств
Получение этилена и изучение его свойств Классификация неорганических веществ. Степень окисления
Классификация неорганических веществ. Степень окисления